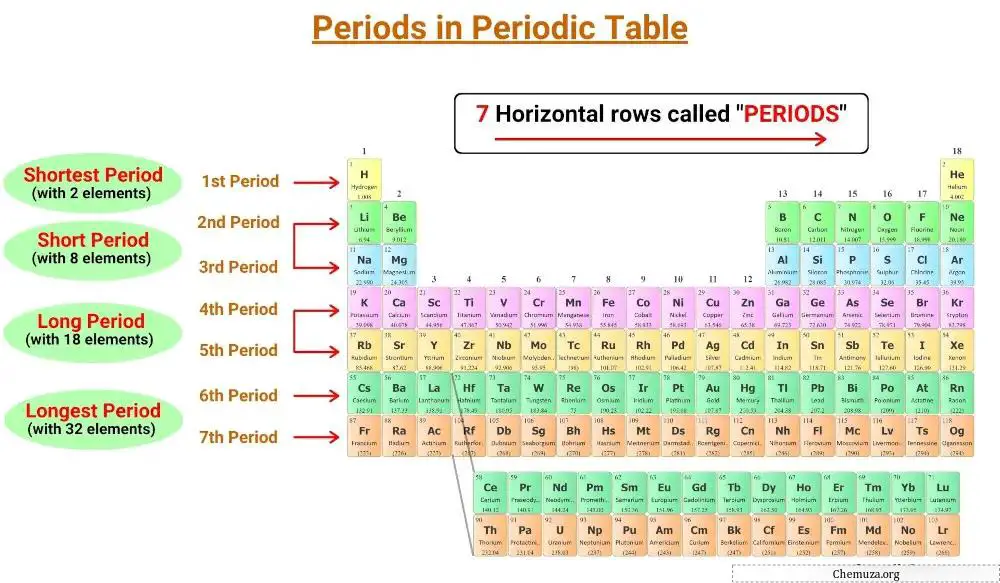
Горизонтальные линии таблицы Менделеева называются периодами, и в таблице Менделеева 7 периодов.
Элементы, находящиеся в одном периоде, имеют одинаковое количество электронных слоев.
Давайте изучим периоды в таблице Менделеева дальше.
Что такое периоды в таблице Менделеева?
В периодической таблице точки — это линии, идущие горизонтально слева направо.
Таблица Менделеева организована таким образом, что элементы со схожими свойствами сгруппированы в столбцы, называемые группами или семействами, при этом элементы одного и того же периода имеют одинаковое количество электронных оболочек.
В таблице Менделеева семь периодов, пронумерованных от 1 до 7. [1]
Количество оболочек элемента и номер его периода
Количество оболочек элемента определяет его период в таблице Менделеева.
Например, элементы периода 1 имеют только одну электронную оболочку, а элементы периода 2 — две электронные оболочки и так далее.
Эта организация помогает химикам предсказывать свойства элемента на основе его местоположения в таблице Менделеева.
Характеристики элементов по периодам
По мере продвижения по периодам таблицы Менделеева некоторые характеристики элементов изменяются предсказуемым образом. Это связано с периодическими тенденциями, наблюдаемыми в свойствах элементов.
Радиус атома:
При движении слева направо в течение определенного периода радиус атома обычно уменьшается. [2]
Это происходит потому, что число протонов в ядре увеличивается, вызывая большее притяжение между ядром и электронами на самом внешнем энергетическом уровне. Это приводит к меньшему атомному радиусу.
Электроотрицательность:
Электроотрицательность — это мера способности атома притягивать к себе электроны в химической связи.
При движении слева направо в течение определенного периода электроотрицательность обычно увеличивается. [3]
Это связано с тем, что радиус атома меньше, а положительный заряд ядра сильнее, что делает его более привлекательным для отрицательно заряженных электронов.
Энергия ионизации:
Энергия ионизации – это количество энергии, необходимое для отрыва электрона от атома.
При движении слева направо в течение определенного периода энергия ионизации обычно увеличивается. [4]
Это связано с тем, что радиус атома меньше, а электроны крепче удерживаются ядром, что затрудняет удаление электрона.
Другие особенности:
Точки плавления и кипения: Обычно с течением времени увеличиваются слева направо, но с некоторыми исключениями.
Металлический характер: уменьшается слева направо с течением времени по мере того, как неметаллы становятся более распространенными.
Реакционная способность: элементы становятся менее реактивными по мере движения слева направо в течение определенного периода времени, поскольку электроны удерживаются крепче и с меньшей вероятностью участвуют в химических реакциях.
Значение периодов в химии
Периоды таблицы Менделеева необходимы для понимания поведения элементов, поскольку они предоставляют информацию об электронной конфигурации элементов и о том, как они взаимодействуют с другими элементами. Вот несколько причин, почему периоды важны в химии:
- Прогнозирование свойств: Таблица Менделеева позволяет ученым предсказывать свойства элементов на основе их положения в таблице. Например, элементы одного и того же периода имеют одинаковое количество электронных оболочек, что может помочь предсказать размер их атомов, реакционную способность и другие свойства.
- Выявление тенденций: расположение элементов в периодической таблице позволяет ученым определять тенденции в их свойствах. Например, электроотрицательность и энергия ионизации имеют тенденцию увеличиваться слева направо с течением времени, а размер атома имеет тенденцию уменьшаться. Эту информацию можно использовать для прогнозирования поведения элементов в химических реакциях.
- Группировка элементов. В периодической таблице элементы группируются по категориям в зависимости от их свойств, например , металлы, неметаллы и металлоиды . Это помогает ученым понять сходства и различия между элементами и то, как они взаимодействуют друг с другом.
- Открытие новых элементов. Таблица Менделеева также помогает ученым предсказывать существование и свойства новых элементов. Исследуя пробелы в таблице, учёные могут предсказывать свойства неоткрытых элементов и исследовать их в лаборатории.
Краткое содержание
В таблице Менделеева есть семь горизонтальных линий, называемых периодами. Элементы одного и того же периода имеют одинаковое количество электронных слоев. В таблице Менделеева семь периодов, пронумерованных от 1 до 7, и количество оболочек элемента определяет его период.
По мере прохождения периода периодической таблицы атомный радиус обычно уменьшается, а электроотрицательность и энергия ионизации обычно увеличиваются. Другие характеристики, такие как температуры плавления и кипения, металлический характер и реакционная способность, также предсказуемо изменяются с течением времени.
Периоды таблицы Менделеева важны для предсказания свойств элементов, выявления тенденций, группировки элементов и открытия новых элементов. Исследуя пробелы в таблице, учёные могут предсказывать свойства неоткрытых элементов и исследовать их в лаборатории.
