Sodyum dikromat kimyasal bir bileşiktir. Oksitleyici bir madde ve oldukça toksik bir maddedir. Metal kaplama ve pigment üretimi gibi çeşitli endüstriyel işlemlerde kullanılır.
| IUPAC Adı | Sodyum dikromat |
| Moleküler formül | Na2Cr2O7 |
| CAS numarası | 10588-01-9 |
| Eş anlamlı | Sodyum dikromat, Disodyum dikromat, Sodyum dikromat |
| InChI | InChI=1S/2Cr.2Na.7O/q2*+6;2*+1;7*-2 |
Sodyum dikromatın özellikleri
Sodyum dikromat formülü
Sodyum dikromatın formülü Na2Cr2O7’dir. İki sodyum (Na) atomu, iki krom (Cr) atomu ve yedi oksijen (O) atomundan oluşur. Formül, bileşikteki her bir elementin oranını temsil eder.
Sodyum Dikromat Molar Kütle
Sodyum dikromatın molar kütlesi, onu oluşturan tüm elementlerin atomik kütleleri toplanarak hesaplanır. Sodyumun (Na) atom kütlesi 22,99 g/mol, kromun (Cr) kütlesi 51,99 g/mol ve oksijenin (O) 16,00 g/mol kütlesi vardır. Bu değerlerin eklenmesi, sodyum dikromat için 261,97 g/mol molar kütlesini verir.
Sodyum dikromatın kaynama noktası
Sodyum dikromatın kaynama noktası yaklaşık 400°C’dir (752°F). Bu, normal atmosferik basınç altında ısıtıldığında bileşiğin sıvı fazdan gaz fazına geçtiği sıcaklıktır.
Sodyum dikromat Erime noktası
Sodyum dikromatın erime noktası yaklaşık 357°C’dir (675°F). Bu, katı bileşiğin sıvı duruma dönüştüğü sıcaklıktır. Numunenin saflığına bağlı olarak erime noktasının biraz değişebileceğini unutmamak önemlidir.
Sodyum dikromatın yoğunluğu g/mL
Sodyum dikromatın yoğunluğu yaklaşık 2,52 g/mL’dir. Yoğunluk, bir maddenin birim hacim başına kütlesinin bir ölçüsüdür. Sodyum dikromat durumunda bu değer, bileşiğin belirli bir hacminin nispeten ağır olduğunu gösterir.
Sodyum Dikromat Molekül Ağırlığı
Sodyum dikromatın moleküler ağırlığı 261,97 g/mol’dür. Bu değer, bileşiğin bir molekülünde bulunan tüm atomların atom ağırlıklarının toplamını temsil eder.
Sodyum dikromatın yapısı
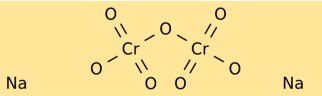
Sodyum dikromat, parlak kırmızı-turuncu kristaller oluşturan bir kristal yapıya sahiptir. Sodyum iyonlarından (Na+) ve dikromat iyonlarından (Cr2O7^2-) oluşur. Dikromat iyonunun bir tarafında iki oksijen atomuna, diğer tarafında üç oksijen atomuna bağlı merkezi bir krom atomu vardır.
Sodyum dikromatın çözünürlüğü
Sodyum dikromat suda çok çözünür. Suda kolayca çözünür ve sarı-turuncu bir çözelti oluşturur. Sodyum dikromatın sudaki çözünürlüğü sıcaklık ve pH gibi faktörlerden etkilenir; daha yüksek sıcaklıklar ve daha düşük pH seviyeleri çözünürlüğü arttırır.
| Dış görünüş | Kırmızı-turuncu kristaller |
| Spesifik yer çekimi | 2.52 |
| Renk | Parlak kırmızı-turuncu |
| Koku | Kokusuz |
| Molar kütle | 261,97 gr/mol |
| Yoğunluk | 2,52 gr/ml |
| Füzyon noktası | 357°C (675°F) |
| Kaynama noktası | 400°C (752°F) |
| Flaş noktası | Uygulanamaz |
| sudaki çözünürlük | Çok çözünür |
| çözünürlük | Suda çözünür, etanol/metanolde az çözünür |
| Buhar basıncı | Müsait değil |
| Buhar yoğunluğu | Müsait değil |
| pKa | Müsait değil |
| pH | Müsait değil |
Sodyum dikromatın güvenliği ve tehlikeleri
Sodyum dikromat önemli güvenlik riskleri oluşturur. Yutulması, solunması veya deri yoluyla emilmesi durumunda oldukça toksiktir. Bu, temas halinde ciddi yanıklara ve göz hasarına neden olabilir. Bileşik aynı zamanda kansere neden olabilecek potansiyel kanserojen olarak da sınıflandırılmaktadır. Ek olarak oksitleyici bir maddedir, yani yanıcı maddelerle şiddetli reaksiyona girerek yangın veya patlama riskini artırabilir. Sodyum dikromat kullanılırken koruyucu kıyafet, eldiven ve gözlük kullanımı da dahil olmak üzere uygun güvenlik önlemleri alınmalıdır. Uyumsuz maddelerden uzak, güvenli ve iyi havalandırılan bir alanda saklanmalıdır. Maruz kalınması veya yutulması durumunda derhal tıbbi müdahale çok önemlidir.
| Tehlike sembolleri | Aşındırıcı, sağlık tehlikesi |
| Güvenlik Açıklaması | Çok toksik, aşındırıcı, kanserojen |
| BM kimlik numaraları | UN3086 |
| HS kodu | 28415000 |
| Tehlike sınıfı | 6.1 |
| Paketleme grubu | II |
| Toksisite | Çok zehirli |
Sodyum dikromat sentezi için yöntemler
Sodyum dikromatın sentezlenmesi için çeşitli yöntemler vardır. Yaygın olarak kullanılan bir yöntem, sodyum kromat (Na2CrO4) ve sodyum dikromat (Na2Cr2O7) arasındaki reaksiyondur. Sülfürik asit (H2SO4) sodyum kromatla reaksiyona girerek sodyum dikromat ve su üretir. Bu reaksiyonun kimyasal denklemi şöyledir:
2Na2CrO4 + 2H2SO4 → Na2Cr2O7 + Na2SO4 + H2O
Başka bir yöntem , potasyum permanganat (KMnO4) gibi güçlü bir oksitleyici madde kullanılarak sodyum kromatın oksidasyonunu içerir. Bu reaksiyonda sodyum kromat, sülfürik asit varlığında potasyum permanganat ile reaksiyona girerek sodyum dikromat, manganez dioksit (MnO2) ve su üretir.
2Na2CrO4 + 6KMnO4 + 7H2SO4 → 2Na2Cr2O7 + 6MnO2 + 7K2SO4 + 8H2O
Sodyum hidroksit (NaOH) ile krom trioksit (CrO3) arasındaki reaksiyon, sodyum dikromat üretir. Reaksiyon sulu bir ortamda gerçekleşir ve sodyum dikromat ve su üretir.
2NaOH + CrO3 → Na2Cr2O7 + H2O
Bu sentetik yöntemleri uygularken, sodyum dikromatın toksik ve tehlikeli yapısı nedeniyle bireyler dikkatli olmalıdır. Sürece dahil olanların refahını sağlamak için uygun güvenlik önlemlerinin ve koruyucu ekipmanların kullanılması zorunludur.
Sodyum dikromatın kullanım alanları
Sodyum dikromatın farklı endüstrilerde çeşitli uygulamaları vardır. İşte bazı kullanımları:
- Metal Kaplama: Elektrokaplama işlemlerinde çelik, alüminyum ve çinko gibi çeşitli metal yüzeylere koruyucu ve dekoratif bir kaplama uygulamak için sodyum dikromat kullanılır.
- Pigment Üretimi: Sodyum dikromat, boyalarda, mürekkeplerde ve boyalarda yaygın olarak bulunan krom sarısı ve krom yeşili gibi pigmentlerin üretiminde hayati bir rol oynar.
- Ahşap Koruyucu: Sodyum dikromat, güçlü oksitleyici özelliği ile özellikle dış cephe uygulamalarında ahşabı çürümeye, böceklere ve mantarlara karşı korur.
- Deri Tabaklama: Tabaklama endüstrisi, deri işleme prosesinde mordan olarak sodyum dikromat kullanarak derinin renk haslığını ve dayanıklılığını artırır.
- Kimyasal Sentez: Sodyum dikromat, organik bileşiklerin sentezi, oksidasyon reaksiyonları ve diğer krom bileşiklerinin hazırlanması dahil olmak üzere çeşitli kimyasal reaksiyonlarda reaktif görevi görür.
- Laboratuvar Uygulamaları: Sodyum dikromat analitik testler, kalibrasyon standartları ve kimyasal araştırmalar için laboratuvar uygulamaları bulur.
- Tekstil Endüstrisi: Sodyum dikromat, renk haslığını artırır ve tekstil boyama ve baskı işlemleri sırasında boyaların kumaşa daha iyi yapışmasını sağlar.
- Fotoğrafçılık: Sodyum dikromat, ışığa duyarlı emülsiyonlarda çok önemli bir bileşendir ve bazı fotoğrafik işlemlerde oksitleyici bir madde olarak işlev görür.
Toksisitesi ve çevre üzerindeki etkisi nedeniyle, sodyum dikromatın güvenlik talimatlarına ve uygun imha yöntemlerine uyarak dikkatli bir şekilde kullanılması önemlidir.
Sorular:
S: 3,00 g sodyum dikromat, Na2Cr2O7’de kaç oksijen atomu vardır?
C: 3,00 g sodyum dikromatta 6,02 x 10^22 oksijen atomu vardır.
S: 4,00 g sodyum dikromat, Na2Cr2O7’de kaç oksijen atomu vardır?
C: 4,00 g sodyum dikromatta 8,03 x 10^22 oksijen atomu vardır.
Soru: 5,00 g sodyum dikromat, Na2Cr2O7’de kaç oksijen atomu vardır?
C: 5,00 g sodyum dikromatta 1,00 x 10^23 oksijen atomu vardır.
S: 6,00 g sodyum dikromat, Na2Cr2O7’de kaç oksijen atomu vardır?
C: 6,00 g sodyum dikromatta 1,20 x 10^23 oksijen atomu vardır.
Soru: 7,00 g sodyum dikromatta kaç oksijen atomu vardır?
C: 7,00 g sodyum dikromatta 1,40 x 10^23 oksijen atomu vardır.
S: Sodyum dikromat MSDS’si?
C: Sodyum dikromatın Malzeme Güvenliği Veri Sayfası (MSDS), özellikleri, kullanım önlemleri ve güvenlik önlemleri hakkında ayrıntılı bilgi sağlar.
S: Sodyum dikromatın yerini ne alabilir?
C: Sodyum dikromatın alternatifleri, spesifik uygulamaya bağlı olarak üç değerlikli krom tuzları veya krom olmayan maddeler gibi diğer krom bileşiklerini içerir.
S: Sodyum dikromat ne için kullanılır?
C: Sodyum dikromat oksitleyici bir madde, ahşap koruyucu ve pigment olarak ve ayrıca metal kaplama ve deri tabaklama gibi çeşitli endüstriyel işlemlerde kullanılır.
S: Sodyum dikromat dihidrattan sarı kromat çözeltisi yapılabilir mi?
C: Evet, sodyum dikromat dihidratın suda çözülmesiyle sarı bir kromat çözeltisi hazırlanabilir.
S: Sodyum dikromatın formülü nedir?
C: Sodyum dikromatın formülü Na2Cr2O7’dir.
S: Sodyum dikromat inorganik midir?
C: Evet, sodyum dikromat inorganik bir bileşiktir.
S: Sodyum dikromat testi ne işe yarar?
C: Sodyum dikromat test amacıyla, örneğin belirli maddelerin varlığını değerlendirmek veya belirli kimyasal reaksiyonları izlemek için kullanılabilir.
