Sodyum borohidrür (NaBH4), organik sentezde indirgeyici madde olarak ve yakıt hücreleri için hidrojen kaynağı olarak kullanılan beyaz kristalli bir tozdur. Suya karşı oldukça reaktif ve duyarlıdır.
| IUPAC Adı | Sodyum tetrahidroborat |
| Moleküler formül | NaBH4 |
| CAS numarası | 16940-66-2 |
| Eş anlamlı | Sodyum borohidrit, sodyum tetrahidridoborat, sodyum borohidrit hidrat, sodyum tetrahidroborat hidrat |
| InChI | InChI=1S/BH4.Na/h1H4;/q+1;-1 |
Sodyum borohidrürün özellikleri
Sodyum borohidrürün kaynama noktası
Sodyum borohidrürün iyi tanımlanmış bir kaynama noktası yoktur çünkü ısıtıldığında ayrışır. Ayrışma sıcaklığı sıcaklık ve basınç koşullarına bağlıdır.
Sodyum borohidrürün erime noktası
Sodyum borohidrürün erime noktası 240 ila 242°C’dir. Bu sıcaklıkta NaBH4’ün katı formu sıvı duruma geçer.
Sodyum borohidrürün yoğunluğu g/ml
Sodyum borohidrürün yoğunluğu 1,33 g/ml’dir. Diğer maddelerle karşılaştırıldığında nispeten yoğun olan beyaz kristal bir katıdır.
Sodyum Borohidrürün molar kütlesi
Sodyum Borohidrürün (NaBH4) molar kütlesi 37,83 g/mol’dür. NaBH4’ün moleküler formülünde bulunan tüm atomların atomik kütlelerinin (1 sodyum atomu, 1 bor atomu ve 4 hidrojen atomu) eklenmesiyle hesaplanır.
Sodyum borohidrürün moleküler ağırlığı
Sodyum borohidrürün moleküler ağırlığı 37,83 g/mol’dür. Bu, NaBH4’ün moleküler formülündeki tek tek atomların atomik kütlelerinin toplamıdır.
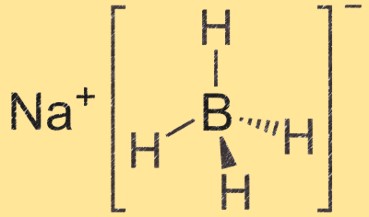
Sodyum borohidrürün yapısı
Sodyum borohidrit, merkezinde bir sodyum iyonu ve ona bağlı dört bor hidrit grubu bulunan tetrahedral bir moleküldür. Bor atomu dört hidrojen atomuna bağlanarak tetrahedral bir yapı oluşturur.
Sodyum Borohidrit Formülü
Sodyum tetrahidroboratın kimyasal formülü NaBH4’tür. Bir sodyum atomu (Na), bir bor atomu (B) ve dört hidrojen atomundan (H) oluşur. Bu formül, bu maddenin kimyasal bileşimini ve elementel bileşimini temsil eder.
| Dış görünüş | Beyaz kristal toz |
| Spesifik yer çekimi | 1.33g/ml |
| Renk | Beyaz |
| Koku | Kokusuz |
| Molar kütle | 37,83 gr/mol |
| Yoğunluk | 1.33g/ml |
| Füzyon noktası | 240-242°C |
| Kaynama noktası | Isıtıldığında ayrışır |
| Flaş noktası | Uygulanamaz |
| sudaki çözünürlük | Suda çözünebilir |
| çözünürlük | Organik çözücülerde çözünür |
| Buhar basıncı | Uygulanamaz |
| Buhar yoğunluğu | Uygulanamaz |
| pKa | Uygulanamaz |
| pH | Uygulanamaz |
Sodyum borhidrürün güvenliği ve tehlikeleri
Sodyum tetrahidroborat yanıcıdır ve suyla reaksiyona girer. Yanıcı hidrojen gazı açığa çıkarabilir ve hava ile patlayıcı karışımlar oluşturabilir. Sodyum tetrahidroborat aynı zamanda cildi ve gözü tahriş edicidir. Sodyum tetrahidroboratla çalışırken maruz kalmayı en aza indirmek için yeterli havalandırma ve kişisel koruyucu ekipman kullanılmalıdır. Ateş kaynaklarından ve sudan uzakta, serin ve kuru bir yerde saklayın.
| Tehlike sembolleri | Yanıcı, Tahriş Edici |
| Güvenlik Açıklaması | S26, S36/37 |
| BM kimlik numaraları | UN3375 |
| HS kodu | 2827.90.90 |
| Tehlike sınıfı | 4.3 |
| Paketleme grubu | II |
| Toksisite | Yutulması, solunması ve ciltle teması halinde orta derecede toksiktir |
Sodyum borohidrürün sentezi için yöntemler
Sodyum borohidrür (NaBH4), aşağıdakiler de dahil olmak üzere çeşitli yöntemlerle sentezlenebilir:
- Metalik sodyumun indirgenmesi: Bu yöntem, NaBH4 üretmek için bor trioksitin (B2O3) metalik sodyum ile indirgenmesini içerir.
- Sodyum Hidritin İndirgenmesi: Sodyum hidrit (NaH), NaBH4 üretmek üzere bor trihalidleri indirgemek için kullanılabilir.
- Lityum Alüminyum Hidrit İndirgemesi: Lityum alüminyum hidrit (LiAlH4), NaBH4 üretmek üzere bor halojenürleri indirgemek için kullanılabilir.
- Hidrojenasyon: Sodyum borohidrit, sodyum borohidrürün (NaBH3H) hidrojenlenmesiyle sentezlenebilir.
Sodyum tetrahidroborat yanıcı ve reaktif olduğundan, uzman ekipman ve eğitimli personel, iyi havalandırılmış bir ortamda tüm bu yöntemleri uygulamalıdır. Seçilen sentez yöntemi istenen verim, saflık ve maliyet hususlarına bağlı olacaktır.
Sodyum borohidrürün kullanım alanları
Sodyum tetrahidroborat (NaBH4) çok yönlü bir indirgeyici ajandır ve çeşitli alanlarda geniş bir uygulama alanına sahiptir. Sodyum tetrahidroboratın yaygın kullanımlarından bazıları şunlardır:
- Organik Sentez: NaBH4, karbonil bileşiklerinin, esterlerin, nitrillerin ve amidlerin karşılık gelen alkollere, aldehitlere ve aminlere indirgenmesinde kullanılır.
- Farmasötikler: Sodyum tetrahidroborat, çeşitli aktif farmasötik bileşenlerin sentezinde ve kiral bileşiklerin hazırlanmasında kullanılır.
- Polimer Bilimi: NaBH4, epoksi reçinelerin ve doymamış polyester reçinelerin indirgenmesinde kullanılır.
- Çevre: Sodyum tetrahidroborat, atık su arıtımında ağır metaller ve boyalar gibi kirleticileri azaltmak için kullanılabilir.
- Gıda Endüstrisi: NaBH4, az yağlı sürülebilir ürünler, dondurma ve çikolata üretiminde indirgeyici madde olarak kullanılır.
Genel olarak, sodyum tetrahidroboratın, hafif indirgeme özellikleri ve karmaşık moleküler yapılardaki fonksiyonel grupları seçici olarak azaltma yeteneği nedeniyle kimyasal sentez alanında değerli bir araç olduğu kanıtlanmıştır.
Sorular:
Bu bileşiklerden hangisi sodyum borohidrür ile indirgenebilir? tüm başvuruyu kontrol et.
Sodyum tetrahidroborat (NaBH4), aşağıdakiler de dahil olmak üzere çok çeşitli bileşikleri azaltabilir:
- Aldehitler ve ketonlar gibi karbonil bileşikleri
- nitriller
- Esterler
- Amidler
- Epoksi reçineler
- Doymamış polyester reçineler
- Bazı boyalar
- Ağır metaller
- Kiral bileşikler
Belirli koşulların ve reaksiyon parametrelerinin indirgeme verimliliğini ve indirgeme işleminin seçiciliğini etkileyebileceğinin dikkate alınması önemlidir. Ek olarak, bazı bileşikler istenmeyen yan reaksiyonlara maruz kalabileceğinden, tüm bileşikler sodyum tetrahidroborat ile indirgemeye uygun değildir.
Sodyum borhidrürün neme maruz bırakılması neden önemlidir?
Sodyum tetrahidroboratın (NaBH4) neme maruz kalması birkaç nedenden dolayı önemlidir:
- Reaktivite: Sodyum tetrahidroborat çok reaktiftir ve nem varlığında hızla ayrışarak hidrojen gazı ve ısı üretebilir. Bu, doğru şekilde kullanılmadığı takdirde patlama ve yangın riski oluşturabilir.
- Hidroliz: Sodyum tetrahidroborat, susuz forma kıyasla azaltıcı özellikleri azaltan sodyum tetrahidroborat hidratı (NaBH4.xH2O) oluşturmak üzere nem varlığında kolayca hidrolize olur.
- Depolama Kararlılığı: Nem, sodyum tetrahidroboratın yavaş yavaş ayrışmasına neden olarak raf ömrünü ve indirgeyici madde olarak etkinliğini azaltabilir.
Bu nedenle, sodyum borohidrürün kuru, hava geçirmez bir kapta saklanması ve neme maruz kalmayı en aza indirmek için iyi havalandırılan bir ortamda kullanılması önemlidir. Neme maruz kalmak kaçınılmazsa, nem giderme maddelerinin veya koruyucu atmosferlerin kullanılması, bunun sodyum tetrahidroboratın stabilitesi ve reaktivitesi üzerindeki etkilerini en aza indirmeye yardımcı olabilir.
Sodyum borohidrit bir katalizör mü?
Sodyum tetrahidroborat (NaBH4) genellikle bir katalizör olarak değil, bir indirgeyici madde olarak kabul edilir. Katalizör, kendisi kalıcı bir değişime uğramadan kimyasal reaksiyonu hızlandıran bir maddedir. Sodyum tetrahidroborat indirgendikçe kimyasal olarak değişir ve indirgeme reaksiyonunda tüketilir.
Organik sentez ve indirgeme reaksiyonlarında genellikle hidrit (H-) iyonlarının kaynağı olarak sodyum tetrahidroborat kullanılır. Sodyum tetrahidroborat, bu hidrit iyonlarını substrat molekülüne aktararak karboniller, nitriller ve esterler gibi fonksiyonel grupları azaltır. İndirgeyici bir madde olarak rolüne rağmen, sodyum tetrahidroborat, proton alıcısı olarak ikincil bir rol oynayabilir, bu da onu reaksiyon koşullarını etkileyebilen ve reaksiyon sonucunu etkileyebilen hafif bir baz haline getirir.
Sodyum borhidrürün suyla karıştırılması durumunda hangi yanıcı gaz üretilir?
Sodyum tetrahidroborat (NaBH4) suyla karıştırılırsa hızlı hidrolize uğrayarak hidratlı sodyum borohidrit (NaBH4.xH2O) ve hidrojen gazı oluşur. Üretilen hidrojen gazı yanıcıdır ve uygun şekilde kullanılmazsa patlama ve yangın tehlikesi oluşturabilir.
Sodyum tetrahidroborat ile su arasındaki reaksiyon ekzotermik olabilir ve ısı üretebilir, bu da hidroliz hızını daha da hızlandırabilir ve hidrojen gazı salınımını artırabilir. Reaksiyon aynı zamanda kısa sürede büyük miktarda gaz üreterek aşırı basınç ve patlama riski yaratabilir.
Bu nedenle, sodyum tetrahidroboratın iyi havalandırılmış bir ortamda işlenmesi ve neme veya suya maruz bırakılmasından kaçınılması önemlidir. Neme maruz kalmak kaçınılmazsa, nem giderme maddelerinin veya koruyucu atmosferlerin kullanılması, hidroliz oranının ve hidrojen gazı salınımının en aza indirilmesine yardımcı olabilir.
Kaç mol kafur sodyum borohidrit ile reaksiyona girer?
Sodyum tetrahidroborat (NaBH4) ile reaksiyona girecek kafurun mol sayısı, reaksiyonun stokiyometrisi, reaktanların konsantrasyonu ve saflığı ve reaksiyon koşulları dahil olmak üzere çeşitli faktörlere bağlıdır. Reaksiyonun stokiyometrisi, sodyum tetrahidroborat kullanılarak kafurun izobornele indirgenmesine ilişkin kimyasal denklemden belirlenebilir:
C10H16O + 4 NaBH4 → C10H18O + 4 NaBO2 + 4 H2
Denkleme göre, bir mol kafur, 4 mol sodyum tetrahidroborat ile reaksiyona girer. Belirli bir miktarda NaBH4 ile reaksiyona girecek gerçek kafur miktarı, reaktanların konsantrasyonuna ve saflığının yanı sıra sıcaklık, zaman ve katalizör gibi reaksiyon koşullarına bağlı olacaktır.
Bu nedenle daha kesin bilgi olmadan sodyum tetrahidroborat ile reaksiyona girecek kafurun tam mol sayısını belirlemek mümkün değildir.
