Nikel sülfat (NiSO4), nikel, kükürt ve oksijen atomlarından oluşan bir bileşiktir. Yaygın olarak elektrokaplamada, katalizörlerde ve bazı gübrelerde besin maddesi olarak kullanılır.
| IUPAC Adı | Nikel(II) sülfat |
| Moleküler formül | NiSO4 |
| CAS numarası | 7786-81-4 |
| Eş anlamlı | Nikel sülfat, sülfürik asidin nikel tuzu, nikel (II) sülfat, nikel (2+); sülfat |
| InChI | InChI=1S/Ni.H2O4S/c;1-5(2,3)4/h;(H2,1,2,3,4)/q+2;/p-2 |
Nikel sülfatın özellikleri
Nikel sülfat formülü
Nikel sülfatın kimyasal formülü NiSO4’tür. Bir nikel atomu (Ni) ve bir sülfat grubunun (SO4) kombinasyonunu temsil eder. Formül, sülfat grubundaki oksijenin yanı sıra nikel ve kükürtün varlığını da açıkça gösterir.
Nikel Sülfat Molar Kütlesi
Nikel sülfatın (NiSO4) molar kütlesi, onu oluşturan elementlerin atomik kütleleri toplanarak hesaplanır. Nikel (Ni) mol başına yaklaşık 58,69 gram atom kütlesine sahipken, kükürt (S) mol başına yaklaşık 32,07 gram atom kütlesine ve oksijen (O) mol başına yaklaşık 16 gram atom kütlesine sahiptir. Bu değerlerin eklenmesiyle nikel sülfatın molar kütlesinin yaklaşık olarak mol başına 154,76 gram olduğu tespit edilir.
Nikel sülfatın kaynama noktası
Nikel sülfatın belirli bir kaynama noktası yoktur çünkü ısıtıldığında ayrışır. Ancak ayrışma sıcaklığının basınç ve diğer maddelerin varlığı gibi faktörlerden etkilendiğini unutmamak önemlidir. Bu nedenle nikel sülfatın yüksek sıcaklıklara maruz kaldığında dikkatli kullanılması tavsiye edilir.
Nikel sülfat Erime noktası
Nikel sülfatın erime noktası yaklaşık 100 santigrat derecedir (212 derece Fahrenheit). Bu sıcaklıkta nikel sülfatın katı formu sıvı duruma geçer. Nikel sülfatın saflığı ve kristal yapısındaki değişikliklerin erime noktasını az da olsa etkileyebileceğini belirtmekte fayda var.
Nikel sülfatın yoğunluğu g/mL
Nikel sülfatın yoğunluğu birim hacim başına kütlesini ifade eder. Nikel sülfatın yoğunluğu tipik olarak mililitre başına 3,68 gram (g/mL) civarındadır. Yoğunluğun numunenin sıcaklığına ve saflığına bağlı olarak değişebileceğine dikkat edilmelidir.
Nikel Sülfat Molekül Ağırlığı
Nikel sülfatın (NiSO4) moleküler ağırlığı, onu oluşturan elementlerin atom ağırlıklarının toplamıdır. Daha önce de belirtildiği gibi nikel sülfatın moleküler ağırlığı mol başına yaklaşık 154,76 gramdır.
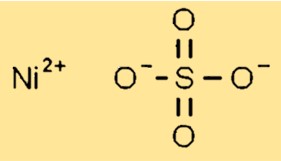
Nikel sülfatın yapısı
Nikel sülfat katı halde kristal bir yapıya sahiptir. Her bir nikel (Ni2+) iyonunun sülfat gruplarından altı oksijen atomu ile çevrelendiği monoklinik kristaller oluşturur. Sülfat grupları, kristal kafesin verimli bir şekilde sıkıştırılmasına izin verecek şekilde düzenlenir.
Nikel sülfatın çözünürlüğü
Nikel sülfat suda orta derecede çözünürlüğe sahiptir. Suda kolayca çözünür, sıcaklık arttıkça çözünürlüğü artar. Diğer iyonların ve maddelerin varlığı çözünürlüğünü etkileyebilir. Ek olarak nikel sülfat, su molekülleri ile birleştirildiğinde hidratlar oluşturabilir ve bu da çeşitli nikel sülfat hidratların oluşumuna yol açar.
| Dış görünüş | Mavi/yeşil kristaller |
| Spesifik yer çekimi | 3.68g/ml |
| Renk | Mavi-yeşil |
| Koku | Kokusuz |
| Molar kütle | 154,76 gr/mol |
| Yoğunluk | 3.68g/ml |
| Füzyon noktası | 100°C (212°F) |
| Kaynama noktası | ayrıştırılmış |
| Flaş noktası | Uygulanamaz |
| sudaki çözünürlük | Çok çözünür |
| çözünürlük | Suda ve etanol gibi organik çözücülerde çözünür |
| Buhar basıncı | Uygulanamaz |
| Buhar yoğunluğu | Uygulanamaz |
| pKa | -1.1 (sülfürik asit) |
| pH | Asit (yaklaşık 4) |
Nikel Sülfatın Güvenliği ve Tehlikeleri
Nikel sülfat dikkate alınması gereken bazı güvenlik riskleri taşır. Potansiyel risklerden kaçınmak için dikkatli bir şekilde ele alınması önemlidir. Ciltte tahrişe veya hassasiyete neden olabileceğinden doğrudan cilt teması en aza indirilmelidir. Olumsuz sağlık etkilerine neden olabileceğinden nikel sülfatın yutulması veya solunmasından kaçınılmalıdır. Nikel sülfatla çalışırken maddeyle teması önlemek için eldiven ve gözlük gibi uygun kişisel koruyucu ekipmanlar kullanılmalıdır. Nikel sülfat, uyumsuz malzemelerden uzakta, serin ve kuru bir yerde saklanmalıdır. Havadaki parçacıkların konsantrasyonunu en aza indirmek için nikel sülfatla çalışırken yeterli havalandırma gereklidir.
| Tehlike sembolleri | Hiçbiri |
| Güvenlik Açıklaması | – Cilt ile temasından kaçının – Yutmaktan ve solumaktan kaçının – Uygun kişisel koruyucu ekipman giyin |
| Birleşmiş Milletler tanımlayıcıları | Uygulanamaz |
| HS kodu | 2833.25 |
| Tehlike sınıfı | sınıflandırılmamış |
| Paketleme grubu | Uygulanamaz |
| Toksisite | Ciltte tahrişe veya hassasiyete neden olabilir |
Nikel sülfat sentez yöntemleri
Nikel sülfatın sentezlenmesi için farklı yöntemler vardır.
Yaygın bir yaklaşım, metalik nikel veya nikel oksit ile sülfürik asit arasındaki reaksiyonu içerir. Bu yöntemde sülfürik asit metalik Ni veya nikel oksidi çözerek nikel sülfatın oluşmasına neden olur. Verimli dönüşümü sağlamak için reaksiyonu sıcaklık ve karıştırma gibi kontrollü koşullar altında gerçekleştirebilirsiniz.
Başka bir yöntem, sülfürik asidin nikel karbonatla reaksiyonunu içerir. Sülfürik asit nikel karbonatı çözerek nikel sülfat üretir. Kimyacılar genellikle bu yöntemi, uygun bir başlangıç malzemesi sağladığından, kolayca bulunabilen nikel karbonata sahip olduklarında kullanırlar.
Ek olarak sülfürik asit, NiSO4’ü sentezlemek için nikel hidroksiti çözebilir. Nikel hidroksitin sülfürik asitte çözünmesi NiSO4 oluşumuna yol açar. Bu yöntem, nikel sülfatın sentezi için bir öncü olarak nikel hidroksitin kullanılması istendiğinde uygundur.
Sentez işlemi sırasında uygun güvenlik önlemlerine uymanız gerektiğini unutmamak önemlidir. Buna uygun koruyucu ekipmanın kullanılması ve kullanım prosedürleri de dahildir. Zararlı buharlara maruz kalma riskini en aza indirmek için reaksiyonları iyi havalandırılan bir alanda gerçekleştirin. Sıcaklık ve konsantrasyon gibi reaksiyon parametrelerinin dikkatli kontrolü, optimum nikel sülfat dönüşümünü ve verimini sağlamak için çok önemlidir.
Nikel Sülfatın Kullanım Alanları
Nikel sülfatın farklı endüstrilerde çeşitli uygulamaları vardır. Yaygın kullanımlarından bazıları şunlardır:
- Elektrokaplama: Elektrokaplama işlemleri, metal yüzeylerde dayanıklı, korozyona dayanıklı bir kaplama oluşturmak için nikel sülfattan yoğun şekilde yararlanır. Nikel sülfat mücevher, otomobil parçaları ve mutfak eşyaları gibi eşyaların görünümünü, sertliğini ve sağlamlığını artırır.
- Katalizör: Nikel sülfat, hidrojenasyon ve oksidasyon işlemleri dahil olmak üzere birçok kimyasal reaksiyonda katalizör görevi görür. Endüstriler, ilaç, petrokimya ve ince kimyasalların üretiminde nikel sülfat katalizörlerini kullanır.
- Piller: Şarj edilebilir piller, özellikle Ni-Cd ve Ni-MH piller, önemli bir bileşen olarak nikel sülfat içerir. Nikel sülfat, elektrot reaksiyonlarını kolaylaştırır ve elektrik enerjisinin verimli bir şekilde depolanmasını ve serbest bırakılmasını sağlar.
- Gübre: Bazı gübreler bitkilere gerekli besinleri sağlamak için nikel sülfattan çözünebilir Ni kullanır. Nikel, bitkilerde çeşitli metabolik süreçlerde önemli bir rol oynar ve bitkilerin büyümesine ve gelişmesine katkıda bulunur.
- Tekstil: Tekstil endüstrisi, kumaşların renk haslığını ve boya emilimini arttırmak için boyama ve baskı işlemlerinde nikel sülfat kullanır. Nikel sülfat canlı, uzun ömürlü renk sonuçları sağlar.
- Farmasötikler: Nikel sülfat, esas olarak aktif bileşen olarak Ni içeren ilaçların üretilmesi veya tıbbi araştırmalarda kullanılan spesifik Ni komplekslerinin formüle edilmesi için farmasötik preparatlarda uygulama alanı bulur.
- Araştırma ve geliştirme: Laboratuvarlar, kimyasal sentez, elektrokimyasal çalışmalar ve malzeme bilimi araştırmaları dahil olmak üzere çeşitli araştırma ve geliştirme amaçları için nikel sülfat kullanır.
Sorular:
S: Nikel(II) sülfatın formülü nedir?
C: Nikel(II) sülfatın formülü NiSO4’tür.
Soru: Nikel(II) sülfat çözeltisine metalik krom ekleniyor. Dengeli kimyasal reaksiyon nedir?
C: Dengeli kimyasal reaksiyon şu şekildedir: Cr + NiSO4 -> CrSO4 + Ni.
S: Nikel amonyum sülfat nasıl yapılır?
C: Nikel amonyum sülfat, nikel sülfat ve amonyum sülfatın suda çözülmesi ve ardından kristalleştirilmesiyle hazırlanabilir.
Soru: Nikel sülfat suda çözünür mü?
C: Evet, nikel sülfat suda çözünür.
S: Nikel sülfatı kim çıkarıyor?
C: Nikel sülfat doğrudan çıkarılmıyor. Nikel cevherleri çıkarılıyor ve bunlardan nikel sülfat üretilebiliyor.
S: NiSO4 bileşiğinin adı nedir?
C: NiSO4 bileşiğine nikel sülfat denir.
Soru: 100 gram hidratta kaç gram NiSO4 var? Kaç mol?
C: 100 g hidrattaki NiSO4 miktarı, spesifik hidrat bileşiğine ve onun molar kütlesine bağlıdır.
S: NiSO4 suda çözünür mü?
C: Evet, NiSO4 suda çözünür.
Soru: Verim %76,9 ise kaç gram NiSO4 elde edilir?
C: Elde edilen NiSO4 gramı başlangıç miktarına ve reaksiyon koşullarına bağlıdır.
S: NiSO4 tehlikeli midir?
C: NiSO4 doğru şekilde kullanılmazsa tehlikeli olabilir. Onunla çalışırken güvenlik talimatlarına uymak önemlidir.
S: Kovalent bileşik NiSO4’ün adı nedir?
C: NiSO4 kovalent bir bileşik değildir. Nikel sülfat adı verilen iyonik bir bileşiktir.
S: NiSO4 bir tuz mudur?
C: Evet, NiSO4, iyonik yapısı ve bir asit (sülfürik asit) ile bir baz (nikel hidroksit) arasındaki reaksiyondan oluşması nedeniyle bir tuz olarak kabul edilir.
S: NiSO4’ün yükü nedir?
C: NiSO4’te nikel iyonu (Ni2+) 2+ pozitif yük taşırken, sülfat iyonu (SO4 2-) 2- negatif yük taşır.
