Nikel karbonat (NiCO3), nikel iyonlarından ve karbonat iyonlarından oluşur. Eşsiz özellikleri nedeniyle seramik ve katalizörlerde kullanılan yeşil bir katıdır.
| IUPAC Adı | Nikel(II) karbonat |
| Moleküler formül | NiCO3 |
| CAS numarası | 3333-67-3 |
| Eş anlamlı | Nikel karbonat; Karbonik asit, nikel tuzu, nikel monokarbonat |
| InChI | InChI=1S/CH2O3.Ni/c2-1(3)4;/h(H2,2,3,4);/q;+2 |
Nikel karbonatın özellikleri
Nikel Karbonat Formülü
Nikel monokarbonatın kimyasal formülü NiCO3’tür. Bir nikel (Ni) atomu, bir karbon (C) atomu ve üç oksijen (O) atomundan oluşur.
Nikel Karbonat Molar Kütlesi
Nikel monokarbonatın (NiCO3) molar kütlesi mol başına yaklaşık 118,7 gramdır. Bu değer, onu oluşturan elementlerin atomik kütlelerinin toplanmasıyla elde edilir.
Nikel karbonatın kaynama noktası
Nikel monokarbonatın belirgin bir kaynama noktası yoktur çünkü kaynama noktasına ulaşmadan önce ayrışma eğilimindedir. Isıtıldığında nikel oksit, karbondioksit ve oksijene ayrışır.
Nikel Karbonat Erime Noktası
Nikel monokarbonatın erime noktası yaklaşık 200°C’dir (392°F). Bu sıcaklıkta katı halden sıvı hale geçer.
Nikel karbonatın yoğunluğu g/mL
Nikel monokarbonatın yoğunluğu santimetreküp başına yaklaşık 3,6 gramdır (g/cm³). Bu yoğunluk değeri, bileşiğin birim hacim başına kütlesini gösterir.
Nikel Karbonat Molekül Ağırlığı
Nikel monokarbonatın (NiCO3) moleküler ağırlığı mol başına yaklaşık 118,7 gramdır. Bileşen atomlarının atom ağırlıklarının eklenmesiyle hesaplanır.
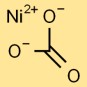
Nikel karbonatın yapısı
Nikel monokarbonat, merkezi bir nikel atomunun üçgen bir düzende üç oksijen atomuna bağlandığı temel bir yapıya sahiptir. Bu karbonat iyonunun çekirdeğini oluşturur. Yapı iyonik ve kovalent bağlarla bir arada tutulur.
Nikel karbonatın çözünürlüğü
Nikel monokarbonat suda çok az çözünür. Çözeltinin pH’ı düştükçe çözünürlüğü artar. Ayrıca hidroklorik asit gibi maddeler içeren asidik çözeltilerde de çözünebilir.
Nikel monokarbonatın özellikleri onu çeşitli uygulamalarda faydalı kılar. Suda çözünmemesi onu seramik ve pigmentlerdeki uygulamalara uygun hale getirir. Yüksek sıcaklıklarda ayrışması, katalitik işlemlerde kullanılmasına katkıda bulunur.
| Dış görünüş | Koyu yeşil |
| Spesifik yer çekimi | 3,6 g/cm³ |
| Renk | Yeşil |
| Koku | Kokusuz |
| Molar kütle | 118,7 g/mol |
| Yoğunluk | 3,6 g/cm³ |
| Füzyon noktası | 200°C (392°F) |
| Kaynama noktası | Kaynamadan önce parçalanır |
| Flaş noktası | Uygulanamaz |
| sudaki çözünürlük | Az çözünür |
| çözünürlük | Hidroklorik asit gibi asitlerde çözünür |
| Buhar basıncı | Müsait değil |
| Buhar yoğunluğu | Müsait değil |
| pKa | Uygulanamaz |
| pH | Uygulanamaz |
Nikel Karbonatın Güvenliği ve Tehlikeleri
Nikel monokarbonat potansiyel güvenlik riskleri oluşturur. Temas halinde cildi ve gözleri tahriş edebilir, kızarıklığa ve rahatsızlığa neden olabilir. Tozunun veya buharının solunması solunum yolu tahrişine veya öksürüğe neden olabilir. Eldiven ve gözlük gibi uygun koruyucu ekipman giyerek dikkatli bir şekilde kullanılması tavsiye edilir. Bileşiği yutmaktan veya solumaktan kaçının. Maruz kalma durumunda etkilenen bölgeleri yıkayın ve belirtiler devam ederse tıbbi yardım alın. Riskleri en aza indirmek için yeterli havalandırma ve muhafaza önlemleri gereklidir. Nikel monokarbonatla çalışırken güvenlik protokollerine uymak, olası sağlık sorunlarını önlemek ve güvenli bir ortam sağlamak açısından çok önemlidir.
| Tehlike sembolleri | Tahriş edici, Sağlık tehlikesi |
| Güvenlik Açıklaması | Tahriş edici; Temastan ve solumaktan kaçının; Dikkatli tutun |
| BM kimlik numaraları | Atıf yapılmadı |
| HS kodu | 2836.40.00 |
| Tehlike sınıfı | sınıflandırılmamış |
| Paketleme grubu | sınıflandırılmamış |
| Toksisite | Cilt ve göz tahrişine neden olabilir; solunması halinde solunum tahrişi |
Nikel karbonat sentez yöntemleri
Nikel monokarbonat çeşitli yöntemlerle sentezlenebilir. Yaygın bir yaklaşım, suda çözünebilir bir nikel tuzu ( nikel klorür veya nikel sülfat gibi) ile çözünebilir bir karbonat tuzu (sodyum karbonat gibi) arasındaki reaksiyonu içerir. İki çözelti karıştırılarak yeşil bir çökelti formunda çözünmeyen nikel monokarbonatın oluşmasına yol açar. Bu çökelti daha sonra filtrelenir, yıkanır ve kurutularak nihai ürün elde edilir.
Başka bir yöntem, nem varlığında nikel oksit veya nikel hidroksit ile karbondioksit gazı arasındaki reaksiyonu içerir. Bunun sonucunda su ile nikel monokarbonat oluşur. Bu işlem genellikle endüstriyel olarak nikel monokarbonat üretmek için kullanılır.
Ek olarak, çözünebilir bir nikel tuzu çözeltisinin, çözünebilir bir karbonat tuzu çözeltisi ile karıştırılması yoluyla bir çökeltme işlemi kullanılabilir. Nihai karışım karıştırılır ve oluşan nikel monokarbonat çökeltisi toplanır ve işlenir.
Bu sentez yöntemleri seramik, katalizör ve pigmentler gibi çeşitli uygulamalar için nikel monokarbonat üretir. Yüksek kaliteli nikel monokarbonat ürünleri elde etmek için reaksiyon koşullarının ve saflaştırma adımlarının dikkatli kontrolü çok önemlidir.
Nikel Karbonatın Kullanım Alanları
Nikel monokarbonat, benzersiz özelliklerinden dolayı çeşitli uygulamalar bulur. Bazı önemli kullanımlar şunları içerir:
- Seramik ve Cam Üretimi: Nikel monokarbonat, seramik ve camı sanatsal ifade ve endüstriyel kullanım için canlı renklerle zenginleştirir.
- Katalizör: Çeşitli kimyasal işlemlerde katalizör veya katalizör öncüsü olarak görev yapar ve yüksek sıcaklıklarda ayrışma sırasında oksijenin salınması yoluyla oksidasyon reaksiyonlarını kolaylaştırır.
- Elektrokaplama: Bir öncü olarak nikel monokarbonatın kullanılması, nikelin çeşitli yüzeylere elektrokaplanmasına olanak tanır, böylece yüzey görünümünü ve korozyon direncini arttırır.
- Pil Endüstrisi: Pil teknolojilerinde, özellikle nikel bazlı olanlarda, katot malzemelerine katkı sağlayarak pil sistemlerinin ilerlemesine destek olur.
- Pigmentler ve mürekkepler: Nikel monokarbonat; pigmentler, mürekkepler ve boyalarda yeşil renk tonunun üretilmesinde ayrılmaz bir rol oynar.
- Tarım: Gübrelerde besin maddesi nikel kaynağı olarak uygulanması bitki büyümesine fayda sağlar ve tarımda kullanılır.
- Tıp: Nadir de olsa araştırmacılar, antimikrobiyal özellikler gösteren başta nikel monokarbonat olmak üzere bazı nikel bileşiklerinden dolayı potansiyel tıbbi uygulamaları araştırıyorlar.
- Fotoğrafçılık: Tarihsel olarak, siyah beyaz fotoğraf tonerlerinde, tonları ve kontrastları zenginleştirici bir rol bulmuştur.
- Tekstil: Tekstil endüstrisi, boyaların emilimini arttırmak ve kumaşlara renk katmak için nikel monokarbonat kullanır.
- Araştırma ve Eğitim: Nikel monokarbonatın kimyasal özellikleri, onun kimya laboratuvarlarında eğitimsel gösteriler, deneyler ve araştırmalar için önemini ortaya koymaktadır.
Bu çok yönlü uygulamalar, seramik estetiğinin geliştirilmesinden piller ve katalizörler gibi ileri teknolojilerde rol oynamaya kadar çeşitli endüstrilerde nikel monokarbonatın önemini göstermektedir.
Sorular:
Soru: Hangi element en reaktiftir?
C: Sodyum.
Soru: Demirin krom, karbon ve nikelle karıştırılmasıyla hangi faydalı malzeme elde edilir?
C: Paslanmaz çelik.
S: Nikel karbonat suda çözünür mü?
C: Pek çözünmez.
Soru: Nikel tetrakarbonilde kaç mol karbon vardır?
C: Dört mol.
S: Karbon çeliğinden nikel kaplama nasıl çıkarılır?
C: Uygun kimyasal soyma maddelerinin veya elektrokimyasal yöntemlerin kullanılması.
S: Nikel(II) nitrat ve sodyum karbonatın net iyonik denklemi?
A: Ni²⁺ + CO₃²⁻ → NiCO₃(lar).
S: Nikel ekstraksiyonunda karbon monoksitin rolü?
C: Cevherlerinden nikeli çıkarmak için indirgeyici madde görevi görür.
S: Nikel monokarbonatın çözünürlüğü?
C: Suda çözünürlüğü düşüktür.
Soru: Karbon, sodyum ve nikelin atom numaraları?
A: Karbon: 6, Sodyum: 11, Nikel: 28.
S: Amonyum karbonat, nikel klorür ve suyu karıştırdığınızda ne olur?
A: Nikel monokarbonat çökeltisinin oluşması ve amonyum klorür gazının salınması.
