Neopentan, merkezi bir karbon atomuna bağlı dört metil grubuna sahip, oldukça dallanmış bir hidrokarbondur. Genellikle NMR spektroskopisinde referans bileşiği ve yakıt katkı maddesi olarak kullanılır.
| IUPAC Adı | 2,2-dimetilpropan |
| Moleküler formül | C5H12 |
| CAS numarası | 463-82-1 |
| Eş anlamlı | Dimetilpropan, tetrametilmetan, 2,2-dimetilpropan, Neo-C5H12, UN 2043 |
| InChI | InChI=1S/C5H12/c1-5(2,3)4/h1-4H3 |
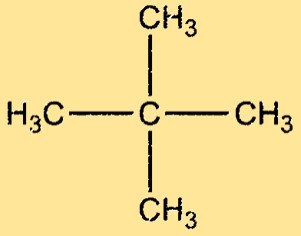
Neopentan yapısı
Neopentan, merkezi bir karbon atomuna bağlı dört metil grubuyla oldukça dallanmış bir yapıya sahiptir. Molekül simetrik ve tetrahedral olup, her bir bitişik karbon atomu çifti arasında 109,5°’lik bir bağ açısına sahiptir. Neopentan molekülü polar değildir ve molekülleri arasında yalnızca zayıf Van der Waals kuvvetleri bulunur.
Neopentanın kaynama noktası
Neopentanın kaynama noktası standart basınçta -9,5°C’dir (-15°F). Bu düşük kaynama noktası, molekülleri arasındaki zayıf moleküller arası kuvvetlerden kaynaklanmaktadır ve buharlaşmayı nispeten kolaylaştırmaktadır. Neopentan, oda sıcaklığında ve basınçta renksiz bir gazdır ve gaz kromatografisinde referans bileşik olarak yaygın olarak kullanılır.
Neopentan Molar Kütle
2,2-dimetilpropan olarak da bilinen neopentanın molar kütlesi 72,15 g/mol’dür. Merkezi bir karbon atomuna bağlı dört metil grubuna sahip oldukça dallanmış bir hidrokarbondur. Neopentanın molar kütlesi, C5H12 olan moleküler formülündeki tüm atomların atom ağırlıkları toplanarak hesaplanabilir.
Neopentan Erime noktası
Neopentanın erime noktası standart basınçta -16,6°C’dir (2°F). Kaynama noktası gibi, neopentanın düşük erime noktası da zayıf moleküller arası kuvvetlerden kaynaklanmaktadır. Neopentan, molekülleri arasında yalnızca zayıf Van der Waals kuvvetleri bulunan polar olmayan bir molekül olduğundan güçlü kristal yapılar oluşturmaz.
Neopentan Yoğunluğu g/ml
Neopentanın yoğunluğu standart sıcaklık ve basınçta 0,623 g/mL’dir. Bu düşük yoğunluk, neopentanın yalnızca 72,15 g/mol olan düşük moleküler ağırlığından kaynaklanmaktadır. Neopentan sudan daha az yoğun olduğundan ikisi karıştırılırsa su yüzeyinde yüzer.
Neopentan Molekül Ağırlığı
Tetrametilmetanın moleküler ağırlığı 72,15 g/mol’dür. Bu değer, beş karbon atomu ve 12 hidrojen atomundan oluşan molekülün tüm atomlarının atom ağırlıklarının toplamını temsil eder. Tetrametilmetanın düşük moleküler ağırlığı onu oldukça uçucu ve yanıcı bir bileşik haline getirir.
Tetrametilmetan formülü
Tetrametilmetanın moleküler formülü, molekülde bulunan atomların sayısını ve türlerini temsil eden C5H12’dir. Formül, tetrametilmetan molekülünde beş karbon atomu ve 12 hidrojen atomu bulunduğunu gösterir. Moleküler formül, molekül içindeki atomların yapısı tarafından belirlenen düzeni hakkında bilgi sağlamaz.
| Dış görünüş | Renksiz gaz |
| Spesifik yer çekimi | 20°C’de 0,623 g/mL |
| Renk | Renksiz |
| Koku | Kokusuz |
| Molar kütle | 72,15 gr/mol |
| Yoğunluk | 20°C’de 0,623 g/mL |
| Füzyon noktası | -16,6°C |
| Kaynama noktası | -9,5°C |
| Flaş noktası | -49°C |
| sudaki çözünürlük | 20°C’de 0,04 g/L |
| çözünürlük | Suda çözünmez |
| Buhar basıncı | 20°C’de 566 mmHg |
| Buhar yoğunluğu | 2,5 (hava = 1) |
| pKa | ~50 |
| pH | Uygulanamaz |
Neopentanın güvenliği ve tehlikeleri
Tetrametilmetan son derece yanıcı bir gazdır ve havayla patlayıcı karışımlar oluşturabilir. Kaynama noktası -9,5°C gibi çok düşük olduğundan ciltle temas etmesi halinde donmalara da neden olabilir. Tetrametilmetan gazının solunması baş dönmesine, mide bulantısına ve baş ağrısına neden olabilir. Tetrametilmetanı dikkatli bir şekilde kullanmak ve alev, kıvılcım veya diğer tutuşturucu kaynaklara maruz kalmaktan kaçınmak önemlidir. Tetrametilmetan serin, kuru ve iyi havalandırılan bir yerde, ısıdan ve oksitleyici maddelerden korunarak saklanmalıdır. Tetrametilmetanla çalışırken eldiven ve gözlük gibi uygun kişisel koruyucu ekipmanlar giyilmelidir.
| Tehlike sembolleri | F+ |
| Güvenlik Açıklaması | Son derece yanıcı gaz. Donmaya neden olabilir. Sadece iyi havalandırılmış bir ortamda kullanın. Isıdan ve tutuşturucu kaynaklardan uzak tutun. Koruyucu eldiven ve gözlük kullanın. |
| BİR KİMLİK | UN2451 |
| HS kodu | 2901.1 |
| Tehlike sınıfı | 2.1 |
| Paketleme grubu | Hiçbiri |
| Toksisite | Düşük toksisite |
Neopentan sentez yöntemleri
Tetrametilmetanın sentezlenmesi için birkaç farklı yöntem vardır.
Yaygın bir yöntem, izobüten ve formaldehitin zeolit gibi katı bir asit katalizörü üzerinde reaksiyonunu içerir. Reaksiyon, daha sonra tetrametilmetan verecek şekilde dehidrate edilebilen neopentil alkol üretir.
Tetrametilmetan sentezlemenin başka bir yöntemi, 2,2-dimetilpropanın yüksek sıcaklıklarda termal ayrışmasını içerir. Bu reaksiyon tetrametilmetan ve diğer hidrokarbonları üretir.
Üçüncü bir yöntem, etil klorür ve çinkonun magnezyum varlığında reaksiyona girerek dietilçinko üretmesini içerir; bu daha sonra izobütilen ile reaksiyona girerek tetrametilmetan üretebilir.
Tetrametilmetan, izopentanın dehidrojenasyonundan kaynaklanan izopentenin hidrojenlenmesiyle sentezlenebilir.
Hammaddelerin mevcudiyeti, maliyet, istenen verim ve nihai ürünün saflığı gibi çeşitli faktörlere bağlı olarak, tetrametilmetan sentezinin farklı yöntemleri uyarlanabilir.
Neopentanın Kullanım Alanları
Tetrametilmetanın birçok önemli endüstriyel ve bilimsel uygulaması vardır.
- Yüksek saflığı ve iyi tanımlanmış özellikleri sayesinde gaz kromatografisinde referans malzeme olarak kullanılır.
- Tetrametilmetan ayrıca kalorimetrik ve termodinamik ölçümler için standart olarak kullanılır.
- Tetrametilmetanın bir diğer önemli kullanımı, izolasyon, yastıklama ve paketleme gibi çok çeşitli uygulamalarda kullanılan poliüretan köpüklerin üretiminde şişirici madde olarak kullanılmasıdır.
- Düşük kaynama noktası ve iyi termodinamik özellikleri nedeniyle soğutma sistemlerinde soğutucu olarak kullanılır. Ancak, yüksek yanıcılık özelliği ve potansiyel çevresel etkileri nedeniyle soğutucu olarak kullanımı büyük ölçüde terk edilmiştir.
- Tetrametilmetan ayrıca reçine, kaplama ve plastik üretiminde kullanılan neopentil glikol gibi diğer organik bileşiklerin sentezinde de kullanılır.
Eşsiz özellikleri onu çeşitli endüstriyel ve bilimsel uygulamalar için çok yönlü ve değerli bir bileşik haline getirir. Ancak güvenli ve sorumlu kullanımın sağlanması için tetrametilmetanın potansiyel tehlikeleri dikkatle değerlendirilmeli ve yönetilmelidir.
Sorular:
S: Neopentan (2,2-dimetilpropan) kaç tane kiral karbon atomuna sahiptir?
C: Neopentanın kiral karbon atomu yoktur. Her karbon atomunun etrafında tetrahedral geometriye sahip simetrik bir moleküldür, dolayısıyla tüm karbon atomları eşdeğerdir.
S: Hangisinin kaynama noktası daha yüksek: heksan, pentan veya neopentan?
C: Heksan en yüksek kaynama noktasına sahiptir, bunu pentan ve ardından neopentan takip eder. Aslında bir hidrokarbonun kaynama noktası, molekül ağırlığı ve özgül yüzey alanının yanı sıra moleküller arası kuvvetlerin kuvvetiyle de artar. Heksan, üç bileşik arasında en yüksek moleküler ağırlığa ve spesifik yüzey alanına sahiptir ve aynı zamanda doğrusal yapısı nedeniyle daha yüksek kaynama noktasına yol açan en güçlü moleküller arası kuvvetlere sahiptir. Pentan ve neopentan, daha küçük moleküler boyutları ve daha zayıf moleküller arası kuvvetleri nedeniyle daha düşük kaynama noktalarına sahiptir.
