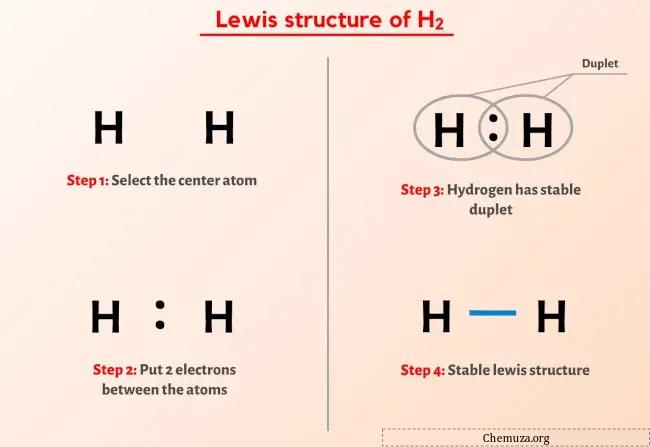
Lewis yapısı H2 (diatomik hidrojen), iki hidrojen (H) atomu arasında tek bir bağa sahiptir.
H2’nin Lewis yapısının yukarıdaki görüntüsünden hiçbir şey anlamadıysanız, benimle kalın ve H2’nin Lewis yapısının çizilmesine ilişkin ayrıntılı adım adım açıklamayı alacaksınız.
O halde H2’nin Lewis yapısını çizmenin basit adımlarına geçelim.
H2 Lewis Yapısını Çizim Adımları
Adım 1: H2 molekülündeki toplam değerlik elektronu sayısını bulun
H2 molekülündeki değerlik elektronlarının toplam sayısını bulmak için öncelikle tek bir hidrojen atomunda bulunan değerlik elektronlarını bilmeniz gerekir.
(Değerlik elektronları herhangi bir atomun en dış yörüngesinde bulunan elektronlardır.)
Burada size periyodik tabloyu kullanarak hidrojenin değerlik elektronlarını nasıl kolayca bulacağınızı anlatacağım.
H2 molekülündeki toplam değerlik elektronları
→ Hidrojen atomunun verdiği değerlik elektronları:
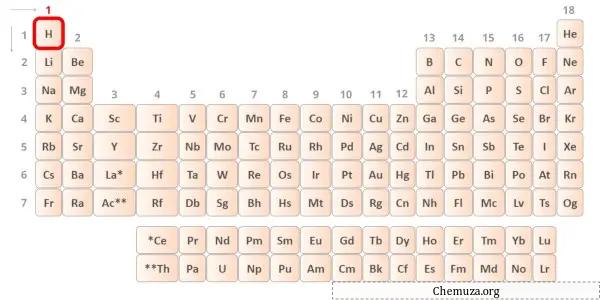
Hidrojen periyodik tablonun 1. grup elementidir. [1] Bu nedenle hidrojende bulunan değerlik elektronu 1’dir .

Yukarıdaki resimde gösterildiği gibi hidrojen atomunda yalnızca bir değerlik elektronunun bulunduğunu görebilirsiniz.
Bu yüzden,
H2 molekülündeki toplam değerlik elektronları = 1(2) = 2 .
Adım 2: bir eskiz yapın
Bir Lewis yapısının taslağını çizerken, daha az elektronegatif olan atomun merkezde kaldığını unutmamalısınız.
Şimdi burada verilen molekül H2’dir (hidrojen). Her iki atom da aynıdır, dolayısıyla atomlardan herhangi birini merkez atom olarak seçebilirsiniz.

Adım 3: Her atomu aralarına bir çift elektron yerleştirerek bağlayın
Şimdi H2 molekülünde elektron çiftlerini iki hidrojen (H) atomu arasına yerleştirmeniz gerekiyor.

Bu, bir H2 molekülünde iki hidrojen (H) atomunun kimyasal olarak birbirine bağlandığını gösterir.
Adım 4: Atomları Kararlı Hale Getirin
Burada H2 molekülünün diyagramında hidrojen atomlarının bir ikili oluşturduğunu ve dolayısıyla kararlı olduğunu görebilirsiniz.
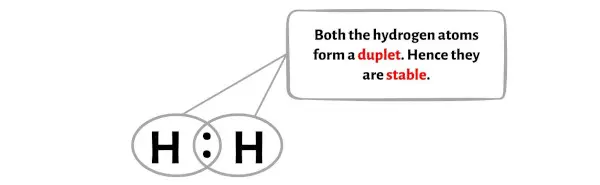
Ek olarak, 1. adımda H2 molekülünde bulunan toplam değerlik elektronu sayısını hesapladık.
H2 molekülünün toplam 2 değerlik elektronu vardır ve bu iki değerlik elektronu yukarıdaki H2 diyagramında kullanılmıştır.
H2’nin yukarıdaki Lewis nokta yapısında, her bir bağ elektronu çiftini (:) tek bir bağ (|) olarak da temsil edebilirsiniz. Bunu yapmak H2’nin aşağıdaki Lewis yapısını elde edecektir.
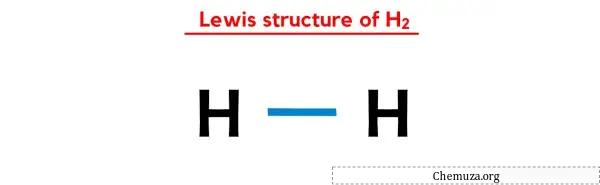
Umarım yukarıdaki tüm adımları tamamen anlamışsınızdır.
Daha fazla pratik yapmak ve daha iyi anlamak için aşağıda listelenen diğer Lewis yapılarını deneyebilirsiniz.
Daha iyi anlamak için şu Lewis yapılarını deneyin (veya en azından görün):
