Klorosülfonik asit, HSO₃Cl formülüne sahip güçlü bir asittir. Çok aşındırıcıdır, organik sentezde reaktif olarak ve deterjan ve boya üretiminde sülfonlama maddesi olarak kullanılır.
| IUPAC’ın adı | Klorosülfonik asit |
| Moleküler formül | HSO₃Cl |
| CAS numarası | 7790-94-5 |
| Eş anlamlı | Sülfürik klorohidrin, klorosülfürik asit, klorosülfonik asit |
| InChI | InChI=1S/ClHO3S/c1-5(2,3)4/h(H,2,3,4) |
Klorosülfonik asidin özellikleri
Klorosülfonik asit formülü
Klorosülfonik asidin formülü HSO₃Cl’dir. Bir hidrojen atomu, bir kükürt atomu, üç oksijen atomu ve bir klor atomundan oluşur.
Klorosülfonik Asit Molar Kütlesi
Klorosülfürik asidin molar kütlesi, onu oluşturan atomların atomik kütleleri toplanarak hesaplanır. HSO₃Cl’nin molar kütlesi mol başına yaklaşık 116,5 gramdır.
Klorosülfonik asidin kaynama noktası
Klorosülfürik asidin kaynama noktası nispeten yüksektir. Yaklaşık 151 santigrat derece (304 Fahrenheit derece). Bu sıcaklıkta klorosülfürik asit sıvı fazdan gaz fazına dönüşür.
Klorosülfonik asit Erime noktası
Klorosülfürik asidin erime noktası yaklaşık -82 santigrat derece (-116 derece Fahrenheit) civarındadır. Bu, klorosülfürik asidin katı formunun sıvıya dönüştüğü sıcaklıktır.
Klorosülfonik asit yoğunluğu g/mL
Klorosülfürik asit, oda sıcaklığında mililitre başına yaklaşık 1,75 gram (g/mL) yoğunluğa sahiptir. Bu, belirli bir hacimdeki klorosülfürik asidin, eşit hacimdeki suya kıyasla nispeten ağır olduğu anlamına gelir.
Klorosülfonik Asit Molekül Ağırlığı
Klorosülfürik asidin moleküler ağırlığı, kimyasal formülündeki tüm atomların atom ağırlıklarının eklenmesiyle hesaplanır. Klorosülfürik asitin molekül ağırlığı mol başına yaklaşık 116,5 gramdır.
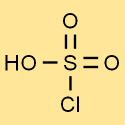
Klorosülfonik asidin yapısı
Klorosülfürik asidin yapısı, üç oksijen atomuna bağlı bir kükürt atomu ve bir klor atomundan oluşur. Hidrojen atomu oksijen atomlarından birine bağlanır. Bu yapı, klorosülfürik aside benzersiz özelliklerini ve reaktivitesini verir.
Klorosülfonik asidin çözünürlüğü
Klorosülfürik asit suda çok çözünür. Suda kolayca çözünür ve kuvvetli asidik bir çözelti oluşturur. Klorosülfürik asidin çözünürlüğü, polar yapısından ve su molekülleri ile hidrojen bağlarının oluşmasından kaynaklanmaktadır.
| Dış görünüş | Renksiz ila sarı sıvı |
| Spesifik yer çekimi | 1,75 (20°C’de) |
| Renk | Renksizden sarıya |
| Koku | Güçlü, keskin koku |
| Molar kütle | 116,5 gr/mol |
| Yoğunluk | 1,75 g/mL (20°C’de) |
| Füzyon noktası | -82°C (-116°F) |
| Kaynama noktası | 151°C (304°F) |
| Flaş noktası | Müsait değil |
| sudaki çözünürlük | karışabilir |
| çözünürlük | Kloroform, diklorometan, nitrobenzen gibi organik çözücülerde çözünür |
| Buhar basıncı | Müsait değil |
| Buhar yoğunluğu | Müsait değil |
| pKa | -2.6 |
| pH | Çok asidik (pH < 1) |
Not: Bu tabloda verilen değerlerin klorosülfürik asit ile ilgili genel özellikler olduğunu lütfen unutmayın. Gerçek değerler, bileşiğin spesifik koşullarına ve saflığına bağlı olarak biraz değişebilir.
Klorosülfonik asidin güvenliği ve tehlikeleri
Klorosülfürik asit önemli güvenlik riskleri oluşturur ve çok dikkatli kullanılmalıdır. Çok aşındırıcıdır ve cilt, göz ve solunum sistemi ile teması halinde ciddi yanıklara neden olabilir. Solunması veya yutulması, solunum sıkıntısı ve iç organlarda hasar gibi ciddi sağlık risklerine neden olabilir. Suyla şiddetli reaksiyona girerek zehirli gazlar açığa çıkarır ve ısı üretir. Organik maddelerle temas halinde yangın ve patlama riskleri mevcuttur. Klorosülfürik asitle çalışırken eldiven, gözlük ve solunum cihazı gibi yeterli kişisel koruyucu ekipman kullanılmalıdır. Bu tehlikeli maddeyle çalışırken maruziyeti en aza indirmek ve güvenliği sağlamak için uygun havalandırma ve muhafaza önlemleri çok önemlidir.
| Tehlike sembolleri | Aşındırıcı (C), Zararlı (Xn) |
| Güvenlik Açıklaması | – Çok dikkatli kullanın\n- Uygun koruyucu ekipman kullanın\n- Ciltle, gözlerle temasından ve solumaktan kaçının\n- İyi havalandırılmış bir alanda saklayın\n- Su veya reaktif maddelerle karıştırmayın |
| BM kimlik numaraları | BM 1751 |
| HS kodu | 28121100 |
| Tehlike sınıfı | Sınıf 8 – Aşındırıcı maddeler |
| Paketleme grubu | Paketleme grubu II |
| Toksisite | Çok zehirli; ciddi yanıklara ve solunum hasarına neden olur |
Klorosülfonik asit sentezi için yöntemler
Klorosülfürik asidi sentezlemek için çeşitli yöntemler vardır. Yaygın bir yöntem, kükürt trioksit (SO₃) ile hidrojen klorür (HCl) arasındaki reaksiyonu içerir. Bu süreçte, klorosülfürik asit üretmek için HCl çözeltisi SO₃ gazıyla kabarcıklandırılır. Reaksiyonun yüksek ekzotermikliği nedeniyle sıcaklık ve reaksiyon koşullarının dikkatli kontrolü gereklidir.
Başka bir yöntemde, klor gazının (Cl₂) sülfürik asit (H₂SO₄) ile reaksiyonundan klorosülfürik asit üretilir. Klor gazının konsantre sülfürik asitten geçişi klorosülfürik asit oluşumuna neden olur. Güvenliği sağlamak için bu ekzotermik reaksiyona karşı uygun önlemleri almalısınız.
Ek olarak, klorosülfürik asidin hazırlanması, sülfürik asidin sülfüril klorür (SO₂Cl₂) ile reaksiyonunu içerir. Sülfüril klorür, sülfürik asitle reaksiyona girerek klorosülfürik asit ve hidrojen klorür gazı oluşturur.
Klorosülfürik asit sentezinin iyi donanımlı bir laboratuvarda uygun güvenlik protokolleri takip edilerek gerçekleştirilmesi gerektiğine dikkat edilmelidir. Kimyager, güvenliğini sağlamak için eldiven, gözlük ve başlık gibi koruyucu ekipman kullanmalıdır.
Bu sentez yöntemleri kimyagerlerin, organik sentez, sülfonasyon reaksiyonları ve boya ve deterjan üretimi dahil olmak üzere çeşitli endüstriyel uygulamalarda kullanılan çok yönlü bir bileşik olan klorosülfürik asit üretmesine olanak tanır.
Klorosülfonik Asitin Kullanım Alanları
Klorosülfürik asit, çok yönlü özelliklerinden dolayı çeşitli endüstrilerde geniş uygulama alanları bulmaktadır. İşte bazı kullanımları:
- Klorosülfürik asit, esterifikasyonlar, sülfonasyonlar ve halojenasyonlar dahil olmak üzere çeşitli organik sentez reaksiyonlarına aktif olarak katılarak güçlü bir reaktif görevi görür. Fonksiyonel grupları etkili bir şekilde tanıtır ve moleküler yapıları değiştirir.
- Boyaların üretiminde klorosülfürik asit çok önemli bir rol oynar çünkü aromatik bileşikleri aktif olarak sülfonatlayarak sülfonik asit gruplarının oluşmasına olanak tanır. Bu gruplar boyaların çözünürlüğünü arttırır ve renk özelliklerini iyileştirir.
- Deterjan üretiminde klorosülfürik asit, deterjan bileşiklerinin sentezi sırasında aktif olarak sülfonlama maddesi olarak işlev görür. Yüzey aktif maddelerin oluşumuna aktif olarak katkıda bulunur, temizleme ve köpüklenme özelliklerini geliştirir.
- İlaç endüstrisi, araştırma ve üretimde aktif bir bileşen olarak klorosülfürik asidi yaygın olarak kullanır. Farmakolojik özellikleri üzerinde önemli bir etkiye sahip olan sülfonamid gruplarını ilaç moleküllerine aktif olarak sokar.
- Polimerizasyon reaksiyonları, özel polimerlerin sentezi için katalizör veya başlatıcı olarak klorosülfürik asidi aktif olarak kullanır. Bu polimerler kaplamalar, yapıştırıcılar ve elektrik yalıtımı gibi çeşitli endüstrilerde aktif olarak uygulama alanı bulmaktadır.
- Sülfonik asitler, sülfürik asit esterleri ve klorosülfonatlar dahil olmak üzere çeşitli kimyasalların üretiminde önemli bir ara madde olarak hizmet eder. Bu bileşikler farmasötikler, tarım kimyasalları ve polimer üretimi gibi çeşitli endüstrilerde uygulama alanı bulmaktadır.
- Laboratuvarda araştırmacılar, esterleşme, asilasyon ve dehidrasyon reaksiyonları gibi çeşitli kimyasal reaksiyonlar için reaktif olarak klorosülfürik asidi aktif olarak kullanıyor.
Aşındırıcı yapısı ve potansiyel sağlık riskleri nedeniyle klorosülfürik asidin dikkatle kullanılması önemlidir.
Sorular:
S: Asetanilid ve klorosülfonik asitten asetamidobenzensülfonil klorürü nasıl oluşturabilirim?
A: Asetamidobenzensülfonil klorür, asetanilitin klorosülfürik asit ile işlenmesiyle oluşturulur, bu da amino grubunun sülfonil klorür grubuyla ikame edilmesiyle sonuçlanır.
S: Klorosülfonik asit nasıl kullanılır?
A: Klorosülfürik asit, fonksiyonel grupları eklemek veya moleküler yapıları değiştirmek için sülfonasyon, esterifikasyon ve asilasyon gibi çeşitli kimyasal reaksiyonlarda reaktif olarak kullanılır.
S: Klorosülfonik asit iyi bir ayrılan grup mudur?
C: Evet, sülfonik asit grubunun stabilitesi ve ikame reaksiyonlarına girebilme yeteneği nedeniyle klorosülfürik asit iyi bir ayrılan gruptur.
S: Klorosülfonik asit nasıl giderilir?
C: Klorosülfürik asit, sodyum karbonat gibi bir bazla nötralize edilmeli, daha sonra suyla seyreltilmeli ve yerel düzenlemelere uygun olarak dikkatli bir şekilde atılmalıdır.
S: Klorosülfonik asit suyla temas ettiğinde ne olur?
C: Klorosülfürik asit suyla temas ettiğinde kuvvetli bir şekilde reaksiyona girerek ısı ve kükürt dioksit ve hidrojen klorür gibi zehirli gazlar açığa çıkarır.
S: Sodyum lauril sülfat, klorosülfonik asidi başka bir reaktifle değiştirerek hazırlanabilir mi?
C: Evet, sodyum lauril sülfat, lauril alkol ile reaksiyonda klorosülfürik asidin sülfürik asit ile değiştirilmesi ve ardından sodyum hidroksit ile nötralizasyon yoluyla sentezlenebilir.
S: Klorosülfonik asidin yoğunluğu nedir?
C: Klorosülfürik asidin yoğunluğu oda sıcaklığında yaklaşık 1,75 g/mL’dir.
Soru: Bir mol asetamidobenzensülfonil klorür üretmek için kaç mol klorosülfonik asit gereklidir?
A: Bir mol asetamidobenzensülfonil klorür, bir mol asetanilidin bir mol klorosülfürik asit ile reaksiyona sokulmasıyla elde edilebilir.
S: Klorosülfonik asit oksidanlarla birlikte saklanabilir mi?
C: Hayır, klorosülfürik asit oksitleyici maddelerden ayrı olarak saklanmalıdır çünkü oksitleyici maddelerle temas ettiğinde şiddetli reaksiyona girebilir veya yangın riskini artırabilir.
