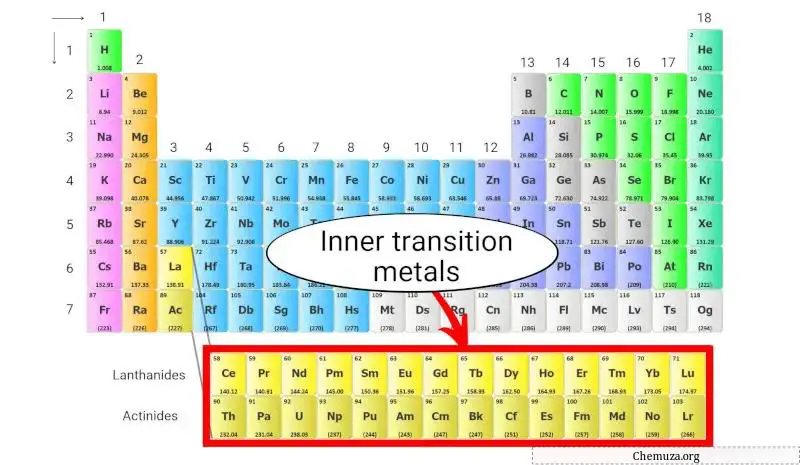
İç geçiş metalleri, periyodik tablonun alt iki sırasında, ana geçiş metali bloğunun hemen altında yer alan bir grup kimyasal elementtir.
İç geçiş metalleri iki gruba ayrılır:
- Lantanitler atom numaraları 57 ila 71 arasında değişen ve
- Aktinitler atom numaraları 89 ile 103 arasında değişen maddelerdir.
Periyodik tablonun iç geçiş elemanlarını daha fazla inceleyelim.
İç geçiş metalleri nelerdir? Peki neden en alta yerleştirilmişler?
İç geçiş metalleri periyodik tablonun en altında yer alan element grubunu oluşturur.
Bu iç geçiş metalleri, geçiş metallerinin yalnızca bir parçasıdır ve ayrıca geçiş metallerine benzer özelliklere sahiptir. Ancak 3. grubun uzantısı olarak iç kısımda yer alırlar.
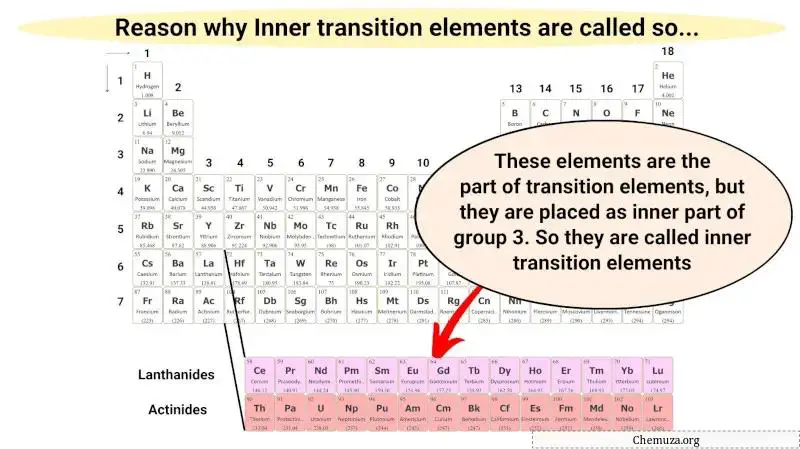
Bu nedenle bu metalik elementlere iç geçiş metalleri adı verilir.
Neden periyodik tablonun en altına yerleştirilirler?
Eğer iç geçiş metalleri grup 3’ün bir uzantısı olarak yerleştirilirse, periyodik tablo çok uzun görünecektir (aşağıda gösterildiği gibi).

Yani A4 formatındaki kağıda sığdırmak için alt tarafa 2 sıra iç geçiş metali yerleştirilir.
Ayrıca, bu iç geçiş elementlerinin değerlik elektronları f-orbitalinde bulunur, bu nedenle bu elementler benzer kimyasal özellikler gösterir.
Bu nedenlerden dolayı iç geçiş metalleri periyodik tablonun en altına yerleştirilir.
İç geçiş metallerinin listesi
İç geçiş metallerinin listesi aşağıda verilmiştir.
| Atomik numara | Sembol | Eleman adı ve sembolü |
| 57 | Orada | Lantan |
| 58 | Bu | Seryum |
| 59 | PR | Praseodimyum |
| 60 | SD | Neodimyum |
| 61 | ÖĞLEDEN SONRA | Prometyum |
| 62 | Biraz | Samaryum |
| 63 | BİZ | Evropyum |
| 64 | Tanrı | Gadolinyum |
| 65 | tüberküloz | Terbiyum |
| 66 | Dy | Disporsiyum |
| 67 | Ho | Holmiyum |
| 68 | Ah | Erbiyum |
| 69 | TM | Tülyum |
| 70 | Yb | İterbiyum |
| 71 | Okumak | Lutesyum |
| 89 | AC | Aktinyum |
| 90 | Bu | Toryum |
| 91 | Pensilvanya | Protaktinyum |
| 92 | sen | Uranyum |
| 93 | Np | Neptünyum |
| 94 | Abilir | Plütonyum |
| 95 | Am | Amerikanyum |
| 96 | santimetre | Curium |
| 97 | B.K. | Berkelyum |
| 98 | Görmek | Kaliforniya |
| 99 | Dır-dir | Einsteinyum |
| 100 | FM | fermiyum |
| 101 | Maryland | Mendelevyum |
| 102 | HAYIR | Nobelyum |
| 103 | Sol/Sağ | Lawrence |
İç geçiş metalleri hakkında gerçekler
İç geçiş metalleri hakkında bazı ilginç gerçekler:
- İki tür iç geçiş metali vardır: lantanitler ve aktinitler. Lantanitler, atom numaraları 57 ( lantan ) ila 71 ( lutesyum ) arasında değişen 15 elementtir; aktinidler ise atom numaraları 89 ( aktinyum ) ila 103 ( lawrensiyum ) arasında değişen 15 elementtir.
- İç geçiş metalleri, f-orbitallerin varlığı nedeniyle benzersiz elektronik konfigürasyonlara sahiptir. Bu, yüksek erime ve kaynama noktaları, karmaşık iyon oluşumu ve paramanyetizma gibi olağandışı kimyasal ve fiziksel özelliklere neden olur.
- İç geçiş metallerinin çoğu radyoaktiftir ve bazıları nükleer reaktörlerde ve silahlarda kullanılmıştır.
- İç geçiş metalleri teknoloji ve endüstride önemlidir. Örneğin, güçlü mıknatıslar yapmak için neodimyum ve samaryum kullanılır [1] ve katalitik konvertörlerde araç emisyonlarını azaltmak için seryum kullanılır. [2]
- Lantanitler aynı zamanda “nadir toprak elementleri” olarak da adlandırılır çünkü bunlar yer kabuğunda nispeten nadirdir. Ancak aslında nadir değildirler ve birçok mineralde bulunurlar.
- Aktinitlerin tümü radyoaktiftir ve uranyum ve plütonyum gibi bazıları nükleer enerji ve silahlar için önemlidir. Ancak radyoaktiviteleri nedeniyle çevre ve sağlık riskleri de taşıyorlar.
- İç geçiş metalleri eski çağlardan beri bilinmektedir ve takı ve dekorasyon için kullanılmıştır. Ancak 20. yüzyıla kadar geniş çapta incelenmemiş veya anlaşılmamıştı.
İç geçiş metallerinin özellikleri
İç geçiş metallerinin bazı özellikleri şunlardır:
- Elektronik konfigürasyon: İç geçiş metalleri kısmen doldurulmuş f-orbitallere sahiptir, bu da onlara benzersiz elektronik konfigürasyonlar ve olağandışı kimyasal ve fiziksel özellikler kazandırır.
- Yüksek erime ve kaynama noktaları: İç geçiş metalleri, f yörüngelerinde eşleşmemiş elektronların varlığından kaynaklanan güçlü metalik bağ nedeniyle yüksek erime ve kaynama noktalarına sahiptir.
- Paramanyetizma: İç geçiş metalleri paramanyetiktir, yani f yörüngelerinde eşleşmemiş elektronların varlığından dolayı manyetik bir alana çekilirler.
- Karmaşık iyonların oluşumu: İç geçiş metalleri, diğer atomlardan veya moleküllerden gelen elektronları barındırabilen boş f yörüngelerinin varlığı nedeniyle karmaşık iyonlar oluşturabilir.
- Radyoaktivite: Birçok iç geçiş metali, çekirdeklerinde kararsız izotopların bulunması nedeniyle radyoaktiftir.
- Oksidasyon durumları: İç geçiş metalleri, f yörüngelerinde çok sayıda değerlik elektronunun bulunması nedeniyle, yüksek oksidasyon durumları da dahil olmak üzere bir dizi oksidasyon durumu sergiler.
- Benzer kimyasal özellikler: Lantanitler ve aktinitlerin benzer kimyasal özellikleri vardır, bu da onların birbirlerinden ayrılmasını zorlaştırır.
- Metalik parlaklık: İç geçiş metalleri genellikle parlaktır ve yüksek ışık yansıtma özelliğinden dolayı metalik bir parlaklığa sahiptir.
İç geçiş metallerinin kullanımları
İç geçiş metalleri benzersiz özelliklerinden dolayı geniş bir kullanım alanına sahiptir. İç geçiş metallerinin bazı kullanım alanları şunlardır:
- Nükleer enerji: Pek çok iç geçiş metali, özellikle de uranyum gibi aktinit, nükleer reaktörler ve silahlar için yakıt olarak kullanılır.
- Mıknatıslar: Neodimyum, samaryum ve gadolinyum gibi lantanitler, bilgisayar sabit diskleri, rüzgar türbinleri ve MRI makineleri dahil olmak üzere çeşitli uygulamalar için güçlü mıknatıslar yapmak için kullanılır.
- Aydınlatma: Floresan ve LED aydınlatma için fosfor yapımında europium ve terbium gibi lantanitler kullanılır. [3]
- Kataliz: Seryum gibi lantanitler, petrol rafinerisi ve kirlilik kontrolü dahil olmak üzere birçok endüstriyel proseste katalizör olarak kullanılır.
- Cam üretimi: Erbiyum ve iterbiyum gibi lantanitler camı renklendirmek için kullanılırken, seryum camı parlatmak için kullanılır.
- Tıbbi görüntüleme: Gadolinyum ve terbiyum gibi lantanitler, MRI taramaları için kontrast maddelerde kullanılır. [4]
- Elektronik: Disprosyum ve terbiyum gibi lantanitler, mikrodalga filtreleri ve LCD ekranlar gibi elektronik cihazlarda kullanılır.
- Savunma: Nükleer silahlar ve zırh delici mühimmatlar da dahil olmak üzere savunma teknolojilerinde iç geçiş metalleri kullanılır.
Özet
İç geçiş metalleri, periyodik tablonun alt iki sırasında, ana geçiş metali bloğunun hemen altında yer alan bir grup kimyasal elementtir.
İki gruba ayrılırlar: Atom numaraları sırasıyla 57 ila 71 ve 89 ila 103 arasında değişen Lantanitler ve Aktinitler.
İç geçiş metallerinin yeri periyodik tablonun en altındadır çünkü değerlik elektronları benzer kimyasal özelliklere sahip olan f yörüngesindedir.
İç geçiş metalleri yüksek erime ve kaynama noktalarına, karmaşık iyon oluşumuna ve paramanyetizmaya sahiptir. Ayrıca f-orbitallerinde çok sayıda değerlik elektronunun mevcudiyeti nedeniyle yüksek oksidasyon durumları da dahil olmak üzere bir dizi oksidasyon durumu sergilerler.
