Fosfor pentaklorür PCl5 formülüne sahip kimyasal bir bileşiktir. Çeşitli kimyasal reaksiyonlarda reaktif olarak kullanılır. Suyla kuvvetli reaksiyona girerek hidrojen klorür gazı açığa çıkarır.
| IUPAC Adı | Fosfor pentaklorür |
| Moleküler formül | PCI5 |
| CAS numarası | 10026-13-8 |
| Eş anlamlı | Pentaklorofosforan, fosfor (V) klorür, fosfor klorür, fosfor (V) klorür |
| InChI | InChI=1S/Cl5P/c1-6(2,3,4)5 |
Fosfor pentaklorürün özellikleri
Fosfor Pentaklorür Formülü
Fosfor pentaklorürün formülü PCl5’tir. Beş klor atomuna bağlı bir fosfor atomundan oluşur. Formül bileşikteki atomların oranını temsil eder.
Fosfor Pentaklorür Molar Kütlesi
Fosfor(V) klorürün molar kütlesi, onu oluşturan tüm elementlerin atomik kütleleri toplanarak hesaplanır. Fosforun molar kütlesi mol başına yaklaşık 30,97 gramdır ve her klor atomunun molar kütlesi mol başına yaklaşık 35,45 gramdır. Bunların eklenmesi, fosfor (V) klorür için mol başına yaklaşık 208,24 gramlık bir molar kütle sağlar.
Fosfor pentaklorürün kaynama noktası
Fosfor (V) klorürün kaynama noktası yaklaşık 167,8 santigrat derecedir. Bu sıcaklıkta bileşik sıvıdan gaza faz değişimine uğrar. Kaynama noktası bileşikte mevcut olan moleküller arası kuvvetlerden etkilenir.
Fosfor pentaklorür Erime noktası
Fosfor(V) klorürün erime noktası yaklaşık -93,6 santigrat derecedir. Bu, bileşiğin katı halden sıvı duruma geçtiği sıcaklıktır. Erime noktası, bileşiğin fiziksel davranışını belirlemede önemli bir özelliktir.
Fosfor pentaklorürün yoğunluğu g/mL
Fosfor(V) klorürün yoğunluğu mililitre başına yaklaşık 2,1 gramdır. Yoğunluk, bir maddenin birim hacim başına kütlesini temsil eder. Fosfor (V) klorürün yoğunluğu, parçacıklarının düzenini ve kompaktlığını anlamaya yardımcı olur.
Fosfor Pentaklorür Molekül Ağırlığı
Fosfor(V) klorürün moleküler ağırlığı mol başına yaklaşık 208,24 gramdır. Bileşikte bulunan tüm atomların atom ağırlıklarının toplamıdır. Molekül ağırlığı, belirli bir kütle veya hacimdeki madde miktarının belirlenmesi gibi çeşitli hesaplamalarda faydalıdır.
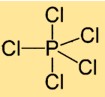
Fosfor pentaklorürün yapısı
Fosfor (V) klorür, bir fosfor atomunun beş klor atomu ile çevrelendiği moleküler bir yapıya sahiptir. Klor atomları merkezi fosfor atomunun etrafında simetrik olarak düzenlenir ve trigonal çift piramidal bir geometri oluşturur.
Fosfor pentaklorürün çözünürlüğü
Fosfor (V) klorür suda çok az çözünür. Suyla kuvvetli reaksiyona girerek hidrojen klorür gazı açığa çıkarır. Ancak benzen ve karbon tetraklorür gibi polar çözücülerde kolaylıkla çözünür. Fosfor(V) klorürün çözünürlüğü solventin polaritesi ve kimyasal özelliklerinden etkilenir.
| Dış görünüş | Renksiz kristaller |
| Spesifik yer çekimi | 2,1g/ml |
| Renk | Renksiz |
| Koku | Dönüm |
| Molar kütle | 208,24 gr/mol |
| Yoğunluk | 2,1g/ml |
| Füzyon noktası | -93,6°C |
| Kaynama noktası | 167,8°C |
| Flaş noktası | Uygulanamaz |
| sudaki çözünürlük | Şiddetli tepki veriyor |
| çözünürlük | Benzen ve karbon tetraklorür gibi polar çözücülerde çözünür |
| Buhar basıncı | Müsait değil |
| Buhar yoğunluğu | Müsait değil |
| pKa | Müsait değil |
| pH | Uygulanamaz |
Fosfor pentaklorürün güvenliği ve tehlikeleri
Fosfor (V) klorür çeşitli güvenlik riskleri oluşturur. Aşındırıcıdır ve temas halinde ciltte, gözlerde ve solunum sisteminde ciddi yanıklara neden olabilir. Dumanının veya tozunun solunması tahrişe ve solunum hasarına neden olabilir. Bileşik suyla şiddetli reaksiyona girerek toksik hidrojen klorür gazı açığa çıkarır. Ayrıca organik maddelerle çok reaktiftir ve potansiyel olarak yangına veya patlamaya neden olur. Fosfor(V) klorür kullanılırken eldiven, gözlük ve solunum cihazı gibi koruyucu ekipmanların kullanımı da dahil olmak üzere uygun önlemler alınmalıdır. Kazaları önlemek ve riskleri en aza indirmek için iyi havalandırılmış, uyumsuz maddelerden uzak bir alanda saklanmalı ve kullanılmalıdır.
| Tehlike sembolleri | Aşındırıcı |
| Güvenlik Açıklaması | Depozito ile işlem yapın. Uygun koruyucu ekipman kullanın. |
| BM kimlik numaraları | UN1806 |
| HS kodu | 2812.20.00 |
| Tehlike sınıfı | 8 (Aşındırıcı maddeler) |
| Paketleme grubu | II (Orta dereceli tehlike) |
| Toksisite | Yutulması veya solunması halinde toksiktir. Ciddi tahrişe neden olabilir. |
Fosfor pentaklorür sentez yöntemleri
Çeşitli yöntemler fosfor (V) klorürün sentezine izin verir. Yaygın bir yöntem, fosfor triklorür (PCl3) ile klor gazı (Cl2) arasındaki reaksiyonu içerir. Bu işlemde reaksiyon kabı hem bileşikleri hem de ısıyı birleştirir veya demir gibi bir katalizör reaksiyonu başlatır. Klor gazı, PCl3’ü PCl5’e dönüştüren bir oksitleyici madde görevi görür. Reaksiyon şu şekilde ilerler:
PCl3 + Cl2 → PCl5
Fosfor (V) klorürü sentezlemenin başka bir yöntemi, fosfor ve klor gazı arasındaki reaksiyonu içerir. Bu yöntem daha doğrudandır ve aşağıdaki reaksiyonu içerir:
P4 + 10Cl2 → 4PCl5
Bu reaksiyonda fosfor ve klor gazı uygun koşullar altında reaksiyona girerek fosfor(V) klorürün oluşmasına neden olur.
Her iki sentez yönteminin de dikkatli kullanım ve uygun güvenlik önlemleri gerektirdiğini unutmamak önemlidir. Reaksiyonlar oldukça reaktif ve aşındırıcı maddeler içerdiğinden koruyucu ekipman ve yeterli havalandırma gereklidir. Ayrıca kazaları önlemek ve olaya karışan personelin güvenliğini sağlamak için bu reaksiyonların kontrollü bir ortamda gerçekleştirilmesi esastır.
Fosfor pentaklorürün kullanım alanları
Fosfor (V) klorür, benzersiz özellikleri ve reaktivitesi nedeniyle çeşitli uygulamalar bulur. İşte bazı kullanımları:
- Kimyasal sentez: Organik sentez, karboksilik asitleri asit klorürlere ve alkolleri alkil klorürlere dönüştürmek için reaktif olarak yaygın olarak fosfor(V) klorür kullanır.
- Farmasötikler: Antibiyotikler ve boyalar da dahil olmak üzere farmasötik bileşiklerin sentezi, önemli bir ara madde olarak büyük ölçüde fosfor(V) klorüre dayanır.
- Katalizör: Fosfor (V) klorür, Friedel-Crafts asilasyonu ve Beckmann yeniden düzenlenmesi gibi çeşitli kimyasal reaksiyonları katalize eder.
- Polimer endüstrisi: Polivinil klorür (PVC) ve polikarbonatlar da dahil olmak üzere çeşitli polimerlerin üretiminde klorlama maddesi olarak fosfor(V) klorür kullanılır.
- Laboratuar Uygulamaları: Laboratuar uygulamalarında, fosfor(V) klorür, laboratuar aparatlarından su izlerini uzaklaştırmak için bir kurutma maddesi olarak ve çeşitli reaksiyonlarda bir klorlama ve dehidrasyon maddesi olarak görev yapar.
- Herbisitler ve Pestisitler: Yabani otların büyümesini kontrol etmek ve zararlıları ortadan kaldırmak için herbisit ve pestisitlerin üretimi, fosfor (V) klorürün kullanımını içerir.
- Kimyasal Savaş Ajanları: Tarihsel olarak fosfor(V) klorür, kimyasal savaş ajanlarının üretimine aktif olarak katkıda bulunmuştur, ancak bu amaçlarla kullanımı artık katı düzenlemelere ve kısıtlamalara tabidir.
- Metal Yüzey İşlemi: Metal yüzey işleme prosesleri, yapışma özelliklerini geliştirmek ve korozyon direncini arttırmak için fosfor (V) klorür kullanır.
- Alev Geciktiriciler: Tekstil, plastik ve diğer malzemelere yönelik alev geciktirici katkı maddelerinin üretiminde fosfor(V) klorür bulunur.
- Farmasötik Üretim: Fosfor(V) klorür, vitaminler ve hormon türevlerinin sentezi de dahil olmak üzere çeşitli farmasötik ürünlerin üretiminde uygulama alanı bulur.
Aşındırıcı yapısı ve potansiyel sağlık riskleri nedeniyle fosfor(V) klorürün dikkatle kullanılması ve uygun güvenlik protokollerinin takip edilmesi önemlidir.
Sorular:
S: Fosfor pentaklorürün doğru formülü nedir?
C: Fosfor(V) klorürün doğru formülü PCl5’tir.
S: Fosfor pentaklorürün moleküler formülü nedir?
C: Fosfor(V) klorürün moleküler formülü PCl5’tir.
S: 15,2 g P4’ün tam reaksiyonuyla hangi kütlede fosfor pentaklorür üretilir?
A: Üretilen fosfor (V) klorürün kütlesi yaklaşık 208,24 g olacaktır.
S: Fosfor pentaklorürün formu nedir?
A: Fosfor (V) klorürün şekli trigonal çift piramidaldir.
S: Fosfor pentaklorür molekülünün kütlesi nedir?
C: Bir fosfor(V) klorür molekülünün kütlesi mol başına yaklaşık 208,24 gramdır.
S: Fosfor pentaklorürün özellikleri?
C: Fosfor (V) klorür aşındırıcıdır, suyla şiddetli reaksiyona girer ve kimyasal sentezde reaktif olarak kullanılır.
S: Fosfor(V) klorürün bağ açıları?
C: Fosfor pentaklorürdeki bağ açıları yaklaşık 120 derece (ekvatordaki klor atomları arasında) ve 90 derecedir (eksenel klor atomları arasında).
S: Fosfor pentaklorür nasıl yapılır?
A: Fosfor (V) klorür, fosfor triklorürün (PCl3) klor gazı (Cl2) ile reaksiyona sokulması veya fosfor ile klor gazı arasında doğrudan reaksiyona sokulması yoluyla yapılabilir.
S: Fosfor pentaklorürdeki fosforun elektronik geometrisi nedir?
A: Fosfor (V) klorürdeki fosforun elektronik geometrisi trigonal çift piramidaldir.
