Demir III nitrat kimyasal bir bileşiktir. Demir iyonlarının nitrat iyonlarıyla birleştirilmesiyle oluşur. Endüstriyel uygulamalarda ve laboratuvar reaktifi olarak yaygın olarak kullanılır.
| IUPAC Adı | Demir(III) nitrat |
| Moleküler formül | Fe(NO3)3 |
| CAS numarası | 10421-48-4 |
| Eş anlamlı | Ferrik nitrat, demir trinitrat, nitrik asidin demir (III) tuzu |
| InChI | InChI=1S/Fe.3NO3/c;3 2-1(3)4/q+3;3 -1 |
Demir (III) nitratın özellikleri
Demir(III) nitrat formülü
Demir III nitratın formülü Fe(NO3)3’tür. Bir demir iyonu (Fe) ve üç nitrat iyonundan (NO3) oluşur. Bu formül demir katyonunun nitrat anyonlarıyla birleşimini temsil eder.
Demir(III) Nitrat Molar Kütlesi
Demir nitratın molar kütlesi, onu oluşturan elementlerin atomik kütleleri toplanarak hesaplanabilir. Demirin (Fe) molar kütlesi 55,845 g/mol iken, her nitrat iyonunun (NO3) molar kütlesi 62,0049 g/mol’dür. Bu değerlerin eklenmesi demir nitrat için yaklaşık 241,86 g/mol molar kütle verir.
Demir (III) nitratın kaynama noktası
Demir nitratın belirli bir kaynama noktası yoktur. Isıtıldığında çeşitli nitrojen oksitlere ayrışır ve sonuçta demir oksit oluşturur. Ayrışma sıcaklığı, konsantrasyon ve diğer maddelerin varlığı gibi faktörlere bağlıdır.
Demir (III) nitratın erime noktası
Demir nitratın erime noktası yaklaşık 47°C’dir (117°F). Bu sıcaklıkta katı bileşik sıvı duruma dönüşür. Erime noktasının safsızlıklar veya bileşiğin tam bileşimi gibi faktörlere bağlı olarak biraz değişebileceğini unutmamak önemlidir.
Demir(III) nitratların yoğunluğu g/mL
Fe(NO3)3’ün yoğunluğu yaklaşık 1,68 g/mL’dir. Yoğunluk, bir maddenin birim hacmi başına kütlesini temsil eder. Bu durumda bileşiğin mililitre başına Fe(NO3)3 kütlesini gösterir.
Demir(III) Nitrat Molekül Ağırlığı
Demir nitratın moleküler ağırlığı yaklaşık 241,86 g/mol’dür. Molekül ağırlığı, bir moleküldeki tüm atomların atom ağırlıklarının toplamını ifade eder.
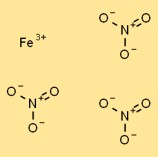
Demir (III) nitratın yapısı
Demir nitrat katı halde kristal yapıya sahiptir. Koordineli nitrat anyonları (NO3-) ile çevrelenmiş Fe3+ katyonlarından oluşur. Demir katyonları iyonik bağlarla bir arada tutulurken, nitrat anyonları elektrostatik kuvvetler tarafından katyonlara çekilir.
Demir(III) nitratların çözünürlüğü
Demir nitrat suda çok çözünür. Berrak, soluk sarı bir çözelti oluşturmak için suda kolayca çözünür. Demir nitratın diğer çözücüler veya maddeler içindeki çözünürlüğü değişebilir.
| Dış görünüş | Soluk sarı kristaller |
| Spesifik yer çekimi | 1.68 |
| Renk | Soluk sarı |
| Koku | Kokusuz |
| Molar kütle | 241,86 gr/mol |
| Yoğunluk | 1.68g/ml |
| Füzyon noktası | 47°C (117°F) |
| Kaynama noktası | ayrıştırılmış |
| Flaş noktası | Uygulanamaz |
| sudaki çözünürlük | Çok çözünür |
| çözünürlük | Suda ve polar çözücülerde çözünür |
| Buhar basıncı | Müsait değil |
| Buhar yoğunluğu | Müsait değil |
| pKa | Müsait değil |
| pH | Asit |
Demir(III) Nitratın Güvenliği ve Tehlikeleri
Demir nitrat bazı güvenlik riskleri oluşturur ve kullanırken dikkatli olunmalıdır. Cildi, gözleri ve solunum sistemini tahriş edici olduğu düşünülmektedir. Bileşik ile doğrudan temastan kaçınılmalı ve eldiven ve gözlük gibi koruyucu ekipmanlar giyilmelidir. Demir nitratın yutulması veya solunması zararlı etkilere neden olabilir ve bu nedenle yutulmamalı veya solunmamalıdır. Solunum riskini en aza indirmek için bu bileşikle iyi havalandırılmış bir alanda çalışmak önemlidir. Kazara maruz kalma veya yutulma durumunda derhal tıbbi yardıma başvurulmalıdır. Güvenliği sağlamak için uygun depolama ve taşıma uygulamalarına uyulmalıdır.
| Tehlike sembolleri | Xi,O |
| Güvenlik Açıklaması | Cilt ve göz tahrişine neden olur. Solunum yolu tahrişine neden olabilir. Yutulduğunda zararlı. |
| BM kimlik numaraları | UN 1466 (Susuz) |
| HS kodu | 28342990 |
| Tehlike sınıfı | 5.1 (Oksitleyici madde) |
| Paketleme grubu | II |
| Toksisite | Orta derecede toksisite |
Demir (III) nitratın sentezi için yöntemler
Demir nitrat çeşitli yöntemlerle sentezlenebilir; yaygın yöntem, demir(III) oksidin (Fe2O3) konsantre nitrik asit (HNO3) içinde çözülmesidir. Bu reaksiyon, aşağıdaki denklemle temsil edilen demir nitratın oluşumuyla sonuçlanır:
Konsantre nitrik asit demir(III) oksidi çözerek Fe(NO3)3 üretmenin yanı sıra su da üretir:
Fe2O3 + 6HNO3 → 2Fe(NO3)3 + 3H2O.
Başka bir yöntem, metalik demirin, demiri oksitleyerek demir nitrat oluşturan bir nitrik asit ve hidrojen peroksit karışımıyla birleştirilmesini içerir. Bu iyi bilinen reaksiyon “aqua regia” yöntemi adını hak ediyor.
Nitrik asit ve hidrojen peroksit karışımına metalik demir eklenmesi, demir nitrat ve su üretimine yol açar:
2Fe + 8HNO3 + 6H2O2 → 2Fe(NO3)3 + 6H2O.
İlgili kimyasalların aşındırıcı ve oksitleyici yapısı nedeniyle bu reaksiyonları gerçekleştirirken dikkatli olmak çok önemlidir. Koruyucu giysiler giymek ve iyi havalandırılmış bir alanda çalışmak gibi uygun güvenlik önlemlerine uymak gerekir.
Saygın kimyasal tedarikçileri, ticari olarak temin edilebilen demir nitratı sunarak endüstrilerdeki ve laboratuvarlardaki çeşitli uygulamalar için tutarlı ve güvenilir bir bileşik kaynağı sağlar.
Demir (III) nitratın kullanımları
Demir nitratın çeşitli endüstrilerde ve laboratuvarlarda birçok pratik kullanımı vardır. İşte demir nitratın bazı önemli uygulamaları:
- Endüstriyel katalizör: Naylon ve diğer polimerlerin üretimi de dahil olmak üzere çeşitli endüstriyel işlemlerde katalizör olarak demir nitrat kullanılır.
- Boyama ve Pigmentler: Boyama ve pigmentleme endüstrisi, boyaları kumaşlara sabitlemek ve renk haslığını arttırmak için mordan olarak demir nitratı kullanır.
- Dağlayıcı: Metal işleme ve elektronik endüstrileri, metal yüzeyler üzerinde karmaşık desenler ve tasarımlar oluşturmak için demir nitratı aşındırıcı olarak kullanır.
- Laboratuvar Reaktifi: Demir nitrat, özellikle diğer bileşiklerin sentezi için çeşitli kimyasal reaksiyonlar ve deneyler için ortak bir laboratuvar reaktifi görevi görür.
- Oksitleyici Ajan: Demir nitrat, güçlü oksitleyici özelliklerinden dolayı organik sentez dahil kimyasal reaksiyonlarda oksitleyici ajan olarak görev yapar.
- Su Arıtma: Demir nitrat, su arıtma proseslerinde endüstriyel atık sudan fosfatlar ve sülfitler gibi yabancı maddeleri uzaklaştırmak için faydalıdır.
- Fotoğrafçılık: Bazı fotografik işlemlerde, özellikle demir bazlı fotografik emülsiyonların hazırlanmasında demir nitrat kullanılır.
- Analitik Kimya: Demir nitrat, belirli maddeleri tespit etmek ve ölçmek için kolorimetrik analiz gibi analitik kimya tekniklerinde uygulama alanı bulur.
- Ahşabın Korunması: Ahşap koruyucu tedaviler, ahşabı mantar çürümesinden ve böcek istilasından korumak için aktif bileşen olarak demir nitratı kullanır.
- Farmasötik uygulamalar: Bazı farmasötik ürünlerin ve ilaçların formülasyonu demir nitratın kullanımını içerir.
Aşındırıcı ve oksitleyici yapısı nedeniyle demir nitratla çalışırken uygun kullanım ve güvenlik önlemlerinin alınması gerektiğine dikkat etmek önemlidir.
Sorular:
S: Demir(III) nitrat yanıcı mıdır?
C: Hayır, demir nitrat yanıcı değildir.
S: Demir(III) nitratın güvenlik ve kullanım sorunları nelerdir?
C: Güvenlik endişeleri ciltte, gözlerde ve solunum yollarında tahrişi içerir. Bu nedenle uygun koruyucu ekipman ve önlemlerle kullanılmalıdır.
S: Hangi formül demir(III) nitratı temsil eder?
C: Demir nitratın formülü Fe(NO3)3’tür.
Soru: Demir(III) nitratın formülü nedir?
C: Demir(III) nitratın formülü Fe(NO3)3’tür.
Soru: Demir(III) nitratın molar kütlesi nedir?
A: Fe(NO3)3’ün molar kütlesi yaklaşık 241,86 g/mol’dür.
Soru: Demir hidroksit suda çözünür mü?
C: Demir hidroksit suda çok az çözünür.
S: Demir(III) nitratla reaksiyona girer mi?
C: Hayır, kalsiyum (Ca) genellikle Fe(NO3)3 ile reaksiyona girmez.
S: Aspirinin hangi kısmı demir(III) nitrat ile reaksiyona girer?
C: Demir(III) nitrat, aspirin molekülünde bulunan karboksilat grubu (-COO-) ile reaksiyona girer.
Soru: Demir(III) nitratın moleküler kütlesi nedir?
C: Fe(NO3)3’ün moleküler kütlesi yaklaşık 241,86 g/mol’dür.
S: Al, demir(III) nitratla reaksiyona girer mi?
C: Evet, alüminyum (Al), Fe(NO3)3 ile reaksiyona girerek alüminyum nitrat ve metalik demir oluşturabilir.
Soru: 3,80 M demir(III) nitrat çözeltisindeki 50,0 g suda kaç mol nitrat çözülür?
C: Nitrat molünü belirlemek için çözeltinin hacmi gereklidir, çünkü yalnızca suyun molaritesi ve kütlesi sağlanır.
