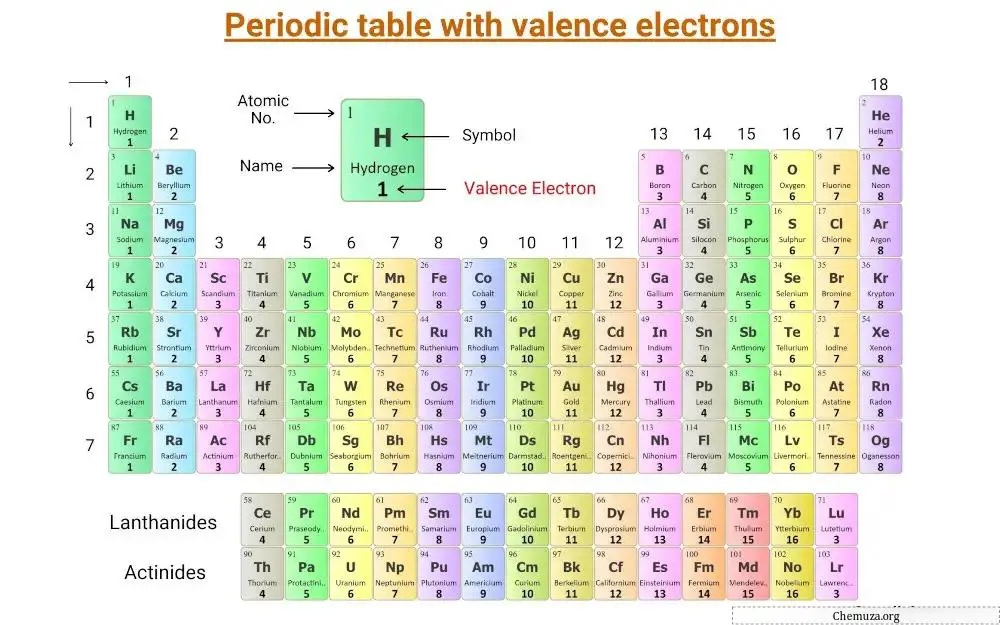
Bu, değerlik elektronlarının etiketlendiği periyodik bir tablodur .
Değerlik elektronları kavramını, ana grup elementlerinin ve geçiş elementlerinin değerlik elektronlarının sayısıyla birlikte anlayalım.
Değerlik elektronları nedir?
Değerlik elektronları, kimyasal bağlanmada yer alan bir atomun en dış kabuğunda veya enerji seviyesinde bulunan elektronlardır.
Örneğin magnezyumun en dış yörüngesinde 2 elektronu vardır, dolayısıyla 2 değerlik elektronu vardır. [1]
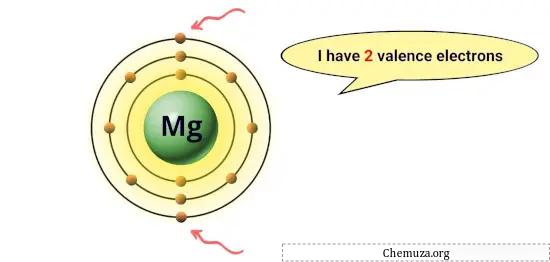
Bu elektronlar, bir elementin reaktifliği ve diğer atomlarla oluşturabileceği kimyasal bağ türleri gibi kimyasal özelliklerinden sorumludur.
Bir atomun sahip olduğu değerlik elektronlarının sayısı, onun periyodik tablodaki konumunu ve kimyasal bağ oluşturma yeteneğini belirler.
Ana grup elementlerinin değerlik elektronları
Temsili elementler olarak da adlandırılan ana grup elementleri, periyodik tablonun 1, 2 ve 13’ten 18’e kadar olan gruplarında bulunur.
Bu elementlerdeki değerlik elektronlarının sayısı grup numaralarına eşittir.
Örneğin, lityum ve sodyum gibi Grup 1 elementleri bir değerlik elektronuna sahipken, magnezyum ve kalsiyum gibi Grup 2 elementleri iki değerlik elektronuna sahiptir.
Bor ve alüminyum gibi Grup 13 elementlerinin üç değerlik elektronu vardır ve bu böyle devam eder.
Bu değerlik elektronları, elementlerin benzersiz kimyasal özelliklerinden ve reaktivitesinden sorumludur.
Geçişin değerlik elektronları ve iç geçiş elemanları
Geçiş elemanlarının ve iç geçiş elemanlarının değerlik elektronlarının belirlenmesi, ana grup elemanlarının değerlik elektronlarının belirlenmesinden daha karmaşıktır.
Gerçekte, geçiş elemanlarının alt katmanı d ve iç geçiş elemanlarının alt katmanı f tam olarak doldurulmamıştır ve dış alt katmana s çok yakındır.
Sonuç olarak, geçiş elemanlarındaki d ve s alt kabuklarının ve iç geçiş elemanlarındaki f ve s alt kabuklarının elektronları değerlik elektronları gibi davranabilir.
Geçiş elemanları için değerlik elektronları, d-alt kabuk ve s-alt kabuk elektronlarının katkısı nedeniyle 3 ila 12 arasında değişebilir. Bazı durumlarda tamamlanmamış d yörüngelerindeki elektronlar da değerlik elektronları olarak kabul edilir. [2]
Benzer şekilde, iç geçiş elemanları (veya f-blok elemanları) için, değerlik elektronları, f-alt kabuk ve s-alt kabuk elektronlarının katkısı nedeniyle 3 ila 16 arasında değişebilir. [3] Tamamlanmamış d yörüngelerindeki elektronlar, bazı iç geçiş metallerindeki değerlik elektronları olarak da düşünülebilir.
Geçiş ve iç geçiş elemanları için değerlik elektronlarının, soy gaz çekirdeğinin dışındaki kabuklarda bulunan elektronlar olduğuna dikkat etmek önemlidir.
