Benzil veya C14H10O2, boyaların sentezinde öncü olarak ve polimer kimyasında fotobaşlatıcı olarak kullanılan sarı kristalli bir organik bileşiktir. Aynı zamanda indirgeyici bir madde olarak da görev yapabilir ve benzilik asit oluşumunda bir ara maddedir.
| IUPAC Adı | 1,2-difenil-1,2-dikarboksietilen |
| Moleküler formül | C14H10O2 |
| CAS numarası | 134-81-6 |
| Eş anlamlı | 1,2-Difenil-1,2-propandion, 1,2-Difeniletanedion, Benzilyum, Benzil |
| InChI | InChI=1S/C14H10O2/c15-13(14(16)17)11-6-8-12(9-7-11)10-5-3-1-2-4-6/h1-9H,10- 17H2 |
Benzil Molekül Ağırlığı
Benzilin moleküler ağırlığı 210,24 g/mol’dür. Bir benzil molekülündeki tüm atomların atomik kütlelerinin toplamıdır. Benzilin moleküler ağırlığı, C14H10O2 moleküler formülüne göre hesaplanır.
Benzil Yoğunluğu g/mL
Benzilin yoğunluğu 1,20 g/mL’dir. Bir maddenin birim hacmi başına kütlesinin ölçümüdür. Benzil’in yoğunluğunun nispeten düşük olması, diğer yüksek yoğunluklu maddelerle karşılaştırıldığında işlenmesini kolaylaştırır.
Benzilin kaynama noktası
Benzinin kaynama noktası 350°C’dir (662°F). Bir sıvının buhar basıncının atmosfer basıncına eşit olduğu ve sıvının buhara dönüştüğü sıcaklıktır. Bir maddenin kaynama noktası basınç, molekül ağırlığı ve moleküller arası kuvvetler gibi çeşitli faktörlere bağlıdır.
Benzil Erime Noktası
Benzilin erime noktası 98°C’dir (270°F). Bu, katının sıvıya dönüştüğü sıcaklıktır. Benzilin erime noktası nispeten düşüktür, bu da onu organik sentezlerde yararlı bir ara madde haline getirir.
Benzil Molar Kütlesi
C14H10O2’nin molar kütlesi 210,24 g/mol’dür. 12 gram saf karbon-12’nin içerdiği varlık sayısıyla aynı sayıda varlık (örneğin atom, molekül, iyon) içeren madde miktarıdır. Benzilin molar kütlesi, C14H10O2 moleküler formülüne göre hesaplanır.
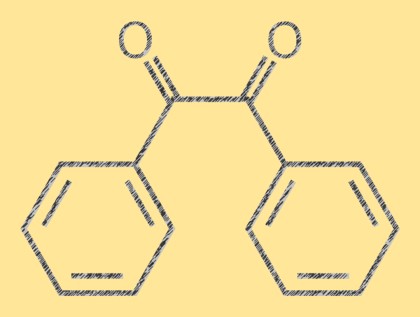
Benzilin yapısı
Benzil, C14H10O2 moleküler formülüne sahip sarı kristalli bir organik bileşiktir. Merkezi bir karbon-karbon çift bağına bağlı iki fenil grubundan oluşan bir diketondur. Molekül düzlemseldir ve çift bağ düzlemseldir. Benzil molekülü, onu analitik kimyada referans bileşik olarak faydalı kılan karakteristik bir parlak sarı renge sahiptir.
Benzil Formülü
Benzilin kimyasal formülü C14H10O2’dir. Benzili oluşturan elementleri ve bunların göreceli oranlarını temsil eder. Formül, benzilin 14 karbon atomu, 12 hidrojen atomu ve 2 oksijen atomundan oluştuğunu gösterir.
Benzil NMR
C14H10O2 nükleer manyetik rezonans (NMR) spektroskopisi ile analiz edilebilir. NMR spektroskopisi, moleküllerin kimyasal yapısı ve etkileşimleri hakkında bilgi sağlayan güçlü bir araçtır. NMR spektroskopisinde çekirdeğin manyetik özellikleri, çekirdeğin kimyasal ortamını belirlemek ve molekülün bağları ve kimyasal kaymaları hakkında bilgi elde etmek için kullanılır. C14H10O2 NMR spektrumu, moleküldeki proton sayısı ve her protonun kimyasal ortamı hakkında bilgi sağlayarak C14H10O2’nin yapısının doğrulanmasına yardımcı olur.
| Dış görünüş | Sarı kristal katı |
| Spesifik yer çekimi | 1.20g/ml |
| Renk | SARI |
| Koku | Kokusuz |
| Molar kütle | 210,24 gr/mol |
| Yoğunluk | 1.20g/ml |
| Füzyon noktası | 94,8°C |
| Kaynama noktası | 350°C (662°F) |
| Flaş noktası | Müsait değil |
| sudaki çözünürlük | Suda az çözünür |
| çözünürlük | Etanol ve eterde çözünür |
| Buhar basıncı | Müsait değil |
| Buhar yoğunluğu | Müsait değil |
| pKa | Müsait değil |
| pH | Müsait değil |
Benzilin güvenliği ve tehlikeleri
C14H10O2 orta derecede toksik bir madde olarak kabul edilir ve dikkatle kullanılmalıdır. Oldukça yanıcıdır ve ısı kaynaklarından ve kıvılcımlardan uzak tutulmalıdır. C14H10O2 buharlarının solunması göz, burun ve boğazda tahrişe ve solunum problemlerine neden olabilir. C14H10O2 ile cilt teması ciltte tahrişe ve kızarıklığa neden olabilir. C14H10O2’nin yutulması mide tahrişine ve sindirim sorunlarına neden olabilir. Çok miktarda yutulması halinde kusma, baş dönmesi ve bilinç kaybı gibi daha ciddi sağlık sorunlarına yol açabilir. C14H10O2 ile çalışırken koruyucu eldiven ve göz koruması kullanmak ve maruz kalmayı en aza indirmek için iyi havalandırılan bir alanda çalışmak önemlidir. C14H10O2 ile temas sonrasında olumsuz reaksiyonlar meydana gelirse derhal doktora başvurulması önerilir.
| Tehlike sembolleri | Yanıcı |
| Güvenlik Açıklaması | S24/25 – Cilt ve gözlerle temasından kaçının |
| BM kimlik numaraları | UN2024 – Tehlikeli mallar, tehlike sınıfı 3 |
| HS kodu | 2915.90.90 |
| Tehlike sınıfı | 3 – Yanıcı sıvılar |
| Paketleme grubu | III – Orta risk |
| Toksisite | Orta derecede toksik |
Benzil sentez yöntemleri
C14H10O2, aşağıdakiler de dahil olmak üzere çeşitli yöntemlerle sentezlenebilir:
- Difenilmetanolün oksidasyonu: Difenilmetanol, C14H10O2 oluşturmak üzere krom trioksit kullanılarak oksitlenir. C14H10O2 sentezinde basit ve uygun maliyetli olması nedeniyle yaygın olarak kullanılan bir yöntemdir.
- Wacker Oksidasyonu: Bu yöntem, alkeni C14H10O2’ye dönüştürmek için bir paladyum katalizörü ve bir hidroperoksit oksidanının kullanılmasını içerir. Reaksiyon genellikle etanol veya su gibi bir solventin varlığında gerçekleştirilir.
- Knoevenagel Yoğunlaşması: Bu yöntemde benzaldehit ile barbitürik asitin sodyum hidroksit veya potasyum hidroksit gibi kuvvetli bir baz varlığında reaksiyonuyla C14H10O2 sentezlenir.
- Ullmann reaksiyonu: Bu yöntem, iki aromatik bileşiğin bakır katalizli bir reaksiyon yoluyla birleştirilmesini içerir. C14H10O2 sentezinde iki benzaldehit molekülü reaksiyona girerek C14H10O2’yi oluşturur.
- Baeyer-Villiger Oksidasyonu: Bu yöntemde, C14H10O2, bir peroksiasit oksidan ve katalitik miktarda bir tersiyer amin varlığında sikloheksanonun C14H10O2’ye oksitlenmesiyle sentezlenir.
C14H10O2 sentez yönteminin seçimi, ham maddelerin mevcudiyeti, ürünün arzu edilen verimi ve saflığı ve sentez prosesinin maliyeti ve süresi gibi çeşitli faktörlere bağlıdır.
Benzilin kullanım alanları
C14H10O2, çeşitli alanlarda birçok kullanıma sahip çok yönlü bir kimyasaldır. C14H10O2’nin yaygın kullanımlarından bazıları şunlardır:
- İnce kimyasal üretiminde, antioksidanlar, alev geciktiriciler ve boyalar dahil olmak üzere çeşitli ince kimyasalların üretiminde hammadde olarak C14H10O2 kullanılır.
- Polimer sentezi, çeşitli endüstrilerde geniş bir uygulama yelpazesine sahip polikarbonatlar ve poliüretanlar dahil olmak üzere polimerlerin sentezinde C14H10O2’yi kullanır.
- Pestisitler, mahsulleri ve bahçe zararlılarını kontrol etmek için bazı pestisitlerin sentezinde C14H10O2’yi bir ara madde olarak kullanır.
- Kozmetikler, parfüm ve kolonya gibi bazı kozmetik ürünlerinde taze, çiçeksi bir aroma sağlamak için C14H10O2’yi koku olarak kullanır.
- Tat ve koku endüstrisi, gıda ve kozmetik ürünlerine odunsu ve çiçeksi bir aroma kazandırmak için tat ve koku bileşeni olarak C14H10O2’yi kullanır.
Sonuç olarak C14H10O2, ince kimya, ilaç ve kozmetik endüstrileri de dahil olmak üzere çeşitli endüstrilerde geniş bir kullanım alanına sahip çok yönlü bir kimyasaldır.
Sorular:
Benzil polar mıdır?
Evet, C14H10O2 polardır. Karbonil (-C=O) ve fenil (-C6H5) grupları gibi polar fonksiyonel grupların varlığı nedeniyle polar bir moleküler yapıya sahiptir. Bu polar yapı, C14H10O2’yi su ve alkol gibi polar solventlerde çözünür, ancak hidrokarbonlar gibi polar olmayan solventlerde çözünmez hale getirir. C14H10O2’nin polar yapısı aynı zamanda hidrojen bağları ve dipol-dipol etkileşimleri gibi çeşitli polar reaksiyonlara katılmasına da olanak tanır.
Benzilik asit oluşumu ne tür bir reaksiyonla gerçekleşir?
C14H10O2’den C14H10O2ik asit oluşumu, benzilik asit yeniden düzenlemesi olarak bilinen bir tür yeniden düzenleme reaksiyonudur. Bu reaksiyon, benzilik asitte yeni bir karboksilik asit fonksiyonel grubu oluşturmak için C14H10O2’deki karbonil grubunun yeniden düzenlenmesidir. Benzilik asit yeniden düzenlemesi, siklik ketonların amidlere veya karboksilik asitlere yeniden düzenlenmesini içeren bir tür nükleofilik ikame reaksiyonu olan Beckmann yeniden düzenlemesinin bir örneğidir. Reaksiyon mekanizması, siklik bir ara ürünün oluşumunu, ardından karbonil grubunun göçünü ve ayrılan grubun ortadan kaldırılmasını içerir.
