Bakır sülfat, CuSO4 formülüne sahip mavi kristalli bir katıdır. Tarımda, fungisit olarak, boya ve pigment üretiminde yaygın olarak kullanılır.
| IUPAC Adı | Bakır(II) sülfat |
| Moleküler formül | CuSO4 |
| CAS numarası | 7758-98-7 |
| Eş anlamlı | Mavi vitriol, bakır sülfat, bakır sülfat, sülfürik asidin bakır (2+) tuzu, bakır (II) sülfat, bakır vitriol, mavi taş |
| InChI | InChI=1S/Cu.H2O4S/c;1-5(2,3)4/h;(H2,1,2,3,4)/q+2;/p-2 |
Bakır Sülfatın Molar Kütlesi
Bakır sülfatın molar kütlesi susuz form (CuSO4) için 159.609 g/mol ve pentahidrat form (CuSO4·5H2O) için 249.685 g/mol’dür. Molar kütle, bir moleküldeki tüm atomların atomik kütlelerinin toplamıdır. Bakır sülfatın molar kütlesi, susuz formdaki bir bakır (Cu) atomu, bir kükürt (S) atomu ve dört oksijen (O) atomunun atomik kütlesinin eklenmesiyle veya susuz formun molar kütlesinin aşağıdaki formülle eklenmesiyle hesaplanır. pentahidrat formundaki beş su molekülünün (H2O) molar kütlesi.
Bakır sülfatın kaynama noktası
Bakır sülfatın belirli bir kaynama noktası yoktur çünkü kaynama noktasına ulaşmadan ayrışır. Bununla birlikte, bakır sülfatın pentahidrat formu ısıtıldığında su moleküllerini kaybeder, bu da yaklaşık 650°C’de ayrışan susuz bakır sülfatla sonuçlanır. Bakır sülfatın ayrışması endotermik bir süreçtir, yani ısıyı emer.
Bakır sülfatın erime noktası
Bakır sülfatın erime noktası pentahidrat formu için 110°C, susuz formu için ise 650°C’dir. Erime noktası, katı bir maddenin sıvı duruma geçtiği sıcaklıktır. Bakır sülfatın pentahidrat formu, bakır, kükürt ve oksijen atomları arasındaki iyonik bağları bozabilen su moleküllerinin varlığı nedeniyle susuz formdan daha düşük bir sıcaklıkta erir.
Bakır sülfatın yoğunluğu g/ml
Bakır sülfatın yoğunluğu susuz form için 3,6 g/mL, pentahidrat form için ise 2,284 g/mL’dir. Yoğunluk birim hacim başına kütlenin ölçüsüdür. Bakır sülfatın yoğunluğu, yapısındaki su moleküllerinin sayısından etkilenir çünkü pentahidrat formu, birim hacim başına susuz forma göre daha fazla su molekülü içerir.
Bakır sülfatın moleküler ağırlığı
Bakır sülfatın moleküler ağırlığı susuz form için 159.609 g/mol ve pentahidratlı form için 249.685 g/mol’dür. Molekül ağırlığı, bir moleküldeki tüm atomların atom ağırlıklarının toplamıdır. Bakır sülfatın moleküler ağırlığı, ihtiyaç duyulan veya üretilen bakır sülfat miktarını belirlemek için kimyasal reaksiyonlarda ve stokiyometri hesaplamalarında kullanılır.
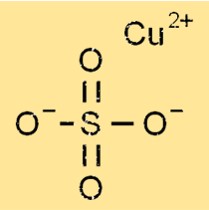
Bakır sülfatın yapısı
Bakır sülfat, bir bakır atomunun dört oksijen atomu ve iki kükürt atomu ile çevrelendiği, hem susuz hem de pentahidrat formlarında oktahedral bir yapıya sahiptir. Pentahidrat formunda, oktahedral yapıya beş su molekülü bağlanarak hidratlı bir kristal kafes oluşturulur. Bakır, kükürt, oksijen ve su molekülleri arasındaki iyonik bağlar bakır sülfatın kristal yapısını oluşturur.
Bakır sülfat formülü
Kuprik sülfatın formülü CuSO4’tür; bu, onun bir bakır (Cu) atomu, bir kükürt (S) atomu ve dört oksijen (O) atomundan oluştuğunu gösterir. Ayrıca yaygın olarak bakır (II) sülfat veya Mavi Vitriol olarak da bilinir. Formül, bir molekülde bulunan her bir elementin atom sayısını gösterir.
| Dış görünüş | Mavi kristal katı |
| Spesifik yer çekimi | 3,6 (susuz); |
| Renk | Mavi |
| Koku | Kokusuz |
| Molar kütle | 159,609 g/mol (susuz); |
| Yoğunluk | 3,6 g/mL (susuz); |
| Füzyon noktası | 110°C (pentahidrat); |
| Kaynama noktası | Kaynamadan önce parçalanır |
| Flaş noktası | Uygulanamaz |
| sudaki çözünürlük | 31,6g/100ml (20°C) |
| çözünürlük | Metanolde çözünür, gliserolde çözünür, etanolde az çözünür, eterde çözünmez |
| Buhar basıncı | Uygulanamaz |
| Buhar yoğunluğu | Uygulanamaz |
| pKa | 1.99 |
| pH | 3,5 – 4,5 |
Bakır sülfatın güvenliği ve tehlikeleri
Bakır sülfat, uygun şekilde kullanılmazsa sağlık riskleri oluşturabilir. Yutulması halinde zararlıdır ve cilt veya gözlerle teması halinde tahrişe veya yanıklara neden olabilir. Tozunun veya buharının solunması solunum yolu tahrişine veya hasara neden olabilir. Aynı zamanda çevre için potansiyel bir tehlikedir ve sudaki yaşam için toksik olabilir. Bakır sülfatla çalışırken koruyucu kıyafet, eldiven ve gözlük takmak gibi önlemler alınmalıdır. Yutulması halinde zehir kontrol merkezine başvurun veya derhal tıbbi yardım isteyin. Cilt veya gözlerle teması halinde birkaç dakika suyla yıkayın ve doktora başvurun.
| Tehlike sembolleri | Xi (Rahatsız edici) |
| Güvenlik Açıklaması | Cilt ve gözlerle temasından kaçının. Koruyucu eldiven ve göz/yüz koruması kullanın. Yutulması halinde doktora başvurunuz. |
| BİR tanımlayıcılar | UN3077 (susuz için); UN1512 (pentahidrat için) |
| HS kodu | 2833.25.00 |
| Tehlike sınıfı | 9 (Çeşitli tehlikeli mallar) |
| Paketleme grubu | III |
| Toksisite | Yutulması halinde zararlı olabilir, cilt ve göz tahrişine neden olur ve solunum yolu tahrişine neden olabilir. |
Bakır sülfat sentez yöntemleri
Bakır sülfatı sentezlemek için bakırın sülfürik asitle veya bakır oksit veya bakır hidroksitin sülfürik asitle reaksiyona sokulması gibi çeşitli yöntemler kullanılabilir.
Birinci yöntemi kullanarak bakır sülfatı sentezlemek için, sülfürik asit içeren bir reaksiyon kabına bakır eklenir ve reaksiyonu başlatmak için ısı uygulanır. Bakır, sülfürik asitle reaksiyona girerek bakır sülfat ve su üretir. Bundan sonra elde edilen karışım soğutulur ve bakır sülfat kristallerinin kalan çözeltiden ayrılması için süzülür.
Bakır sülfatı sentezlemek için bakır oksit veya bakır hidroksit, bir reaksiyon kabında sülfürik asitle reaksiyona sokulabilir. Reaksiyondan sonra karışım soğutulur ve kalan çözeltiden bakır sülfat kristalleri süzülür.
Başka bir yöntem, bakırın bir reaksiyon kabında kükürt dioksit ve oksijenle reaksiyona sokulmasını içerir. Reaksiyon bakır sülfat ve su üretir. Ortaya çıkan karışım soğutulur ve bakır sülfat kristallerini elde etmek için süzülür.
Bakır sülfat üretmek için elektroliz yöntemi kullanılabilir. Bu işlemde, sulu bir bakır sülfat çözeltisi elektrolize tabi tutulur ve bu da anot üzerinde bakır sülfatın birikmesine neden olur. Daha sonra bakır sülfat kristalleri çözeltiden ayrılarak kurutulur.
Bakır sülfatın kullanım alanları
Bakır sülfatın yaygın kullanımlarından bazıları şunlardır:
- Bitki büyümesi için gerekli olan bakırın toprağa sağlanması için gübre olarak kullanılır. Bitkilerdeki mantar hastalıklarını kontrol etmek için pestisit olarak kullanılır.
- Hayvanların büyümesi ve gelişmesi için gerekli olan bakır kaynağı olarak hayvan yemlerine eklenir.
Endüstri
- Elektrokaplamada diğer metallerin yüzeyine bakır biriktirmek için kullanılır, bu da onların korozyon direncini artırır.
- Su arıtımında yosun ve diğer yabancı maddeleri sudan uzaklaştırmak için yosun öldürücü ve topaklaştırıcı olarak kullanılır.
- Analitik kimyada indirgeyici şekerlerin ve proteinlerin belirlenmesinde reaktif olarak kullanılır.
- Tekstil sektöründe boyaları kumaşlara sabitlemek ve onlara daha canlı bir renk kazandırmak amacıyla mordan olarak kullanılır.
- İlaç endüstrisinde besin takviyeleri ve ilaçlar için bakır kaynağı olarak kullanılır.
- Ayrıca pigment, mürekkep ve boya üretiminin yanı sıra pil, katalizör ve ahşap koruyucuların üretiminde de kullanılır.
Sorular:
Soru: Bakır sülfat suda çözünür mü?
C: Evet, bakır sülfat suda oldukça çözünür. Oda sıcaklığında 100 mililitre suda maksimum 203 grama kadar çözünebilir.
S: Yakınımdaki bakır sülfat nereden satın alınır?
C: Bakır sülfat çoğu hırdavatçıdan, bahçe merkezinden ve çevrimiçi perakendecilerden satın alınabilir. Bakır sülfat tarımda ve hayvan yeminde yaygın olarak kullanıldığından, yerel çiftlik tedarik mağazanıza veya yem mağazanıza da danışabilirsiniz.
S: Bir galon su başına ne kadar bakır sülfat?
C: Bir galon su başına ihtiyaç duyulan bakır sülfat miktarı, spesifik uygulamaya bağlıdır. Örneğin tarımda önerilen uygulama oranı genellikle dönüm başına 1 ila 10 pound arasındadır. Su arıtımında önerilen doz genellikle litre su başına 0,2 ila 1,0 miligram arasındadır. Doğru kullanımı sağlamak için bakır sülfat ürün etiketi üzerindeki talimatların dikkatle takip edilmesi önemlidir.
S: Bakır(ii) sülfatın formülü nedir?
C: Bakır(II) sülfatın formülü CuSO4’tür.
