Dekan (C10H22), düz bir zincir halinde düzenlenmiş on karbon atomu içeren bir hidrokarbon bileşiğidir. Temizleme ve üretim işlemleri gibi çeşitli endüstriyel uygulamalarda yaygın olarak solvent olarak kullanılır.
| IUPAC Adı | Dekan |
| Moleküler formül | C10H22 |
| CAS numarası | 124-18-5 |
| Eş anlamlı | n-Dekan, Desil hidrit, n-Amilmetin, Kapdekan |
| InChI | InChI=1S/C10H22/c1-3-5-7-9-10-8-6-4-2/h3-10H2,1-2H3 |
Dekanın özellikleri
Dekan formülü
Dekanın formülü C10H22’dir. On karbon atomu ve yirmi iki hidrojen atomundan oluşan bir hidrokarbon bileşiğini temsil eder. Formül, bir dekan molekülünde bulunan atomların tam sayısını ve türünü gösterir.
Dekanın Molar Kütlesi
Desil hidrürün molar kütlesi, onu oluşturan elementlerin atomik kütleleri toplanarak hesaplanabilir. Karbonun (C) molar kütlesi 12,01 g/mol ve hidrojenin (H) molar kütlesi 1,008 g/mol’dür. Bu nedenle desil hidrürün molar kütlesi yaklaşık 142,28 g/mol’dür.
Dekanın kaynama noktası
Dekanın kaynama noktası yaklaşık 174°C’dir (345°F). Bu, normal atmosferik basınçta desil hidrürün o sıcaklıkta buharlaşmaya ve gaz haline dönüşmeye başladığı anlamına gelir. Kaynama noktası desil hidrürün önemli bir özelliğidir ve fiziksel özelliklerini ve uygulamalarını belirlemek için kullanılır.
Dekan Erime Noktası
Desil hidrürün erime noktası yaklaşık -29°C’dir (-20°F). Bu, desil hidrürün katı halinden sıvı durumuna geçtiği sıcaklık anlamına gelir. Bu düşük erime noktası, desil hidrürün normal koşullar altında kolayca sıvılaştırılabilir olmasını sağlar.
Dekanın yoğunluğu g/mL
Desil hidrürün yoğunluğu yaklaşık 0,73 g/mL’dir. Yoğunluk birim hacim başına kütlenin ölçüsüdür. Desil hidrürün yoğunluğu, eşit hacimdeki suya kıyasla göreceli ağırlığını veya hafifliğini gösterir. Desil hidritin düşük yoğunluğu, sudan daha hafif olduğunu göstermektedir.
Dekan Molekül Ağırlığı
Desil hidrürün moleküler ağırlığı yaklaşık 142,28 g/mol’dür. Bir desil hidrit molekülündeki tüm atomların atom ağırlıklarının eklenmesiyle hesaplanır. Molekül ağırlığı, desil hidrit molekülünün boyutu ve kütlesi hakkında değerli bilgiler sağlar.
Dekanın yapısı
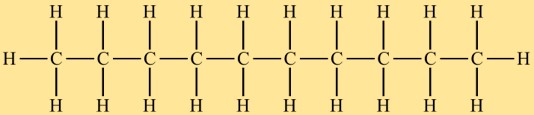
Desil hidrit, on karbon atomunun doğrusal bir düzenlemeyle birbirine bağlandığı düz bir zincir yapısına sahiptir. Her karbon atomu, çevresindeki hidrojen atomlarıyla dört tek kovalent bağ oluşturur. Desil hidrürün karbon zinciri dallanmamıştır ve bu yapısal özellik onun kimyasal ve fiziksel özelliklerini etkiler.
Dekanın çözünürlüğü
Desil hidrit suda çözünmez ancak benzen, eter ve heksan gibi polar olmayan çözücülerde çözünür. Polar olmayan doğası, su gibi polar maddelerle etkileşimini engeller. Desil hidrit çözünürlüğü, çeşitli endüstriyel işlemlerde ve uygulamalarda, özellikle de polar olmayan solventlerle uğraşırken önemli bir husustur.
| Dış görünüş | Renksiz sıvı |
| Spesifik yer çekimi | 0,73 |
| Renk | Renksiz |
| Koku | Kokusuz |
| Molar kütle | 142,28 gr/mol |
| Yoğunluk | 0,73 gr/ml |
| Füzyon noktası | -29°C (-20°F) |
| Kaynama noktası | 174°C (345°F) |
| Flaş noktası | 43°C (109°F) |
| sudaki çözünürlük | Çözünmez |
| çözünürlük | Benzen, eter ve heksan gibi polar olmayan solventlerde çözünür |
| Buhar basıncı | 20°C’de 1,22 mmHg |
| Buhar yoğunluğu | 4,88 (hava = 1) |
| pKa | Uygulanamaz |
| pH | Doğal |
Decane’nin güvenliği ve tehlikeleri
Desil hidrürün belirli güvenlik hususları ve tehlikeleri vardır. Yanıcıdır ve açık alev veya kıvılcımlara maruz kaldığında tutuşabileceği için dikkatli kullanılmalıdır. Desil hidrit buharı havadan ağırdır, bu da zemin boyunca ilerleyebileceği ve alçak alanlarda birikerek potansiyel bir yangın veya patlama tehlikesi oluşturabileceği anlamına gelir. Desil hidrit ile doğrudan temas ciltte tahrişe neden olabilir ve ayrıca göz tahrişine de neden olabilir. Desil hidrit ile çalışırken eldiven ve gözlük gibi uygun koruyucu önlemlerin kullanılması önemlidir. Kapalı alanlarda desil hidrit buharlarının konsantrasyonunu en aza indirmek için yeterli havalandırma çok önemlidir.
| Tehlike sembolleri | Yanıcı |
| Güvenlik Açıklaması | – Açık alevlerden uzak tutun, – İyi havalandırılmış alanlarda kullanın – Eldiven ve koruyucu gözlük kullanın, – Cilt ve gözlerle doğrudan temasından kaçının. |
| Birleşmiş Milletler tanımlayıcıları | BM 2247 |
| HS kodu | 2901.10.00 |
| Tehlike sınıfı | Sınıf 3 (Yanıcı sıvı) |
| Paketleme grubu | GE II |
| Toksisite | Düşük toksisite |
Dekan sentezi yöntemleri
Desil hidrürün sentezlenmesi için çeşitli yöntemler vardır.
- Desil hidrürün sentezlenmesi için yaygın bir yöntem, paladyum veya nikel gibi uygun bir katalizörün varlığında desenin hidrojen gazı ile reaksiyona sokulmasıdır. Bu işlem, dekenenin karbon-karbon çift bağlarını doyurarak onu desil hidrite dönüştürür.
- Diğer bir yöntem, genellikle geçiş metali kompleksleri olan katalizörlerin, desil hidrit de dahil olmak üzere daha yüksek molekül ağırlıklı hidrokarbonlar oluşturmak için etilen moleküllerini birleştirdiği etilen oligomerizasyonudur.
- Petrol rafine etme işlemleri aynı zamanda desil hidrit de üretir. Bu işlemde, ham petrolün damıtılması, saf desil hidrit elde etmek için desil hidrit ve benzer hidrokarbonları içeren bir fraksiyonu ayırır ve saflaştırır.
- Fischer-Tropsch işlemi, yüksek sıcaklık ve basınç koşulları altında, genellikle bir demir veya kobalt katalizörü olan bir katalizör üzerinde karbon monoksit ve hidrojenin reaksiyona sokulmasıyla desil hidritin sentezine izin verir. Bu işlem, desil hidrit de dahil olmak üzere bir hidrokarbon karışımıyla sonuçlanır.
Bu endüstriyel ölçekli sentez yöntemlerinin özel ekipman ve uzmanlık gerektirdiğini vurgulamak çok önemlidir. Sentez yönteminin seçimi, ham maddelerin mevcudiyeti, istenen saflık ve ekonomik hususlar gibi faktörlere bağlıdır.
Dekanın kullanım alanları
Desil hidrit, özellikleri ve karakteristikleri nedeniyle farklı endüstrilerde çeşitli uygulamalar bulur. Desil hidrürün bazı yaygın kullanımları şunlardır:
- Çözücü: Desil hidrit, temizleme ve yağ giderme uygulamaları gibi endüstriyel işlemlerde çözücü olarak kullanılır. Çeşitli polar olmayan maddeleri çözme yeteneği onu bu işlemlerde faydalı kılar.
- Yakıt: Dizel yakıt, bir bileşen olarak desil hidrit içerir ve bunu, dizel yakıtların ateşleme kalitesini değerlendiren setan indeksini ölçmek için referans bileşik olarak kullanır. Dizel yakıtın yanma özelliklerine katkıda bulunur.
- Kimyasal ara madde: Desil hidrit, diğer kimyasalların üretimi için bir yapı taşı görevi görür. Desil hidrit, yüzey aktif maddeler, yağlayıcılar ve polimerler dahil olmak üzere çeşitli bileşiklerin sentezi için bir hammadde görevi görür.
- Ekstraktant: İlaç ve gıda endüstrileri ekstraktant olarak desil hidriti kullanır. Bazı bileşiklerin ve aromaların ham maddelerden ayrılmasına ve saflaştırılmasına yardımcı olur.
- Araştırma ve Laboratuvar Uygulamaları: Bilimsel araştırma ve laboratuvarlarda desil hidrit kullanılmaktadır. Gaz kromatografisinde referans bileşik olarak ve kalibrasyon amacıyla standart olarak hizmet eder.
- Kozmetik formülasyonlar: Kozmetik ve kişisel bakım ürünleri, formülasyonlarına desil hidrit katar. Çeşitli cilt ve saç bakım ürünlerinde yumuşatıcı, yumuşatıcı ve viskozite düzenleyici olarak görev yapar.
- Endüstriyel yağlayıcılar: Endüstriyel uygulamalar, desil hidrürün düşük uçuculuğu ve iyi yağlayıcılığından, onu yağlayıcı olarak kullanarak yararlanır. Hareketli parçalar arasındaki sürtünmeyi ve aşınmayı azaltır.
- Kalibrasyon Standartları: Analitik kimya, kalibrasyon standardı olarak desil hidrit kullanır. Analitik cihaz ve tekniklerin kalibrasyonuna ve validasyonuna yardımcı olur.
Genel olarak desil hidrürün çok yönlü özellikleri, onu üretimden araştırma ve geliştirmeye kadar çeşitli endüstrilerde değerli kılmaktadır.
Sorular:
S: Dekan nedir?
A: Desil hidrit, on karbon atomu ve yirmi iki hidrojen atomundan oluşan, C10H22 moleküler formülüne sahip bir hidrokarbondur.
S: 1-desinin dekana indirgenmesi için kaç eşdeğer hidrojen gazı gerekir?
C: 1-desinin desil hidrüre indirgenmesi için iki eşdeğer hidrojen gazı gerekir.
S: Dekan polar mıdır?
C: Hayır, desil hidrit polar değildir çünkü polar olmayan kovalent bağlarla bağlanan karbon ve hidrojen atomlarından oluşur.
S: İyot C10H22’de çözünür mü?
C: Evet, iyot C10H22’de (desil hidrit) çözünür çünkü iki madde polar değildir ve karışabilir.
Soru: Aşağıdaki maddelerden hangisinin viskozitesi en yüksektir? (a) C4H10 (b) C8H18 (c) C10H22
C: C10H22 (desil hidrit), daha büyük moleküler boyutu ve daha uzun karbon zinciri nedeniyle verilen maddeler arasında en yüksek viskoziteye sahip olacaktır.
Soru: 53,0 g CHCl3 içindeki 23,0 g dekanın (C10H22) donma noktasını hesaplayın.
C: Donma noktasının hesaplanması, çözücünün donma noktası alçalması sabiti (CHCl3) ve donma noktası alçalmasını belirlemek için bileşenlerin mol kesirleri gibi ek bilgiler gerektirir.
