Oktan, yanmalı motorlarda kullanılan yüksek oktanlı bir yakıttır. Motor performansını artırır, vuruntuyu azaltır ve güç çıkışını artırır. Yüksek performanslı araçlarda ve yarış arabalarında yaygın olarak kullanılır.
| IUPAC Adı | Oktan |
| Moleküler formül | C8H18 |
| CAS numarası | 111-65-9 |
| Eş anlamlı | n-Oktan, Normal Oktan, Oktan |
| InChI | InChI=1S/C8H18/c1-3-5-7-8-6-4-2/h3-8H2.1-2H3 |
Oktan özellikleri
Oktan Formülü
Oktanın formülü C8H18’dir. Sekiz karbon atomu ve on sekiz hidrojen atomundan oluşur. Bu moleküler formül, tek bir oktan molekülündeki atomların dizilişini temsil eder.
Oktan Molar Kütlesi
Oktanın molar kütlesi, kimyasal formülündeki tüm atomların atomik kütlelerinin eklenmesiyle hesaplanır. Oktanın molar kütlesi mol başına yaklaşık 114,22 gramdır. Bu, belirli bir numunedeki oktan miktarını içeren çeşitli hesaplamalarda önemlidir.
Oktan sayısının kaynama noktası
Octan’ın kaynama noktası yaklaşık 125,5 santigrat derece (257,9 derece Fahrenheit) civarındadır. Bu, oktanın sıvı fazdan gaz fazına geçtiği sıcaklıktır. Oktanın kaynama noktası moleküler yapısından ve moleküller arası kuvvetlerden etkilenir.
Oktan erime noktası
Octan’ın erime noktası yaklaşık -57 santigrat derece (-70,6 derece Fahrenheit) civarındadır. Bu, oktanın katıdan sıvıya değiştiği sıcaklıktır. Oktanın erime noktası moleküler yapı ve moleküller arası kuvvetler gibi faktörlere bağlıdır.
Oktan yoğunluğu g/mL
Oktanın yoğunluğu mililitre başına yaklaşık 0,703 gramdır (g/mL). Yoğunluk, bir maddenin birim hacmi başına kütlenin bir ölçüsüdür. Oktanın yoğunluğu, yoğunluğu 1 g/mL olan suyunkinden daha düşüktür, bu da oktanın sudan daha az yoğun olduğunu gösterir.
Oktan Molekül Ağırlığı
Oktanın moleküler ağırlığı mol başına yaklaşık 114.22 gramdır. Bir oktan molekülündeki tüm atomların atom ağırlıklarının toplamıdır. Molekül ağırlığı, bir reaksiyonda ihtiyaç duyulan oktan miktarının belirlenmesi gibi çeşitli hesaplamalarda çok önemlidir.
Oktan yapısı
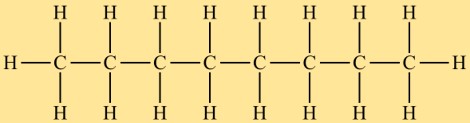
Oktan alkan sınıfına aittir ve doğrusal bir yapıya sahiptir. Onlara hidrojen atomlarının bağlı olduğu sekiz karbon atomundan oluşan bir zincirden oluşur. Oktandaki atomların düzeni, dallanmış veya döngüsel bir yapı olmayacak şekildedir.
Oktan sayısı çözünürlüğü
Oktan suda çözünmez olarak kabul edilir. Polar olmayan yapısından dolayı polar çözücülerde düşük çözünürlük gösterir. Bununla birlikte oktan, diğer hidrokarbonlar, yağlar ve organik çözücüler gibi polar olmayan çözücülerde oldukça çözünür.
| Dış görünüş | Renksiz sıvı |
| Spesifik yer çekimi | 0,703g/ml |
| Renk | Renksiz |
| Koku | Kokusuz |
| Molar kütle | 114,22 gr/mol |
| Yoğunluk | 0,703g/ml |
| Füzyon noktası | -57°C (-70,6°F) |
| Kaynama noktası | 125,5°C (257,9°F) |
| Flaş noktası | -18°C (0°F) |
| sudaki çözünürlük | Çözünmez |
| çözünürlük | Polar olmayan solventlerde çözünür |
| Buhar basıncı | 20°C’de 12,9 mmHg |
| Buhar yoğunluğu | 3,47 (hava = 1) |
| pKa | ~45 |
| pH | Doğal |
Oktan Güvenliği ve Tehlikeleri
Octan, dikkate alınması gereken bazı güvenlik riskleri taşır. Oldukça yanıcıdır ve kolayca tutuşarak yangın tehlikesi oluşturabilir. Oktan buharları havayla patlayıcı karışımlar oluşturarak yangın ve patlama riskini artırabilir. Oktanı dikkatli bir şekilde kullanmak, yeterli havalandırmayı sağlamak ve tutuşma kaynaklarından kaçınmak önemlidir. Oktanın ciltle teması tahrişe ve kuruluğa neden olabilir. Oktanın yutulması veya solunması, solunum tahrişi ve merkezi sinir sistemi etkileri dahil olmak üzere sağlık risklerine neden olabilir. Güvenlik önlemlerine uymak, uygun kişisel koruyucu ekipman kullanmak ve oktanı uyumsuz maddelerden uzak tutmak önemlidir.
| Tehlike sembolleri | Yanıcı (F), Tahriş Edici (Xi) |
| Güvenlik Açıklaması | Isıdan/kıvılcımdan/açık alevden uzak tutun. İyi havalandırılan bir ortamda kullanınız. Cilt ve gözlerle temasından kaçının. |
| BM kimlik numaraları | BM 1262 |
| HS kodu | 2901.10.10 |
| Tehlike sınıfı | 3 – Yanıcı sıvılar |
| Paketleme grubu | III |
| Toksisite | Zayıf |
Oktan sentezi yöntemleri
Oktanı çeşitli yöntemler sentezleyebilir. Yaygın bir yöntem, nafta gibi petrol fraksiyonlarını katalitik olarak yeniden düzenlemektir. İşlem, naftayı ısıtır ve onu genellikle platin veya renyum gibi bir katalizörden geçirerek hidrokarbon moleküllerinin yeniden düzenlenmesini sağlar. Bu yeniden düzenleme, özellikle oktan olmak üzere daha yüksek oktanlı bileşikler üretir.
Başka bir yöntem izobütanın bütenlerle alkile edilmesidir. Asit katalizörleri olarak görev yapan sülfürik asit veya hidroflorik asit , dallanmış bir hidrokarbon olan izobütanın doymamış hidrokarbonlarla (bütenler) reaksiyonunu kolaylaştırır. Bu reaksiyon dallanmış zincirli oktan moleküllerini oluşturur.
İzomerizasyon, oktan üretmek için ek bir yaklaşımdır. Heksan veya heptan gibi düz zincirli hidrokarbonları dallı zincirli izomerlere dönüştürür. Zeolitler veya platin katalizörleri dahil olmak üzere çeşitli katalizörler bu işlemi katalize edebilir.
Ayrıca oktan, tolüen veya ksilen gibi aromatik hidrokarbonların hidrojen gazı ve uygun bir katalizör kullanılarak hidrojenlenmesiyle de elde edilebilir. Bu reaksiyon, aromatik bileşikleri, oktan üretmek üzere daha da hidrojeni giderilebilen sikloheksana dönüştürür.
Bu sentez yöntemleri, benzinde yakıt bileşeni olarak yaygın olarak kullanılan oktan üretiminde önemli rol oynamaktadır. Bu teknikleri kullanarak istenilen oktan sayısına sahip bir oktan elde edilebilmekte, yanmalı motorlarda optimum performans ve verimlilik sağlanmaktadır.
Oktanın kullanım alanları
Octan, faydalı özellikleri nedeniyle farklı endüstrilerde çeşitli kullanım alanları bulmaktadır. Oktan’ın bazı önemli uygulamaları şunlardır:
- Yakıt: Oktan öncelikle benzinde yakıt bileşeni olarak kullanılır. Yakıtın oktan sayısını artırarak motor performansını artırır, vuruntuyu azaltır ve motor hasarını önler. Bu özellikle yüksek performanslı araçlarda ve yarış arabalarında önemlidir.
- Yanmalı Motorlar: Oktan, otomobiller, motosikletler ve küçük motorlar da dahil olmak üzere içten yanmalı motorlar için çok önemlidir. Araç ve makinelerin çalışması ve tahriki için gerekli enerji kaynağını sağlar.
- Kimyasal Sentez: Oktan, çeşitli kimyasalların üretiminde öncü görevi görür. Alkoller, aldehitler ve asitler gibi diğer hidrokarbon bileşiklerinin sentezi için hammadde olarak kullanılır.
- Laboratuvar Çözücüsü: Oktan, laboratuvarlarda polar olmayan bir çözücü olarak kullanılır. Düşük polaritesi, onu polar olmayan bileşiklerin çözülmesi için uygun hale getirerek araştırmacıların belirli deneyler ve ekstraksiyonlar yapmasına olanak tanır.
- Standart Referans: Oktan sayılarını belirlemek ve farklı yakıtların performansını karşılaştırmak için araştırmacılar ve uzmanlar oktanı aktif olarak referans ve referans bileşiği olarak kullanır. Benzin ve diğer hidrokarbon yakıtların kalitesi ve verimliliğine ilişkin standartların belirlenmesine yardımcı olur.
- Kalibrasyon: Oktan, doğru ve hassas ölçümler sağlamak için gaz kromatografları gibi ekipmanların kalibrasyonunda kullanılır. Bilinen özellikleri ve iyi karakterize edilmiş davranışı onu güvenilir bir kalibrasyon standardı haline getirir.
- Araştırma ve Geliştirme: Oktan, otomotiv ve yakıt endüstrilerinde araştırma ve geliştirme amacıyla gereklidir. Bilim adamları ve mühendisler, yakıt verimliliğini artırmak, emisyonları azaltmak ve alternatif yakıtlarda yenilik yapmak için oktanın özelliklerini, yanma özelliklerini ve çevresel etkilerini aktif olarak inceliyorlar.
Octan, ulaşıma aktif olarak güç sağlıyor, kimyasal sentezi mümkün kılıyor, laboratuvar çalışmalarını kolaylaştırıyor ve otomotiv ve enerji endüstrilerindeki ilerlemelere yön veriyor.
Sorular:
Soru: Hangi bileşiğin erime noktası en yüksektir?
C: Al2(CO3)3.
S: Bu C8H18(g) izomerinin standart oluşum entalpisi nedir?
C: C8H18(g) izomerinin standart oluşum toplu ısısı, söz konusu izomere özeldir ve değerin belirlenmesi için tanımlanmasını gerektirir.
S: 5,90 mol C8H18’in gram cinsinden kütlesi nedir?
C: 5,90 mol C8H18’in kütlesi yaklaşık 789,26 gramdır.
S: Hangi ifade bütanın (C4H10) erime noktasını oktanın (C8H18) erime noktasıyla en iyi karşılaştırır?
C: Oktan (C8H18), bütandan (C4H10) daha yüksek bir erime noktasına sahiptir.
S: C8H18’in adı nedir?
C: C8H18’in adı oktandır.
S: Oktan nedir?
A: Oktan, C8H18 moleküler formülüne sahip bir alkan hidrokarbondur. Genellikle benzinde yanıcı bir bileşen olarak kullanılır.
Soru: Benzinin oktan sayısı nedir?
C: Benzinin oktan sayısı, yanma sırasında vuruntuya karşı direnç gösterme yeteneğini ifade eder. Yakıtın vuruntu önleyici özelliklerini ve yüksek sıkıştırmalı motorlara uygunluğunu gösterir.
S: Oktan sayısı ve setan sayısı nedir?
C: Oktan sayısı benzinin vuruntu önleyici özelliklerini ölçerken, setan sayısı dizel yakıtın tutuşma kalitesini ölçer.
S: Oktan nedir?
C: Oktan sayısı, yakıtın yanma sırasında vuruntuya karşı direnç gösterme performansını temsil eden sayısal bir değerdir. Yakıtın tutuşmadan önce sıkıştırmaya direnme yeteneğini gösterir.
S: Hidrokarbon CH3(CH2)6CH3’ün adı nedir?
C: CH3(CH2)6CH3 hidrokarbonunun adı oktandır.
