Magnezyum asetat (Mg(C2H3O2)2), Mg2+ ve C2H3O2- iyonlarından oluşan bir bileşiktir. Organik sentezlerde kurutma maddesi ve gıda katkı maddesi olarak yaygın olarak kullanılır.
| IUPAC Adı | Magnezyum asetat |
| Moleküler formül | Mg(C2H3O2)2 |
| CAS numarası | 142-72-3 |
| Eş anlamlı | Magnezyum Diasetat, Asetik Asitin Magnezyum Tuzu, Magnezyum Etanoat, CAS 73567-85-6, EINECS 240-882-6, UNII-RS92S4G29A |
| InChI | InChI=1S/2C2H4O2.Mg/c2 1-2(3)4;/h2 1H3,(H,3,4);/q;;+2/p-2 |
Magnezyum asetatın özellikleri
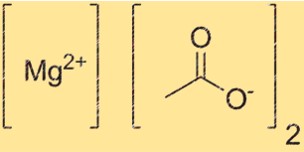
Magnezyum Asetat Formülü
Magnezyum asetatın kimyasal formülü Mg(C2H3O2)2’dir. Bu formül bileşiğin bir Mg2+ iyonu ve iki C2H3O2- iyonundan oluşan bileşimini temsil eder. Formül, belirli bir reaksiyon için gereken bileşik miktarının belirlenmesinde önemlidir. Ayrıca bileşiğin farklı bağlamlarda tanımlanması için de faydalıdır.
Magnezyum Asetat Molar Kütlesi
Mg(C2H3O2)2’nin molar kütlesi 142,39 g/mol’dür. Bu değer Mg2+ (24,31 g/mol) ve C2H3O2- (58,08 g/mol) iyonlarının atomik kütlelerinin eklenmesiyle elde edilir. Molar kütle, belirli bir reaksiyon için gereken Mg(C2H3O2)2 miktarının belirlenmesinde önemli bir özelliktir.
Magnezyum asetatın kaynama noktası
Mg(C2H3O2)2, 117,5°C (243,5°F) gibi nispeten yüksek bir kaynama noktasına sahiptir. Bu özellik, bileşiğin iyonik doğasından ve magnezyum ile asetat iyonları arasındaki güçlü elektrostatik çekimden kaynaklanmaktadır. Bu sıcaklıkta bileşik buharlaşmaya başlayacak, ancak daha yüksek sıcaklıklara maruz kalmadıkça sıvı halde kalacaktır.
Magnezyum asetat Erime noktası
Mg(C2H3O2)2’nin erime noktası 160°C’dir (320°F). Bu değer, bileşiğin katıdan sıvıya dönüşene kadar ısıtılmasıyla elde edilir. Erime noktası, bileşiğin katı halden sıvı duruma geçeceği sıcaklığı belirleyen önemli bir özelliktir. Bu özellik bileşiğin uygun şekilde işlenmesi ve depolanması için gereklidir.
Magnezyum asetatın yoğunluğu g/mL
Mg(C2H3O2)2’nin yoğunluğu 1,45 g/mL’dir. Bu değer bileşiğin kütlesinin hacmine bölünmesiyle elde edilir. Yoğunluk, bileşiğin belirli bir hacminin kütlesini belirleyen önemli bir özelliktir. Safsızlıklar yoğunluğu etkileyebileceğinden bileşiğin saflığını belirlemek için de yararlı bir özelliktir.
Magnezyum Asetat Molekül Ağırlığı
Mg(C2H3O2)2’nin moleküler ağırlığı 142,39 g/mol’dür. Bu değer, magnezyumun atomik kütleleri ve iki asetat iyonunun eklenmesiyle elde edilir. Molekül ağırlığı, belirli bir reaksiyon için gerekli olan bileşiğin miktarını belirleyen önemli bir özelliktir. Ayrıca bileşiğin saflığının belirlenmesinde de faydalıdır.
Magnezyum asetatın yapısı
Mg(C2H3O2)2, Mg2+ katyonlarının iki C2H3O2 anyonuyla çevrelendiği iyonik bir yapıya sahiptir. Mg2+ katyonunun yükü +2, C2H3O2- anyonu ise -1 yüküne sahiptir. Yapı, zıt yüklü iyonlar arasındaki elektrostatik çekimle bir arada tutulur.
| Dış görünüş | Beyaz kristal katı |
| Spesifik yer çekimi | 1,45 gr/ml |
| Renk | Beyaz |
| Koku | Kokusuz |
| Molar kütle | 142,39 gr/mol |
| Yoğunluk | 1,45 gr/ml |
| Füzyon noktası | 160°C (320°F) |
| Kaynama noktası | 117,5°C (243,5°F) |
| Flaş noktası | Uygulanamaz |
| sudaki çözünürlük | Çok çözünür |
| çözünürlük | Etanol, metanol, asetonda çözünür |
| Buhar basıncı | Müsait değil |
| Buhar yoğunluğu | Müsait değil |
| pKa | 4.76 |
| pH | 7,5 – 9,0 |
Magnezyum Asetatın Güvenliği ve Tehlikeleri
Mg(C2H3O2)2’nin amaçlanan uygulamalarda kullanımı genellikle güvenli kabul edilir, ancak herhangi bir kimyasal bileşikte olduğu gibi dikkat edilmesi gereken bazı potansiyel tehlikeler vardır. Solunması veya yutulması halinde cildi, gözleri ve solunum sistemini tahriş edebilir. Uzun süreli veya tekrarlanan maruz kalma sağlık üzerinde daha ciddi etkilere neden olabilir. Mg(C2H3O2)2 dikkatle kullanılmalı ve bu bileşik kullanılırken uygun koruyucu önlemler alınmalıdır. Kazara maruz kalmayı veya çevreye zarar vermeyi önlemek için uygun depolama ve imha protokollerinin takip edilmesi de önemlidir.
| Tehlike sembolleri | Hiçbiri |
| Güvenlik Açıklaması | S22 – Tozu solumayın; S24/25 – Cilt ve gözlerle temasından kaçının; S36/37/39 – Uygun koruyucu kıyafet, eldiven ve göz/yüz koruması kullanın; S45 – Kaza halinde veya kendinizi iyi hissetmiyorsanız derhal doktora başvurun (mümkünse doktora etiketi gösterin) |
| BM kimlik numaraları | Uygulanamaz |
| HS kodu | 29152900 |
| Tehlike sınıfı | Tehlikeli olarak sınıflandırılmadı |
| Paketleme grubu | Uygulanamaz |
| Toksisite | Düşük toksisite, ancak uygun şekilde kullanılmazsa cildi, gözleri ve solunum sistemini tahriş edebilir |
Magnezyum asetat sentez yöntemleri
Magnezyum oksit veya magnezyum hidroksitin asetik asitle reaksiyona sokulması da dahil olmak üzere çeşitli yöntemler kullanarak Mg(C2H3O2)2 sentezleyin.
Yaygın bir yöntemde, Mg(C2H3O2)2 ve su oluşturmak için bir asetik asit çözeltisine magnezyum oksit eklenir. Ortaya çıkan çözeltiyi süzün ve katı bir Mg(C2H3O2)2 ürünü elde etmek için buharlaştırın.
Başka bir yöntem, magnezyum metalinin, bakır klorür veya bakır sülfat gibi bir katalizör varlığında asetik asitle reaksiyonunu içerir. Reaksiyon, yan ürün olarak Mg(C2H3O2)2, hidrojen gazı ve metalik bakır üretir.
Mg(C2H3O2)2 ve sodyum klorür üretmek için magnezyum klorürü su varlığında sodyum asetatla reaksiyona sokarak bir metatez reaksiyonu yoluyla Mg(C2H3O2)2 sentezleyin.
Genel olarak sentez yönteminin seçimi, Mg(C2H3O2)2 ürününün istenen saflığı, ham maddelerin mevcudiyeti ve üretim sürecinin ölçeği gibi faktörlere bağlıdır.
Magnezyum Asetatın Kullanım Alanları
Mg(C2H3O2)2 benzersiz özelliklerinden dolayı çeşitli endüstrilerde geniş bir uygulama alanına sahiptir. Mg(C2H3O2)2’nin bazı yaygın kullanımları şunlardır:
- Gıda katkı maddeleri: Gıdaların besin değerini arttırmak ve bozulmalarını önlemek amacıyla gıda katkı maddesi olarak kullanılır.
- Tıp: Birçok fizyolojik süreçte önemli bir rol oynayan önemli bir mineral olan magnezyum kaynağı olarak tıbbi olarak kullanılır.
- Tekstil: Tekstil endüstrisinde mordan olarak kullanılan, boyaların kumaşlara sabitlenmesine yardımcı olan bir madde.
- Su Arıtma: Su arıtma uygulamalarında sudaki yabancı maddeleri uzaklaştırmak ve borularda ve ekipmanlarda kireç oluşumunu önlemek için kullanılır.
- Beton: Betonun mukavemetini ve dayanıklılığını arttırmak için üretiminde kullanılır.
- Kimyasal sentez: İlaçlar, aromalar ve parfümler gibi diğer kimyasal bileşiklerin sentezi için hammadde olarak kullanılır.
Sorular:
S: Asetik asit ve magnezyum karbonat reaksiyona girdiğinde ne oluşur?
C: Asetik asit ile magnezyum karbonat reaksiyona girdiğinde Mg(C2H3O2)2, karbondioksit ve su oluşur.
S: Kalsiyum magnezyum asetat nereden satın alınır?
C: Kalsiyum Mg(C2H3O2)2 çeşitli kimyasal tedarikçilerinden ve çevrimiçi pazarlardan satın alınabilir.
S: Magnezyum asetat suda çözünür mü?
C: Evet, Mg(C2H3O2)2 suda çözünür, çözünürlüğü oda sıcaklığında yaklaşık 54 g/L’dir.
S: 0,800 mol magnezyum asetat içeren 5,00 L’lik bir çözeltinin molar konsantrasyonu nedir?
A: 0,800 mol Mg(C2H3O2)2 içeren 5,00 L’lik bir çözeltinin molar konsantrasyonu 0,160 M’dir.
