Etil asetat, meyvemsi bir kokuya sahip, renksiz bir sıvıdır. İlaç, kozmetik ve gıda gibi çeşitli endüstrilerde yaygın olarak solvent olarak kullanılır. Etil asetat son derece yanıcıdır ve dikkatle kullanılmalıdır.
| IUPAC Adı | Etil asetat |
| Moleküler formül | C4H8O2 |
| CAS numarası | 141-78-6 |
| Eş anlamlı | Asetik Asit Etil Ester, Etil Etanoat, Asetoksietan, Asetidin, Etil Asetat, Etil Asetik Ester |
| InChI | InChI=1S/C4H8O2/c1-3-6-4(2)5/h3H2.1-2H3 |
Etil asetatın özellikleri
Etil asetatın yoğunluğu g/ml
Etil etanoatın yoğunluğu, standart sıcaklık ve basınç koşulları altında 0,902 g/ml’dir. Bu yoğunluk, etil etanoatın sudan daha az yoğun olduğunu ve suyun üzerinde yüzeceğini gösterir. Bu özellik, sıvı karışımların sıvı-sıvı ekstraksiyon işlemi yoluyla ayrılmasında faydalı olmasını sağlar.
Etil asetatın yapısı
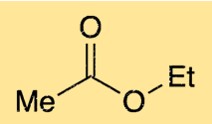
Etil etanoatın yapısı, bir ester fonksiyonel grubuna sahip dört karbonlu bir zincirden oluşur. Ester fonksiyonel grubu, bir karbon atomuna bağlanan bir oksijen atomundan ve bu da başka bir oksijen atomuna bağlanan bir karbon atomundan oluşur. Ester grubundaki oksijen atomu da dört karbonlu zincirdeki karbon atomlarından birine bağlıdır. Bu yapı etil etanoata karakteristik meyvemsi kokusunu verir.
Etil asetatın molar kütlesi
Etil asetatın molar kütlesi 88,11 g/mol’dür. Bir etil asetat molekülündeki tüm atomların atom ağırlıklarının eklenmesiyle belirlenir. Etil asetatın moleküler formülü C4H8O2’dir; bu, her molekülde 4 karbon atomu, 8 hidrojen atomu ve 2 oksijen atomu bulunduğunu gösterir. Etil asetatın molar kütlesi, belirli bir numunedeki madde miktarının veya belirli bir hacimdeki bir maddenin kütlesinin belirlenmesi gibi birçok hesaplamada kullanılır.
Etil asetatın kaynama noktası
Etil etanoatın kaynama noktası standart basınçta 77,1°C’dir (171,8°F). Etil etanoatın nispeten düşük bir kaynama noktasına sahip olması onu birçok endüstriyel uygulamada ekstraksiyon, saflaştırma ve temizleme için bir çözücü olarak faydalı kılar. Kaynama noktasına kadar ısıtıldığında etil etanoat buharlaşır ve yoğunlaşma yoluyla saf bir sıvı olarak toplanabilir.
Etil Asetatın Erime Noktası
Etil etanoatın erime noktası -83,6°C’dir (-118,5°F). Bu düşük erime noktası, etil etanoatın oda sıcaklığında katı yerine genellikle sıvı formda bulunduğu anlamına gelir. Ancak aşırı düşük sıcaklıklarda veya basınç altında katılaşabilir. Etil etanoatın katı formu genellikle beyaz kristalli bir tozdur.
Etil Asetatın Molekül Ağırlığı
Etil etanoatın moleküler ağırlığı 88,11 g/mol’dür. Bu değer bir mol etil etanoat molekülünün kütlesini temsil eder. Molekül ağırlığı, belirli bir numunedeki madde miktarının veya belirli bir hacimdeki maddenin kütlesinin belirlenmesi gibi birçok hesaplamada kullanılır.
Etil Asetat Formülü
Etil etanoatın kimyasal formülü C4H8O2’dir. Bu formül, bir etil etanoat molekülünü oluşturan atomların sayısını ve türünü temsil eder. Formüldeki dört karbon atomu, her bir karbon atomu diğer iki atoma bağlı olacak şekilde bir zincir halinde düzenlenmiştir. Karbon atomlarından ikisi aynı zamanda ester fonksiyonel grubundaki oksijen atomlarına da bağlıdır. Geriye kalan iki karbon atomunun her biri üç hidrojen atomuna bağlıdır.
| Dış görünüş | Renksiz sıvı |
| Spesifik yer çekimi | 0,902 g/cm³ |
| Renk | Renksiz |
| Koku | Meyveli, tatlı |
| Molar kütle | 88,11 g/mol |
| Yoğunluk | 0,902 g/cm³ |
| Füzyon noktası | -83,6°C |
| Kaynama noktası | 77,1°C |
| Flaş noktası | -4°C |
| sudaki çözünürlük | 20°C’de 80 g/L |
| çözünürlük | Alkol, eter, aseton, kloroformda çözünür |
| Buhar basıncı | 20°C’de 73,3 mmHg |
| Buhar yoğunluğu | 3.04 |
| pKa | 4.76 |
| pH | Doğal |
Etil etanoat, çeşitli endüstriyel ve laboratuvar uygulamalarında yaygın olarak kullanılan renksiz bir sıvıdır. Ancak güvenli kullanım ve kullanım için dikkate alınması gereken bazı güvenlik ve sağlık riskleri taşır. Etil etanoata maruz kalmak gözlerde, ciltte ve solunum sisteminde tahrişe neden olabilir. Ayrıca baş ağrısına, baş dönmesine ve mide bulantısına da neden olabilir. Etil etanoat yanıcıdır ve ısıya veya aleve maruz kalması durumunda yangına veya patlamaya neden olabilir. Etil etanoatın iyi havalandırılan bir alanda, tutuşma kaynaklarından uzakta saklanması ve işlenmesi önemlidir. Kazara maruz kalma durumunda, daha fazla zararın önlenmesi için derhal tıbbi yardıma başvurulmalıdır. Yaralanma veya hasar riskini en aza indirmek için etil etanoat kullanılırken uygun güvenlik önlemleri ve koruyucu ekipman kullanılmalıdır.
| Tehlike sembolleri | Şi, F |
| Güvenlik Açıklaması | Cilt ve gözlerle temasından kaçının. Ateşleme kaynaklarından uzak tutun. İyi havalandırılan bir ortamda kullanınız. |
| BİR tanımlayıcılar | UN1173 |
| HS kodu | 2915.31.00 |
| Tehlike sınıfı | 3 – Yanıcı sıvılar |
| Paketleme grubu | GE II |
| Toksisite | LD50 (oral, sıçan) – 2 g/kg |
Etil asetatın sentezi için yöntemler
Esterifikasyon ve dehidrojenasyon olmak üzere iki ana yöntem, endüstride yüksek verimle aktif olarak etil etanoatı sentezler.
Esterleştirme yöntemi, sülfürik asit gibi güçlü bir asit katalizörünün varlığında etanol ile asetik asit arasındaki reaksiyonu içerir. Damıtma, endüstride yaygın olarak kullanılan yüksek verimde etil etanoat üretmek için reaksiyon sonucu ortaya çıkan etil etanoat ve suyu ayırır.
Dehidrojenasyon yöntemi, etanol ve asetik asidin yüksek sıcaklıkta bir bakır(II) oksit katalizörü üzerinde reaksiyonunu içerir. Katalizör, etanolün dehidrojenasyonunu teşvik ederek etilen üretir ve bu daha sonra asetik asitle reaksiyona girerek etil etanoat oluşturur. Bu yöntem esterleştirmeden daha az yaygındır ve genellikle daha yüksek sıcaklıklar ve daha uzun reaksiyon süreleri gerektirir.
Etil etanoatı sentezlemenin başka bir yöntemi, etanol ve asetik anhidrürün reaksiyona sokulmasını içerir. Bu yöntem, damıtma yoluyla ayrılabilen etil etanoat ve asetik asit üretimiyle sonuçlanır.
Etil Asetatın Kullanım Alanları
Etil etanoat, çeşitli endüstriyel ve tüketici uygulamalarında yaygın olarak kullanılan çok yönlü bir kimyasal bileşiktir. Etil etanoatın en yaygın kullanımlarından bazıları şunlardır:
- Solvent: Üreticiler bunu boyalarda, kaplamalarda ve yapıştırıcılarda güçlü bir solvent olarak kullanırlar.
- Aroma maddesi: Yiyecek ve içecek endüstrisinde, özellikle meyve aromalı içeceklerin üretiminde aroma maddesi olarak kullanılır.
- Koku: Hoş meyvemsi kokusu nedeniyle parfümlerde, kolonyalarda ve diğer kişisel bakım ürünlerinde yaygın olarak kullanılan bir içeriktir.
- Uçucu Yağ Ekstraksiyonu: Bitki ve çiçeklerden uçucu yağların ekstraksiyonunda kullanılır.
- İlaçlar: İlaç üretiminde, özellikle antibiyotik üretiminde solvent olarak kullanılır.
- Temizlik maddesi: Elektronik cihazları, tekstil ürünlerini ve diğer malzemeleri temizlemek için kullanılır.
- Suni deri: Suni deri üreticileri, plastikleştirici olarak etil asetat kullanarak malzemeyi yumuşatır ve daha esnek hale getirir.
- Kimyasal ara madde: Kimyasal üreticileri, kimyasal ara madde olarak etil etanoatı kullanarak selüloz asetat, vinil asetat ve etil akrilat gibi başka kimyasallar oluşturur.
Sorular:
S: Etil asetat polar mı yoksa polar değil mi?
C: Etil etanoat, moleküler yapısında karbonil grubu (C=O) ve oksijen atomunun varlığından dolayı polar bir çözücüdür. Ancak su veya etanol gibi diğer çözücüler kadar polar değildir.
S: Etil asetat suyla karışabilir mi?
C: Etil etanoat suyla karışmaz, yani suyla iyi karışmaz. Bunun nedeni iki madde arasındaki polarite farkından kaynaklanmaktadır; çünkü su oldukça polar bir solventtir ve etil etanoat daha az polar bir solventtir.
S: Etil asetat suda çözünür mü?
C: Etil etanoat suda az çözünür ve oda sıcaklığında yaklaşık %8’lik bir çözünürlüğe sahiptir. Ancak bu çözünürlük, iki madde arasındaki polarite farkından dolayı sınırlıdır. Etil etanoat, heksan veya tolüen gibi polar olmayan çözücülerde daha fazla çözünür.
