Kalsiyum karbonat, CaCO3 formülüne sahip kimyasal bir bileşiktir. Yaygın olarak kayalarda ve kabuklarda bulunur ve çimento, boya ve besin takviyelerinin üretiminde kullanılır.
| IUPAC Adı | Kalsiyum karbonat |
| Moleküler formül | CaCO3 |
| CAS numarası | 471-34-1 |
| Eş anlamlı | Kireçtaşı, tebeşir, kalsit, aragonit, mermer, çökeltilmiş kalsiyum karbonat, karbonik asidin kalsiyum tuzu (1:1) |
| InChI | InChI=1S/CH2O3.Ca/c2-1(3)4;/h(H2,2,3,4);/q;+2/p-2 |
CaCO3 Molar kütle
Kalsiyum karbonatın molar kütlesi 100,09 g/mol’dür. Bu, bir mol kalsiyum karbonatın 100.09 gram bileşik içerdiği anlamına gelir. Molar kütle stokiyometrik hesaplamalarda önemlidir çünkü molden grama veya tam tersi dönüşüme izin verir.
Kalsiyum Karbonat Formülü
Kalsiyum karbonatın kimyasal formülü CaCO₃’dur. Bu, her kalsiyum karbonat molekülünün bir kalsiyum atomu, bir karbon atomu ve üç oksijen atomu içerdiği anlamına gelir. Formül, belirli bir uygulama için gereken kalsiyum karbonat miktarının belirlenmesi ve kimyasal özelliklerinin anlaşılması açısından önemlidir.
Kalsiyum karbonatın kaynama noktası
Kalsiyum karbonatın kaynama noktası yoktur çünkü kaynama noktasına ulaşmadan ayrışır. Atmosfer basıncında, kalsiyum karbonat 825°C’nin üzerindeki sıcaklıklarda kalsiyum oksit ve karbondioksite ayrışır. Bu nedenle kalsiyum karbonat, çimento üretimi gibi yüksek sıcaklık uygulamalarında yaygın olarak kullanılır.
Kalsiyum Karbonat Erime Noktası
Kalsiyum karbonatın erime noktası 1339°C’dir. Bu sıcaklıkta kalsiyum karbonat, kalsiyum oksit ve karbondioksit oluşturmak üzere termal ayrışmaya uğrar. Erime noktası, kalsiyum karbonatın yüksek sıcaklıklardaki davranışını anlamak için önemlidir.
Kalsiyum Karbonatın Yoğunluğu g/ml
Kalsiyum karbonatın yoğunluğu 2,71 g/cm³’tür. Bu, kalsiyum karbonatın sudan daha yoğun olduğu ve suya konulduğunda batacağı anlamına gelir. Yoğunluk, kalsiyum karbonatın fiziksel özelliklerini anlamak ve çeşitli uygulamalardaki kullanımlarını belirlemek için önemlidir.
Kalsiyum Karbonat Molekül Ağırlığı
Kalsiyum karbonatın moleküler ağırlığı 100,09 g/mol’dür. Bu, bileşiğin bir kalsiyum atomu, bir karbon atomu ve üç oksijen atomundan oluştuğu anlamına gelir. Molekül ağırlığı, belirli bir uygulama için gerekli olan kalsiyum karbonat miktarının belirlenmesi ve kimyasal özelliklerinin anlaşılması açısından önemlidir.
Kalsiyum karbonatın yapısı
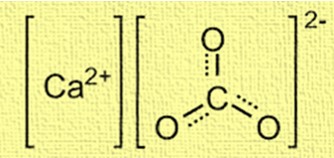
Kalsiyum karbonatın yapısı kristaldir ve kalsiyum iyonlarından (Ca²⁺) ve karbonat iyonlarından (CO₃²⁻) oluşur. Kalsiyum iyonları yapının merkezinde bulunur ve altı karbonat iyonu ile çevrilidir. Karbonat iyonları, her bir oksijen atomunun karbon atomuna bir çift bağ ile bağlandığı, üçgen düzlemsel bir şekilde düzenlenmiştir. Yapı, kalsiyum karbonatın kabukların ve mercan resiflerinin oluşumu gibi çeşitli uygulamalardaki davranışını anlamak için önemlidir.
| Dış görünüş | Beyaz toz veya renksiz kristal |
| Spesifik yer çekimi | 2.71 |
| Renk | Beyaz |
| Koku | Kokusuz |
| Molar kütle | 100,09 gr/mol |
| Yoğunluk | 2,71 g/cm³ |
| Füzyon noktası | 1339°C |
| Kaynama noktası | Kaynamadan önce parçalanır |
| Flaş noktası | Uygulanamaz |
| sudaki çözünürlük | 0,0013 g/100 ml (25°C) |
| çözünürlük | Suda ve çoğu organik çözücüde çözünmez |
| Buhar basıncı | İhmal edilebilir |
| Buhar yoğunluğu | Uygulanamaz |
| pKa | Sabah 9:00 (ilk); 11,8 (saniye) |
| pH | 9,3 – 9,7 (0,1 M sulu çözelti) |
Kalsiyum Karbonatın Güvenliği ve Tehlikeleri
Kalsiyum karbonat, talimatlara uygun olarak kullanıldığında genellikle insanlar ve çevre için güvenli kabul edilir. Ancak kalsiyum karbonat tozunun solunması solunum yollarında, gözlerde ve ciltte tahrişe neden olabilir. Yüksek konsantrasyonda kalsiyum karbonat tozuna uzun süre maruz kalmak akciğer hasarına neden olabilir. Kalsiyum karbonat ayrıca güçlü asitlerle reaksiyona girerek karbondioksit üretebilir ve bu da bazı durumlarda yangın veya patlama tehlikesine neden olabilir. Kalsiyum karbonatla çalışırken koruyucu ekipman giymek ve yeterli havalandırma sağlamak gibi uygun güvenlik prosedürlerinin izlenmesi önemlidir.
| Tehlike sembolleri | Uygulanamaz |
| Güvenlik Açıklaması | Tozu solumaktan kaçının. Koruyucu ekipman giyin. |
| BM kimlik numaraları | Düzenlenmemiş |
| HS kodu | 2836.50.00 |
| Tehlike sınıfı | Düzenlenmemiş |
| Paketleme grubu | Uygulanamaz |
| Toksisite | İnsanlar ve çevre için düşük toksisite |
Kalsiyum karbonat sentez yöntemleri
Çökeltme, karbonasyon ve sol-jel yöntemleri dahil olmak üzere çeşitli yöntemler kalsiyum karbonatı (CaCo3) sentezleyebilir.
Çökeltme yöntemi, bir CaCo3 çökeltisi oluşturmak için kalsiyum hidroksitin kontrollü koşullar altında sodyum karbonat gibi çözünür bir karbonat tuzu ile karıştırılmasını içerir. Nihai ürünü elde etmek için çökeltinin filtrelenmesi ve kurutulması gerekir.
Karbonatlama yöntemi, CaCo3 üretmek için kalsiyum oksidin yüksek basınç ve sıcaklık altında karbondioksit ile reaksiyona sokulmasını içerir. Karbondioksitin kaçmasını önlemek için reaksiyonun kapalı bir sistem içerisinde gerçekleştirilmesi gerekmektedir. Daha sonra, reaksiyona girmemiş herhangi bir kalsiyum oksit veya karbon dioksit, elde edilen CaCo3’ten ayrılmalı ve saflaştırılmalıdır.
Sol-jel yöntemi, kalsiyum alkoksit veya kalsiyum nitrat gibi kalsiyum içeren bir öncünün, bir çözücü ve bir katalizör varlığında hidrolizini ve yoğunlaşmasını içerir. CaCo3 üretmek için elde edilen jelin kurutulması ve kalsine edilmesi gerekir.
CaCo3 sentez yöntemi, mercanlar veya istiridye kabukları gibi canlı organizmaların CaCo3 kristalleri ürettiği biyomineralizasyonun kullanımını içerir. Operatörler bu kristalleri toplar ve son ürünü elde etmek için bunları işler.
Her yöntemin kendine göre avantajları ve dezavantajları vardır ve yöntemin seçimi maliyet, saflık ve son ürünün istenen parçacık boyutu gibi faktörlere bağlıdır.
Kalsiyum Karbonatın Kullanım Alanları
Kalsiyum karbonatın düşük toksisite, yüksek saflık ve düşük maliyet gibi özelliklerinden dolayı çeşitli endüstrilerde birçok kullanımı vardır. Kalsiyum karbonatın bazı yaygın kullanımları şunlardır:
- İnşaat: Kireçtaşı, mermer ve tebeşir şeklinde yapı malzemesi olarak kullanılır. Çimento, harç ve betonun mukavemetini ve dayanıklılığını arttırmak için dolgu maddesi olarak kullanılır.
- İlaçlar: Antasitler ve kalsiyum takviyelerinin üretiminde kullanılır. Tablet ve kapsül formülasyonlarında yardımcı madde olarak kullanılır.
- Yiyecek ve İçecek: Kalsiyumun güçlendirilmesi amacıyla gıda katkı maddesi olarak ve içeceklerde pH ayarlayıcı olarak kullanılır.
- Kağıt ve kağıt hamuru: Kağıt ve karton üretiminde basılabilirliği ve beyazlığı arttırmak için dolgu ve kaplama maddesi olarak kullanılır.
- Plastikler: Plastik ürünlerde mekanik özelliklerini iyileştirmek ve maliyetleri azaltmak amacıyla dolgu ve takviye olarak kullanılır.
- Boyalar ve Kaplamalar: Boya ve kaplamalarda opaklık ve örtücülüğü arttırmak için pigment ve dolgu maddesi olarak kullanılır.
- Tarım: Toprak kalitesini ve ürün büyümesini iyileştirmek için toprak düzenleyici olarak kullanılır.
- Su Arıtma: Asidik suyu nötralize etmek ve sudaki yabancı maddeleri uzaklaştırmak için kullanılır.
Bunlar kalsiyum karbonatın en yaygın kullanımlarından bazılarıdır, ancak çeşitli endüstrilerde başka birçok uygulama da vardır.
Sorular:
Soru: Kalsiyum karbonat suda çözünür mü?
C: Kalsiyum karbonatın suda çözünürlüğü düşüktür; çözünürlüğü 25°C’de yaklaşık 0,0013 g/100 mL’dir.
Soru: Kalsiyum karbonat nedir?
C: Kalsiyum karbonat, CaCO3 formülüne sahip kimyasal bir bileşiktir. Kayalarda, deniz organizmalarının kabuklarında ve çeşitli maden yataklarında bulunan yaygın bir maddedir.
S: Kalsiyum karbonatı nerede bulabilirsiniz?
C: Kalsiyum karbonat kireçtaşı, tebeşir ve mermer gibi çeşitli doğal kaynaklarda bulunabilir. Ayrıca istiridye, istiridye ve mercan gibi deniz organizmalarının kabuklarında da bulunur.
S: Kalsiyum karbonat iyonik mi yoksa kovalent mi?
C: Kalsiyum karbonat, bir kalsiyum katyonu (Ca2+) ve bir karbonat anyonundan (CO32-) oluşan iyonik bir bileşiktir.
S: Kalsiyum karbonat, gömülebilen ve _____ şeklinde sertleştirilebilen bir tür hidrojenlenmiş tortudur.
C: Kalsiyum karbonat, kireçtaşına gömülebilen ve sertleşebilen bir tür hidrojenlenmiş tortudur.
Soru: Prekambriyen siyanobakterilerin kalsiyum karbonattan yaptığı katmanlı yapılara _____ denir.
C: Prekambriyen siyanobakterilerin kalsiyum karbonattan yaptığı katmanlı yapılara stromatolit denir.
