Bromotimol mavisi (BTB), bazik bir çözelti varlığında rengi sarıdan maviye değiştiren bir pH göstergesidir. Bilimsel deneylerde ve tıbbi teşhis aracı olarak yaygın olarak kullanılır.
| IUPAC Adı | 3′,3”-dibromotimolsülfonftalein |
| Moleküler formül | C27H28Br2O5S |
| CAS numarası | 76-59-5 |
| Eş anlamlı | bromotimol sülfonftalein; 4,4′-(1,1-dioksido-3H-2,1-benzoksatiyole-3,3-diil)bis(2-bromo-3-metil-6-(1-metiletil)fenol) |
| InChI | InChI=1S/C27H28Br2O5S/c1-13(2)17-11-20(15(5)23(28)18(17)7-9-19(24(20)29)8-10-21(27) 22(30)12-25(31)32)37(33,34)36-26-14(3)6-4-16(35-26)24-7-9-29-11-10-23( 24)28/h4-7,9-12,31-32H.8H2.1-3H3 |
Bromotimol Mavi Molar Kütle
BTB’nin molar kütlesi 624,38 g/mol’dür. Molar kütle, bir maddenin bir molünün kütlesidir ve kimyasal reaksiyonları içeren hesaplamalarda yaygın olarak kullanılır. BTB’nin molar kütlesi, C27H28Br2O5S olan kimyasal formülündeki tüm atomların atom ağırlıkları toplanarak hesaplanır. Bir maddenin molar kütlesinin bilinmesi, belirli bir reaksiyon için gereken madde miktarının belirlenmesinin yanı sıra reaksiyonda üretilen ürün miktarının belirlenmesi açısından da önemlidir.
Bromotimol mavisinin kaynama noktası
BTB’nin kaynama noktası 760 mmHg’de 636,3°C’dir. Kaynama noktası, bir maddenin belirli bir basınçta sıvı halden gaz haline geçtiği sıcaklıktır. BTB’nin yüksek kaynama noktası, normal koşullar altında kolayca buharlaşmayan veya ayrışmayan stabil bir bileşik olduğunu gösterir. Bir maddenin kaynama noktası onun saflığını belirlemek için kullanılabilir, çünkü safsızlıklar kaynama noktasını değiştirebilir.
Bromotimol mavisi Erime noktası
BTB’nin erime noktası 165-170°C’dir. Erime noktası, katı bir maddenin katı durumdan sıvı duruma geçtiği sıcaklıktır. Bir maddenin erime noktası, onu tanımlamak ve karakterize etmek için kullanılır, çünkü farklı maddeler farklı erime noktalarına sahiptir. BTB’nin erime noktası nispeten yüksektir, bu da onun kolayca ayrışmayan stabil bir bileşik olduğunu gösterir.
Bromotimol mavisi Yoğunluk g/ml
BTB’nin yoğunluğu 1,36 g/mL’dir. Yoğunluk, bir maddenin birim hacim başına kütlesidir ve bir maddedeki moleküllerin ne kadar yoğun olduğunu ölçer. BTB’nin yoğunluğu onun nispeten yoğun bir bileşik olduğunu gösterir ve yoğunluk ölçümlerinde yaygın olarak standart olarak kullanılır.
Bromotimol Mavisi Molekül Ağırlığı
BTB’nin moleküler ağırlığı 624,38 g/mol’dür. Molekül ağırlığı, bir moleküldeki tüm atomların atom ağırlıklarının toplamıdır ve kimyasal reaksiyonlarda önemli bir faktördür. BTB’nin moleküler ağırlığı, belirli bir reaksiyon için gereken madde miktarının yanı sıra bir reaksiyonda üretilen ürün miktarını belirlemek için kullanılır.
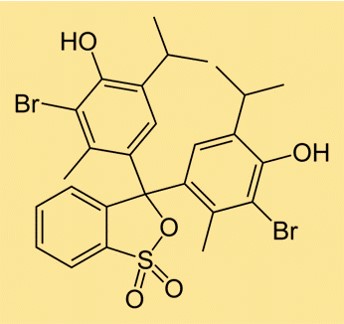
Bromotimol mavisinin yapısı
BTB’nin yapısı, her birine bir brom atomunun bağlı olduğu iki aromatik halkadan oluşur. Ayrıca halkalardan birine bağlı bir sülfonat grubu da vardır ve bu da molekülün suda çözünür olmasını sağlar. BTB’nin yapısı, bir çözeltinin asitliğini veya bazlığını belirlemek için kullanılan diğer pH göstergelerine benzer.
Bromotimol Mavi Formülü
BTB’nin kimyasal formülü C27H28Br2O5S’dir. Formül, moleküldeki atomların sayısını ve türlerini gösterir ve kimyasal reaksiyonlarda, belirli bir reaksiyon için gereken madde miktarını belirlemek için kullanılır. BTB’nin formülü, ona asidik çözeltilerde kendine özgü sarı-yeşil rengini veren iki brom atomu ve suda çözünür hale getiren bir sülfonat grubu içerdiğini gösterir.
| Dış görünüş | Koyu yeşil toz |
| Spesifik yer çekimi | 1.36 |
| Renk | sarımtırak yeşil |
| Koku | Kokusuz |
| Molar kütle | 624,38 gr/mol |
| Yoğunluk | 1.36g/ml |
| Füzyon noktası | 165-170°C |
| Kaynama noktası | 760 mmHg’de 636,3°C |
| Flaş noktası | Uygulanamaz |
| sudaki çözünürlük | Çözünür |
| çözünürlük | Etanolde çözünür, eter ve kloroformda az çözünür |
| Buhar basıncı | Uygulanamaz |
| Buhar yoğunluğu | Uygulanamaz |
| pKa | 6.3 |
| pH | pH 6,0’da sarı, pH 7,6’da yeşil, pH 7,9’da mavi |
Bromotimol mavisinin güvenliği ve tehlikeleri
BTB yutulursa, solunursa veya deri yoluyla emilirse zararlı olabilir. Bu gözlerde, ciltte ve solunum sisteminde tahrişe neden olabilir. Yutma gastrointestinal tahrişe, mide bulantısına, kusmaya ve karın ağrısına neden olabilir. BTB tozunun veya buharının solunması solunum yolu tahrişine, öksürüğe ve nefes almada zorluğa neden olabilir. Bu madde aynı zamanda sudaki yaşama da zararlı olabilir ve su kaynaklarına atılmamalıdır. BTB kullanılırken eldiven ve göz koruması gibi uygun kişisel koruyucu ekipmanlar kullanılmalı ve uygun laboratuvar prosedürleri ve düzenlemelerine uygun olarak kullanılmalı ve atılmalıdır.
| Tehlike sembolleri | Hiçbiri |
| Güvenlik Açıklaması | S22: Tozu solumayın. S24/25: Cilt ve gözlerle temasından kaçının. S36/37/39: Uygun koruyucu kıyafet, eldiven ve göz/yüz koruması kullanın. |
| BİR tanımlayıcılar | Düzenlenmemiş |
| HS kodu | 2921.59.90 |
| Tehlike sınıfı | sınıflandırılmamış |
| Paketleme grubu | Uygulanamaz |
| Toksisite | LD50 (oral, sıçan) = 4.500 mg/kg |
Bromotimol mavisinin sentezi için yöntemler
BTB’yi sentezlemek için farklı yöntemler vardır.
Yaygın bir yöntem, hidroklorik asit gibi güçlü bir asit katalizörünün varlığında timol mavisi ile bromin arasındaki reaksiyondur. Reaksiyon, timol mavisi molekülüne bromun elektrofilik eklenmesi ve ardından bir hidrojen atomunun bir bromin atomu ile ikame edilmesiyle ilerler. Ortaya çıkan bileşik BTB’dir.
Başka bir yöntem, güçlü bir asit katalizörünün varlığında 2,6-dibromoindofenol ile kresol kırmızısı arasındaki reaksiyonu içerir. Reaksiyon, krezol kırmızısı molekülündeki bir hidrojen atomunun, 2,6-dibromoindofenol molekülündeki bir bromin atomu ile elektrofilik ikamesi yoluyla gerçekleşir. Ortaya çıkan bileşik BTB’dir.
Üçüncü bir yöntem, sodyum hidroksit varlığında timol mavisi ile sodyum bromür arasındaki reaksiyonu içerir. Reaksiyon, timol mavisi molekülündeki bir hidrojen atomunun, sodyum bromür molekülündeki bir bromin atomu ile değiştirilmesiyle gerçekleşir. Ortaya çıkan bileşik BTB’dir.
Kullanılan yöntem ne olursa olsun, saf BTB elde etmek için elde edilen ürünün yeniden kristalleştirme veya kolon kromatografisi yoluyla saflaştırılması gerekir.
Bromtimol Mavisinin Kullanım Alanları
BTB’nin çeşitli alanlarda birçok uygulaması vardır. BTB’nin bazı kullanım alanları şunlardır:
- İndikatör: pH aralığı 6,0 ila 7,6 olan asit-baz indikatörü olarak kullanılır. pH 6,0’da sarı, pH 7,6’da yeşil ve pH 7,9’da mavidir.
- Laboratuvar Deneyleri: Karbondioksit ve diğer gazların varlığını test etmek ve solunum katsayısını belirlemek için çeşitli laboratuvar deneylerinde kullanılır.
- Su Ürünleri Yetiştiriciliği: Su ürünleri yetiştiriciliğinde akvaryumlar ve havuzlardaki su pH seviyelerini izlemek için kullanılır.
- Tıbbi Alan: İdrar örneklerinde safra varlığının test edilmesi ve mantar enfeksiyonlarının varlığının tespit edilmesi amacıyla kullanılır.
- Eğitim: Asit-baz reaksiyonlarının ilkelerini göstermek ve öğrencilere pH düzeylerini öğretmek için eğitimde görsel bir yardımcı olarak kullanılır.
- Tarım Endüstrisi: Bitki sağlığı ve büyümesinin belirlenmesinde önemli bir faktör olan toprağın pH seviyelerini ölçmek için kullanılır.
- Çevresel Testler: Göller ve nehirler gibi su kaynaklarının su yaşamına uygunluklarını sağlamak amacıyla pH seviyelerini ölçmek için çevresel testlerde kullanılır.
Genel olarak BTB, çeşitli alanlarda birçok uygulamaya sahip çok yönlü bir bileşiktir.
Sorular:
S: Bromotimol mavisi nedir?
C: BTB, laboratuvar deneylerinde ve diğer çeşitli uygulamalarda yaygın olarak kullanılan bir pH göstergesidir. Bir çözeltinin asitliğine veya alkaliliğine bağlı olarak renk değiştiren kimyasal bir bileşiktir.
S: Bromotimol mavisinin pH aralığı nedir?
C: BTB’nin pH aralığı 6,0 ila 7,6 arasındadır. pH 6,0’da sarı, pH 7,6’da yeşil ve pH 7,9’da mavidir.
S: Bromotimol mavisinin renk değişimi nedir?
C: BTB’nin renk değişimi çözeltinin pH’ına bağlıdır. pH 6,0’da sarı, pH 7,6’da yeşil ve pH 7,9’da mavidir.
Soru: Bromotimol mavisi asit mi yoksa baz mı? C: BTB ne asit ne de bazdır. Bir çözeltinin asitliğine veya alkaliliğine bağlı olarak renk değiştiren bir göstergedir.
