Nitrobenzen veya C6H5NO2, soluk sarı renkte ve belirgin bir kokuya sahip organik bir bileşiktir. Anilin ve diğer kimyasalların üretiminde öncü olarak kullanılır. Aynı zamanda toksik bir maddedir.
| IUPAC Adı | nitrobenzen |
| Moleküler formül | C6H5NO2 |
| CAS numarası | 98-95-3 |
| Eş anlamlı | Nitrobenzol, Nitrobenzen, Mirbane Özü, NB |
| InChI | InChI=1S/C6H5NO2/c8-7(9)6-4-2-1-3-5-6/h1-5H |
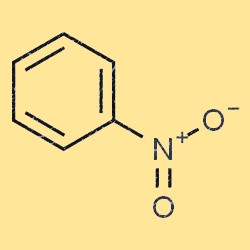
Nitrobenzenin yapısı
Nitrobenzen düz, düzlemsel bir moleküler yapıya sahiptir. Karbon atomlarından birine bağlı bir nitro grubuna (-NO2) sahip bir benzen halkasından (C6H5) oluşur. Nitro grubu elektron çeken bir gruptur, yani benzen halkasının elektron yoğunluğunu azaltır. Bu özellik nitrobenzeni birçok kimyasal reaksiyonda benzenden daha az reaktif hale getirir.
Nitrobenzen formülü
Nitrobenzenin kimyasal formülü C6H5NO2’dir. Bu formül, molekülü oluşturan atomların sayısını ve türünü temsil eder. Benzen halkası molekülün omurgasını oluştururken nitro grubu bileşiğin özelliklerini etkileyen polar fonksiyonel bir grup oluşturur. Nitrobenzenin formülü, onun kimyasal ve fiziksel özelliklerinin yanı sıra diğer maddelerle reaktivitesinin anlaşılması açısından da önemlidir.
Nitrobenzenin molar kütlesi
C6H5NO2 olarak da adlandırılan nitrobenzenin molar kütlesi 123,11 g/mol’dür. Bu, bileşikteki tüm atomların atomik kütlelerinin eklenmesiyle hesaplanır. Nitrobenzenin kimyasal yapısında altı karbon atomu ve bir nitrojen atomu bulunması nedeniyle nispeten yüksek bir molar kütleye sahiptir.
Nitrobenzenin kaynama noktası
Nitrobenzenin kaynama noktası 210,9°C’dir. Bu, benzer moleküler ağırlığa sahip diğer organik bileşiklerle karşılaştırıldığında nispeten yüksektir. Yüksek kaynama noktası, nitrobenzen molekülleri arasındaki hidrojen bağları ve dipol-dipol etkileşimleri gibi güçlü moleküller arası çekici kuvvetlerin varlığından kaynaklanmaktadır.
Nitrobenzenin erime noktası
Nitrobenzenin erime noktası 5,85°C’dir. Bu, kaynama noktasıyla karşılaştırıldığında nispeten düşüktür; bu, katı haldeki moleküller arası çekim kuvvetlerinin sıvı duruma göre daha zayıf olmasıyla açıklanabilir. Ek olarak nitrobenzen polimorfizm sergileyebilir, yani farklı erime noktalarına sahip birden fazla kristal yapıda mevcut olabilir.
Nitrobenzen yoğunluğu g/ml
Nitrobenzenin yoğunluğu oda sıcaklığında (25°C) 1,20 g/mL’dir. Bu, nitrobenzenin aynı sıcaklıkta yoğunluğu 1 g/mL olan sudan daha yoğun olduğu anlamına gelir. Nitrobenzenin yoğunluğu, molekül ağırlığından ve moleküllerinin boyutundan ve şeklinden etkilenir.
Nitrobenzenin moleküler ağırlığı
Nitrobenzenin moleküler ağırlığı 123,11 g/mol’dür. Bu, bileşikteki tüm atomların atomik kütlelerinin eklenmesiyle hesaplanır. Nitrobenzenin moleküler ağırlığı, kaynama noktası, erime noktası ve çözünürlük gibi fiziksel ve kimyasal özelliklerinin belirlenmesinde önemlidir.
| Dış görünüş | Soluk sarı sıvı |
| Spesifik yer çekimi | 1,20 gr/cm3 |
| Renk | Soluk sarı |
| Koku | karakteristik |
| Molar kütle | 123,11 g/mol |
| Yoğunluk | 25°C’de 1,20 g/mL |
| Füzyon noktası | 5.85°C |
| Kaynama noktası | 210,9°C |
| Flaş noktası | 77°C |
| sudaki çözünürlük | 25°C’de 7,9 g/L |
| çözünürlük | Organik çözücülerde çözünür |
| Buhar basıncı | 25°C’de 0,68 mmHg |
| Buhar yoğunluğu | 4,35 (hava=1) |
| pKa | -1.15 |
| pH | 7 (nötr) |
Nitrobenzenin güvenliği ve tehlikeleri
Nitrobenzen, çeşitli güvenlik ve sağlık riskleri oluşturan oldukça toksik bir maddedir. Temas veya solunması halinde ciltte, gözlerde ve solunum yollarında tahrişe neden olabilir. Nitrobenzene uzun süre maruz kalmak karaciğer ve böbrek hasarına, anemiye ve methemoglobinemiye neden olabilir. Nitrobenzen de çok yanıcıdır ve nispeten düşük sıcaklıklarda tutuşabilir. Ayrıca ısıtıldığında, yakıldığında veya ayrıştığında zehirli dumanlar açığa çıkarabilir. Bu nedenle nitrobenzenin dikkatli bir şekilde kullanılması, uygun koruyucu ekipman kullanılması ve serin, kuru bir yerde, tutuşma kaynaklarından ve uyumsuz maddelerden uzakta saklanması önemlidir.
| Tehlike sembolleri | T, N |
| Güvenlik Açıklaması | Çok toksiktir, yutulduğunda, solunduğunda veya deri yoluyla emildiğinde zararlıdır, ciddi cilt yanıklarına ve göz hasarına neden olur. |
| BİR tanımlayıcılar | UN1662 |
| HS kodu | 2904.90.90 |
| Tehlike sınıfı | 6.1 |
| Paketleme grubu | II |
| Toksisite | Çok zehirli |
Nitrobenzen sentez yöntemleri
Nitrobenzen, benzenin nitrasyonu, nitrobenzenin indirgenmesi ve nitrobenzenin hidrojenasyonu dahil olmak üzere çeşitli yöntemlerle sentezlenebilir. En yaygın olarak kullanılan yöntem, benzenin nitrik asit ve sülfürik asit karışımı ile yaklaşık 50°C sıcaklıkta reaksiyonunu içeren benzen nitrasyonudur. Nitratlama reaksiyonu, nitrobenzenin yanı sıra benzenin diğer nitro türevlerinin bir karışımını üretir.
Nitrobenzeni sentezlemenin başka bir yöntemi, demir veya çinko ve hidroklorik asit gibi indirgeyici maddelerin kullanımını içeren nitrobenzen indirgemesidir. İndirgeme reaksiyonu, nitrobenzenin nitro grubunu (-NO2) bir amino grubuna (-NH2) dönüştürerek bir yan ürün olarak anilin üretir.
Nitrobenzenin hidrojenasyonu, anilin sentezinin başka bir yöntemidir. Bu yöntem, nikel veya paladyum gibi bir katalizörün ve nitrobenzen ile reaksiyona girerek anilin üreten hidrojen gazının kullanılmasını içerir.
Nitrobenzenin kullanımları
Nitrobenzen çok çeşitli uygulamalarda kullanılan çok yönlü bir kimyasaldır.
- Kimya endüstrisi, boya, kauçuk ve ilaç üretiminde önemli bir bileşen olan anilinin öncüsü olarak nitrobenzeni kullanır. Nitrobenzen, plastik, reçine ve yapıştırıcı üretiminde kullanılan fenol gibi diğer kimyasalların üretiminde değerli bir hammaddedir.
- Sıvı yağlar, katı yağlar ve mumlar gibi organik bileşikler nitrobenzen kullanılarak çözülebilir, bu da onu yararlı bir çözücü haline getirir. Gıda endüstrisinde nitrobenzen, esas olarak sakız üretiminde tatlandırıcı madde olarak kullanılır.
- C6H5NO2, TNT (trinitrotoluen) gibi patlayıcıların üretiminde önemli bir bileşendir. Bir yakıt katkı maddesi olarak nitrobenzen, benzinin oktan sayısının artmasına yardımcı olur.
- C6H5NO2 ayrıca böcek öldürücüler ve mantar öldürücüler de dahil olmak üzere çeşitli pestisitlerin ve herbisitlerin üretiminde de kullanılır.
- Naylon gibi sentetik elyafların üretimi de önemli bir bileşen olarak nitrobenzene dayanır.
Genel olarak nitrobenzenin çok yönlü doğası, onu kimya, gıda ve tekstil endüstrileri de dahil olmak üzere birçok endüstride önemli bir kimyasal haline getirmektedir. Ancak nitrobenzen kullanırken toksisitesi ve yanıcılığı nedeniyle uygun kullanım ve güvenlik önlemleri gereklidir.
Sorular:
Nitrobenzenin anilin ile reaksiyonu
Nitrobenzenin anilin’e dönüşümü, nitro grubunun (-NO2) bir amino grubuna (-NH2) indirgenmesini ve ardından ara ürünün hidrolizini içeren iki aşamalı bir reaksiyondur.
C6H5NO2’nin indirgenmesi genellikle demir veya çinko gibi bir indirgeyici madde ve hidroklorik asit gibi asidik bir çözelti kullanılarak gerçekleştirilir. Reaksiyon, nitrozobenzen adlı bir ara ürün üretir ve bu daha sonra bir asit veya baz katalizörünün varlığında anilin’e indirgenir.
Nitrozobenzen ara maddesinin anilin’e hidrolizi, ara maddenin seyreltik hidroklorik asit gibi asidik bir çözelti ile işlenmesiyle gerçekleştirilir. Reaksiyon anilinin yanı sıra su ve nitrojen oksit (NO) üretir.
Genel reaksiyon şu şekilde temsil edilebilir: Nitrobenzen + 3 H2 → Anilin + 2 H2O + N2
