Butanal veya butiraldehit, C4H8O formülüne sahip organik bir bileşiktir. Keskin bir kokuya sahip renksiz bir sıvıdır ve genellikle diğer kimyasalların sentezi için hammadde olarak kullanılır.
| IUPAC Adı | Bütanal |
| Moleküler formül | C4H8O |
| CAS numarası | 123-72-8 |
| Eş anlamlı | Butiraldehit, bütirik aldehit, bütanaldehit, bütiral, N-bütanal, bütaldehit, bütiril hidrit, 1-bütanal, 1-bütiraldehit |
| InChI | InChI=1S/C4H8O/c1-2-3-4-5/h4H,2-3H2,1H3 |
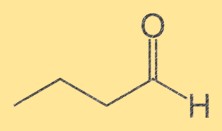
Bütanal yapı
Butanal’in yapısı, bir terminal aldehit grubunun (-CHO) bağlı olduğu dört karbonlu bir zincirden oluşur. Karbon atomları, ilk karbona aldehit grubu eklenecek şekilde sırayla numaralandırılır. Butanal’in yapısı önemlidir çünkü kimyasal ve fiziksel özelliklerini belirler.
Bütanal IR spektrumu
Butanal’in kızılötesi (IR) spektrumu, molekülde bulunan fonksiyonel grupları tanımlamak için kullanılır. Butanal’in IR spektrumu, karbonil grubu (-C=O) için yaklaşık 1730 cm-1’de ve CH gerilme titreşimleri için yaklaşık 2800-3000 cm-1’de karakteristik tepe noktaları gösterir. IR spektrumu organik kimyada bileşikleri tanımlamak ve karakterize etmek için güçlü bir araçtır.
Bütanalin molar kütlesi
Butanal’in molar kütlesi 72,11 g/mol’dür. Bir bileşiğin molar kütlesi, o bileşiğin molekülündeki tüm atomların atomik kütlelerinin toplamıdır. Butanal durumunda molar kütle, dört karbon atomu, sekiz hidrojen atomu ve bir oksijen atomunun atomik kütleleri toplanarak hesaplanır.
Bütanalin kaynama noktası
Butanal’in kaynama noktası 75°C veya 167°F’dir. Bu, sıvının buhar basıncının atmosfer basıncına eşit olduğu ve sıvının kaynamaya başladığı sıcaklıktır. Butanal nispeten düşük bir kaynama noktasına sahiptir, bu da onu uçucu hale getirir ve oda sıcaklığında kolayca buharlaşır.
Bütanalin erime noktası
Butanal’in erime noktası -97°C veya -143°F’dir. Bu, katı bir maddenin sıvı duruma geçtiği sıcaklıktır. Bütanalin erime noktası çok düşüktür, yani oda sıcaklığında genellikle sıvı haldedir.
Butiraldehitin yoğunluğu g/ml
Bütiraldehitin yoğunluğu 0,81 g/mL’dir. Yoğunluk birim hacim başına kütle miktarıdır ve sıvılar için genellikle mililitre başına gram cinsinden ifade edilir. Bütiraldehitin yoğunluğu sudan daha düşüktür, bu da suyun yüzeyinde yüzdüğü anlamına gelir.
Bütiraldehitin moleküler ağırlığı
Bütiraldehitin moleküler ağırlığı 72,11 g/mol’dür. Molar kütle ile aynıdır ve bir bütiraldehit molekülünün kütlesini temsil eder. Molekül ağırlığı kimyasal hesaplamalarda ve analizlerde kullanılan önemli bir parametredir.
Bütiraldehit Formülü
Bütiraldehitin kimyasal formülü C4H8O’dur. Bu formül, bir bütiraldehit molekülündeki her bir elementin atom sayısını gösterir. Bütiraldehitte dört karbon atomu, sekiz hidrojen atomu ve bir oksijen atomu vardır.
| Dış görünüş | Renksiz sıvı |
| Spesifik yer çekimi | 0.81g/ml |
| Renk | Renksiz |
| Koku | Baharatlı, keskin |
| Molar kütle | 72,11 g/mol |
| Yoğunluk | 0.81g/ml |
| Füzyon noktası | -97°C (-143°F) |
| Kaynama noktası | 75°C (167°F) |
| Flaş noktası | -6,7°C (20°F) |
| sudaki çözünürlük | karışabilir |
| çözünürlük | Etanol, eter, asetonda çözünür |
| Buhar basıncı | 20°C’de 44 mmHg |
| Buhar yoğunluğu | 2,5 (hava=1) |
| pKa | 16.92 |
| pH | 4.5-6.5 |
Bütanalin güvenliği ve tehlikeleri
Bütiraldehit yanıcı bir sıvıdır ve ısıya veya aleve maruz kalması durumunda yangın tehlikesi oluşturabilir. Ayrıca temas halinde göz ve cilt tahrişine neden olabilir ve buharlarının solunması solunum yollarının tahriş olmasına neden olabilir. Bu nedenle, bütiraldehitin dikkatli bir şekilde kullanılması ve eldiven ve gözlük gibi uygun kişisel koruyucu ekipman kullanılması önemlidir. Serin, kuru, iyi havalandırılan bir yerde, ısı ve tutuşma kaynaklarından uzakta saklanmalıdır. Maruz kalınması veya yutulması halinde derhal tıbbi yardıma başvurun. Çevrenin kirlenmesini önlemek için bütiraldehit için uygun atık imha prosedürlerinin takip edilmesi de önemlidir.
| Tehlike sembolleri | Alev, Aşındırıcı, Tahriş Edici |
| Güvenlik Açıklaması | Isıdan/kıvılcımdan/açık alevden/sıcak yüzeylerden uzak tutun. Koruyucu eldiven/göz koruması/yüz koruması kullanın. CİLT (veya saç) İLE TEMAS HALİNDE İSE: Kirlenmiş tüm giysileri derhal çıkarın. Cildi su/duş ile durulayın. Yangın durumunda: Söndürmek için kuru kimyevi toz kullanın. |
| BM kimlik numaraları | UN1125 |
| HS kodu | 2912.19.00 |
| Tehlike sınıfı | 3 |
| Paketleme grubu | II |
| Toksisite | Butanal, yutulması, solunması veya deri yoluyla emilmesi halinde zararlıdır. Göz ve cilt tahrişine neden olabilir ve uzun süreli maruz kalma karaciğer ve böbrek hasarına yol açabilir. Ayrıca hayvan çalışmalarında mutajenik ve kanserojen olduğu da gösterilmiştir. Maruziyeti ve kontaminasyonu önlemek için uygun kullanım ve imha önemlidir. |
Bütanal sentez yöntemleri
Butiraldehit, birincil alkollerin oksidasyonu, alkenlerin ozonolizi ve alkenlerin hidroformilasyonu dahil olmak üzere çeşitli yöntemlerle sentezlenebilir.
Bütiraldehit sentezlemenin yaygın bir yöntemi, birincil alkollerin potasyum permanganat veya kromik asit gibi bir oksitleyici madde kullanılarak oksidasyonudur. Birincil alkol ilk önce piridinyum klorokromat gibi yumuşak bir indirgeyici madde kullanılarak karşılık gelen aldehite dönüştürülür ve daha sonra bütiraldehite oksitlenir. Başka bir yöntem, daha sonra sodyum borohidrit gibi bir indirgeyici madde kullanılarak bütiraldehite indirgenebilen aldehitler üretmek için alkenlerin ozon ayrışmasını içerir.
Alkenlerin hidroformilasyonu da bütiraldehitin sentezlenmesinde yaygın olarak kullanılan bir yöntemdir. Bu, alkenin, kobalt karbonil veya rodyum kompleksi gibi bir katalizör varlığında karbon monoksit ve hidrojen gazı ile reaksiyonunu içerir. Elde edilen aldehit daha sonra lityum alüminyum hidrit gibi bir indirgeyici madde kullanılarak bütiraldehite indirgenebilir.
Bütiraldehitin sentezlenmesine yönelik diğer yöntemler arasında Grignard reaktiflerinin formaldehit ile reaksiyonunu ve ketonların bir katalizör varlığında formik asit ve hidrojen gazı ile reaksiyonunu içerir.
Genel olarak sentez yönteminin seçimi, ham maddelerin mevcudiyeti, istenen verim ve saflık ve reaksiyon koşullarının fizibilitesi gibi faktörlere bağlıdır.
Butanalin kullanım alanları
Butanal, reaktifliği ve kendine özgü kokusu nedeniyle çeşitli endüstriyel ve ticari kullanımlara sahiptir.
Butanal’in önemli bir kullanımı, bütil akrilat ve n-butanol gibi diğer kimyasalların üretiminde hammadde olarak kullanılmasıdır. Bu kimyasallar kaplama, yapıştırıcı ve plastik üretiminde kullanılmaktadır.
Butanal ayrıca gıda endüstrisinde aroma maddesi olarak da kullanılır; unlu mamuller, şekerlemeler ve içecekler gibi çeşitli ürünlere meyvemsi, elmaya benzer bir aroma sağlar. Ayrıca parfüm ve sabunlarda koku verici olarak da kullanılır.
Ayrıca Butanal, organik sentezlerde çözücü olarak ve organik kimya reaksiyonlarında reaktif olarak kullanılır. Aldehitleri ikincil alkollere dönüştürmek ve karboksilik asitlerle reaksiyona girerek esterler üretmek için kullanılabilir.
Butanal, güçlü kokusu nedeniyle beyindeki koku alma reseptörü aktivasyonunun mekanizmalarını anlamak için bir araç olarak araştırma çalışmalarında da kullanılmıştır.
Ancak Butanal’in doğru şekilde kullanılmazsa güvenlik riskleri oluşturabileceğini unutmamak ve kullanırken ve saklarken uygun önlemlerin alınması gerektiğini unutmamak gerekir. Genel olarak Butanal’in çok yönlülüğü ve benzersiz özellikleri, onu çeşitli endüstrilerde ve araştırma alanlarında önemli bir kimyasal haline getirmektedir.
Sorular:
Sıvı bütiraldehitin standart oluşum entalpisi nedir, ch3ch2ch2cho(l)?
25°C’de sıvı bütiraldehitin (CH3CH2CH2CHO(l)) standart oluşum entalpisi (∆H°f) -146,6 kJ/mol’dür.
Bu, kendisini oluşturan elementlerin standart hallerinden (bu durumda karbon, hidrojen ve elementel formlarındaki oksijen) 1 mol sıvı bütiraldehidin oluşumuyla ilişkili entalpi değişiminin 25°C’de -146,6 kJ/mol olduğu anlamına gelir. . ve 1 atm basınç.
Negatif işaret reaksiyonun ekzotermik olduğunu, yani ısı açığa çıkardığını gösterir. Bu değer, reaktan veya ürün olarak bütiraldehit içeren reaksiyonların entalpi değişimini hesaplamak için kullanışlıdır.
