4-Etilfenol veya C8H10O, parfümlerde, aromalarda ve tarımda fungisit olarak kullanılan, tatlı, baharatlı ve otsu bir kokuya sahip kimyasal bir bileşiktir. Aynı zamanda şarap bozulmasının bir yan ürünü de olabilir.
| IUPAC Adı | 4-etilfenol |
| Moleküler formül | C8H10O |
| CAS numarası | 104-96-7 |
| Eş anlamlı | p-etilfenol, 4-hidroksietilbenzen, 4-EHP |
| InChI | InChI=1S/C8H10O/c1-7-3-2-6-4-8(7)5-9/h2-5.9H.6H2.1H3 |
Formül 4-etilfenol
4-etilfenolün formülü C8H10O’dur. Formül, moleküldeki atomların sayısını ve türlerini verir ve molekülün molar kütlesini, moleküler ağırlığını ve diğer özelliklerini hesaplamak için kullanılır.
C8H10O NMR
Nükleer manyetik rezonans (NMR) spektroskopisi, bilim adamlarının moleküllerin yapısını ve bileşimini incelemesine olanak tanır. 4-etilfenolün C8H10O NMR spektrumunu analiz ederek, molekülün yapısı ve bileşimi hakkında bilgi veren kimyasal kaymaları, bağlanma sabitlerini ve tepe yoğunluklarını tanımlayabilirler.
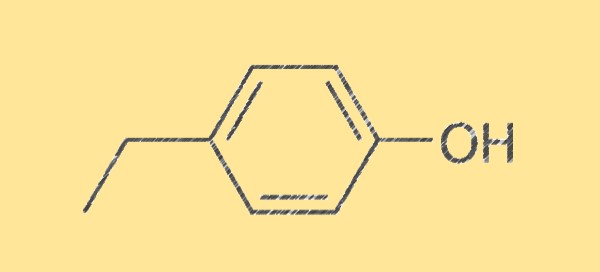
4-etilfenol C8H10O’nun yapısı
4-etilfenolün yapısı, sekiz karbon atomu, on hidrojen atomu ve bir oksijen atomundan oluşan moleküler formülü C8H10O ile karakterize edilir. Tatlı, baharatlı ve otsu bir kokuya sahip renksiz bir sıvıdır. Molekül simetriktir ve bir karbon atomuna bağlı bir hidroksil grubuna (-OH) sahiptir, bu da onu bir fenol yapar.
4-etilfenolün molar kütlesi
4-etilfenolün molar kütlesi 134,17 g/mol’dür. Molar kütle, atomlar, moleküller veya iyonlar gibi bir mol varlık içeren bir maddenin kütlesi olarak tanımlanır. Moleküldeki tüm elementlerin atomik kütlelerinin eklenmesiyle hesaplanır. 4-etilfenol durumunda, moleküler formülü (C8H10O) bize 134,17 g/mol molar kütlesini verir.
4-etilfenolün kaynama noktası
4-etilfenolün kaynama noktası 218,7°C’dir. Bir maddenin kaynama noktası, maddenin buhar basıncının atmosfer basıncına eşit olduğu ve sıvının buhara dönüştüğü sıcaklıktır. 4-etilfenolün kaynama noktası, molekülde mevcut olan moleküller arası çekim kuvvetleri nedeniyle nispeten yüksektir.
4-etilfenolün erime noktası
4-etilfenolün erime noktası 9,7°C’dir. Bir maddenin erime noktası, onun katı halden sıvı hale geçtiği sıcaklıktır. 4-etilfenolün erime noktası, düşük moleküler ağırlığı ve güçlü moleküller arası kuvvetlerin bulunmaması nedeniyle nispeten düşüktür.
4-etilfenol g/ml yoğunluğu
4-etilfenolün yoğunluğu 1,02 g/mL’dir. Bir maddenin yoğunluğu birim hacim başına kütlesi olarak tanımlanır. Bir madde numunesinin kütlesinin hacmine bölünmesiyle hesaplanır. 4-etilfenolün yoğunluğu, düşük moleküler ağırlığı ve güçlü moleküller arası kuvvetlerin bulunmaması nedeniyle nispeten düşüktür.
4-etilfenolün moleküler ağırlığı
4-etilfenolün moleküler ağırlığı 134,17 g/mol’dür. Molekül ağırlığı molar kütle ile aynıdır ve moleküldeki tüm elementlerin atomik kütlelerinin eklenmesiyle hesaplanır. 4-etilfenol durumunda, moleküler formülü (C8H10O) bize 134,17 g/mol moleküler ağırlığı verir.
| Dış görünüş | Renksiz sıvı |
| Spesifik yer çekimi | 1.02g/ml |
| Renk | Renksiz |
| Koku | Tatlı, baharatlı ve otsu bir koku |
| Molar kütle | 134,17 gr/mol |
| Yoğunluk | 1.02g/ml |
| Füzyon noktası | 9,7°C |
| Kaynama noktası | 218,7°C |
| Flaş noktası | 100°C |
| sudaki çözünürlük | Çözünür |
| çözünürlük | Organik çözücülerde çözünür |
| Buhar basıncı | 32 mmHg (20°C) |
| Buhar yoğunluğu | 2,4 (hava = 1) |
| pKa | 9.5 |
| pH | Doğal |
4-etilfenolün güvenliği ve tehlikeleri
Yanıcı bir sıvı olduğundan 4-etilfenol’ü ısı ve tutuşma kaynaklarından uzakta saklayın. Doğrudan temas ciltte ve gözde tahrişe neden olabilir ve buharının veya buğusunun solunması solunum yolu tahrişine neden olabilir. 4-etilfenolle çalışırken koruyucu eldiven, koruyucu gözlük ve solunum cihazı takarak kendinizi koruyun. Dikkatli bir şekilde kullanın ve yerel düzenlemelere uygun olarak uygun şekilde atın.
| Tehlike sembolleri | Yanıcı sıvı, tahriş edici |
| Güvenlik Açıklaması | S2: Çocukların ulaşamayacağı yerde saklayın; S24/25: Cilt ve gözlerle temasından kaçının; S36/37/39: Uygun koruyucu kıyafet, eldiven ve göz/yüz koruması kullanın. |
| BM kimlik numaraları | UN 1993, Alevlenir sıvı, NOS (4-etilfenol) |
| HS kodu | 2909.30.90 |
| Tehlike sınıfı | 3 |
| Paketleme grubu | III |
| Toksisite | Oral LD50 (sıçan) = 5.400 mg/kg. Cilt ve göz tahrişine neden olabilir. Buharının veya buğusunun solunması solunum yolu tahrişine neden olabilir. |
4-etilfenol sentezi için yöntemler
4-Etilfenol, fenolün, sodyum hidroksit veya potasyum hidroksit gibi bir alkalin katalizör varlığında etilen oksitle reaksiyonuyla sentezlenir. Reaksiyon 60-80°C sıcaklıkta ve atmosferik basınçta gerçekleşir. Fenolün etilen okside molar oranı, 4-etilfenolün istenen verimine ve saflığına bağlı olarak 1:1 ila 1:2 arasında değişir. Reaksiyon karışımı daha sonra nötrleştirilir ve arzu edilen ürünü elde etmek üzere damıtılır.
Alternatif bir sentez yöntemi, 4-kloro-o-krezolün, sodyum hidroksit veya potasyum hidroksit gibi bir alkalin katalizör varlığında etilen oksitle reaksiyonunu içerir. Reaksiyon 60-80°C sıcaklıkta ve atmosferik basınçta gerçekleşir. 4-kloro-o-kresolün etilen okside molar oranı, 4-etilfenolün istenen verimine ve saflığına bağlı olarak 1:1 ila 1:2 arasında değişir. Reaksiyon karışımı daha sonra nötrleştirilir ve arzu edilen ürünü elde etmek üzere damıtılır.
Her iki yöntemin de istenen 4-etilfenol verimini ve saflığını elde etmek için sıcaklığın, basıncın ve katalizör konsantrasyonunun dikkatli bir şekilde kontrol edilmesini gerektirdiğini belirtmek önemlidir. Nihai ürünün kalitesini sağlamak için reaksiyon karışımı, reaksiyon yan ürünleri veya ham maddelerden kaynaklanan kirletici maddeler gibi yabancı maddelerin varlığı açısından da dikkatle izlenmelidir.
4-etilfenolün kullanımları
Endüstriler, tatlı, baharatlı ve bitkisel kokusu nedeniyle kişisel bakım ve parfüm, sabun, deterjan ve mum gibi ev ürünlerinde koku bileşeni olarak 4-etilfenol’ü yaygın olarak kullanıyor. Gıda endüstrisi, şekerlemelerde, fırınlanmış ürünlerde ve alkollü içeceklerde tatlandırıcı madde olarak 4-etilfenol kullanır. Bir öncü olarak farmasötik ve ince kimya endüstrileri için p-kresol gibi başka bileşikler de üretir.
Üreticiler 4-etilfenol’ü reçinelerin, plastikleştiricilerin ve diğer polimerlerin üretiminde ve ayrıca kauçuk ve sentetik kokuların sentezinde kullanıyorlar. Araştırmacılar ayrıca mantar büyümesi üzerindeki engelleyici etkilerinden dolayı antifungal bir ajan olarak potansiyelini de araştırıyorlar.
Avrupa Birliği, Amerika Birleşik Devletleri Gıda ve İlaç İdaresi ve Uluslararası Koku Birliği gibi düzenleyici kurumlar, güvenli ve sorumlu kullanımını sağlamak için 4-etilfenolün kullanımını düzenler. 4-etilfenolün güvenli kullanımı, potansiyel sağlık ve çevresel etkilerinin yanı sıra uygun kullanım ve depolamanın da dikkatli bir şekilde değerlendirilmesini gerektirir.
Sorular:
Etilfenoller nelerdir?
Etilfenoller, fenol fonksiyonel grubu ve fenol halkasına bağlı bir etil grubu (-C2H5) içeren bir grup organik bileşiktir. Aromatik alkoller olarak sınıflandırılırlar ve fenol halkası üzerindeki etil grubunun konumuna bağlı olarak farklı fiziksel ve kimyasal özelliklere sahiptirler. Etilfenollerin yaygın örnekleri arasında 4-etilfenol ve 2-etilfenol bulunur. Bu bileşiklerin parfüm, gıda ve kimya endüstrilerinde ve ayrıca diğer kimyasalların sentezinde çeşitli kullanımları vardır. Ancak etilfenollerin kullanımı, potansiyel sağlık ve çevresel etkileriyle ilgili endişeler nedeniyle düzenlenmiştir ve güvenli kullanımları, taşıma ve depolama gerekliliklerinin dikkatli bir şekilde değerlendirilmesini gerektirir.
Aşağıdaki spektral verilerle açıklanan bileşiğin yapısı nedir? formül c8h10o
Spektral veriler tek başına bir bileşiğin yapısını kesin olarak belirleyemez ancak onu tanımlamak için bilgi sağlayabilir. C8H10O formülü, bileşiğin aromatik bir alkol olduğunu ileri sürer; bu, IR spektrumunda bir OH zirvesiyle gösterilen bir alkol fonksiyonel grubunun varlığıyla doğrulanabilir.
1H NMR spektrumu, aromatik hidrojenlerin ve alifatik hidrojenlerin yanı sıra herhangi bir fonksiyonel grubun varlığı gibi moleküldeki hidrojen atomlarının sayısı ve türü hakkında bilgi sağlayabilir. 13C NMR spektrumu aynı zamanda molekülde bulunan karbon atomlarının türü ve bunların ortamı hakkında da bilgi sağlayabilir.
Bu bilgiye dayanarak bileşiğin yapısını çıkarmak mümkündür ancak bunu kesin olarak doğrulamak için ek bilgi ve analize ihtiyaç duyulacaktır. C8H10O formülüne sahip bir bileşik için bazı olası yapılar, diğerlerinin yanı sıra fenol, kresol veya ksilenolleri içerebilir.
Sizce c8h10o kimyasal formülüyle temsil edilen NMR spektrumunun yapısı nedir?
Aromatik alkol olarak C8H10O kimyasal formülüne sahip bir molekülün olası yapısını belirleyebilirsiniz. 1H NMR spektrumunda hidroksil proton için tekli veya ikili bir sinyal ve aromatik proton sinyali için birkaç tepe görmeyi beklersiniz. 13C NMR spektrumunda aromatik halkanın karbonlarına ve karbonil grubuna yönelik sinyalleri görüyorsunuz.
Çevre, solvent ve molekül konsantrasyonunun yanı sıra safsızlıklar veya izomerler gibi çeşitli faktörler NMR spektrumlarını etkileyebilir. Molekülün yapısını kesin olarak belirlemek için, gerçek NMR spektrumunu analiz etmeli ve yorumlamalısınız, ancak kimyasal formüle dayalı bir tahminde bulunabilirsiniz.
C8h10o’nun doymamışlık derecesi nasıl hesaplanır?
Bir molekülün doymamışlık derecesi aşağıdaki formül kullanılarak hesaplanabilir:
Doymamışlık derecesi = (2 + halka sayısı) + (çift bağ sayısı / 2)
C8H10O formülüne sahip molekülün aromatik bir halka olması nedeniyle tek bir halkası vardır. Molekülün alkol olması ve çift bağ içermemesi nedeniyle çift bağ yoktur.
Bu nedenle C8H10O için doymamışlık dereceleri şu şekilde hesaplanacaktır:
Doymamışlık dereceleri = (2 + 1) + (0/2) = 3
Bu sonuç, C8H10O molekülünün üç derece doymamışlığa sahip olduğunu ve bu nedenle aromatik bir alkol olma ihtimalinin yüksek olduğunu gösterir. Doymamışlık derecelerinin hesaplanması, bir bileşiğin moleküler yapısını tahmin etmek ve doymamış fonksiyonel gruplar veya halkalar içerip içermediğini belirlemek için hızlı ve kullanışlı bir yol sağlar. Ancak bu yöntemin bazı sınırlamaları olduğu ve her bileşik için uygun olmadığı unutulmamalıdır.
c8h10o nedir?
C8H10O, 8 karbon atomu, 10 hidrojen atomu ve 1 oksijen atomu içeren bir molekülün kimyasal formülüdür. Molekül, diğerlerinin yanı sıra fenol, kresol veya ksilenol gibi aromatik alkoller de dahil olmak üzere birçok farklı kimyasal bileşikten biri olabilir.
Kızılötesi spektroskopi, nükleer manyetik rezonans spektroskopisi veya kütle spektrometrisi gibi teknikler, moleküler yapısına ve özelliklerine bağlı olarak molekülün gerçek kimliğini belirler.
