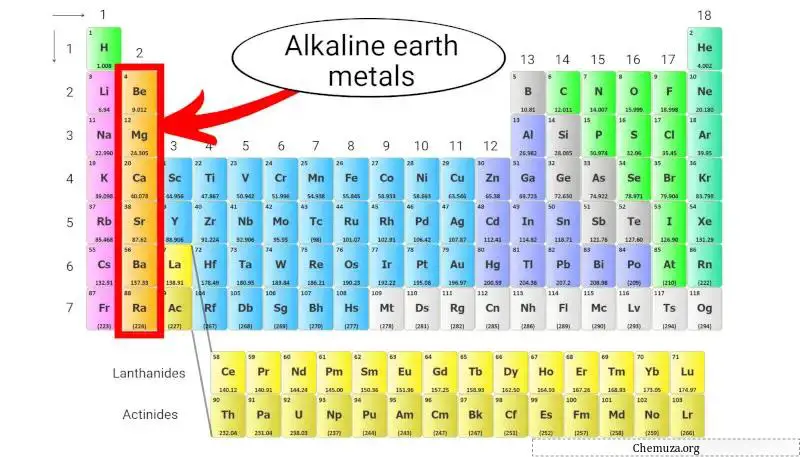
Alkali toprak metaller periyodik tablonun ikinci sütununda yer alan bir grup elementtir. Berilyum (Be), magnezyum (Mg), kalsiyum (Ca), stronsiyum (Sr), baryum (Ba) ve radyum (Ra) içerir.
Bu metallerin en dış kabuklarında iki elektron bulunur; bu da onları kimyasal olarak reaktif kılar ancak ilk sütunda yer alan alkali metaller kadar reaktif değildir.
Periyodik tablodaki alkali toprak metalleri hakkında daha fazlasını keşfedelim.
Alkali toprak metalleri nelerdir?

Alkali toprak metaller periyodik tablonun 2. grubunun bir parçasıdır ve iki özel özelliğe sahiptir.
- Su ile reaksiyona girdiklerinde alkali veya bazik nitelikte hidroksitler üretirler.
- Oksit mineralleri (BeO, manyezit, MgO, beril vb.) esas olarak yer kabuğunda bulunur ve ısıya karşı dayanıklıdır.
Açıklama
Toprak alkali metaller (Mg, Ca, Sr, Ba ve Ra) suyla reaksiyona girdiğinde alkali (veya bazik) nitelikte hidroksitler oluştururlar. [2]
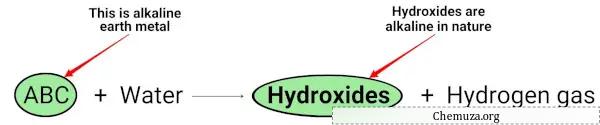
Yukarıdaki kimyasal denklemde alkali metallerin doğada bazik olan (pH> 7 olan) hidroksitler verdiğini ve hidrojen gazı açığa çıkardığını görebilirsiniz.
Örneğin:
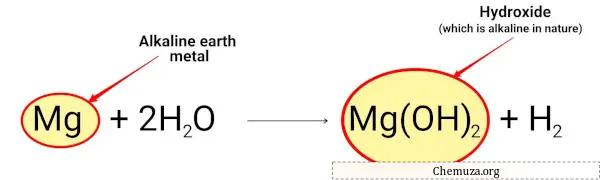
Magnezyum su ile reaksiyona girerek alkali yapıda olan magnezyum hidroksiti oluşturur.
Ek olarak, bu metaller öncelikle yer kabuğunda (oksitler halinde) bulunur ve bu oksitlenmiş mineraller ısıya dayanıklıdır. [2]
Bu iki kriter bu metallere “toprak alkali metaller” adını verir.
(Not: Aynı zamanda Grup 2 elementi olan berilyumun suyla reaksiyona girdiğinde alkali bir çözelti oluşturmadığını belirtmek önemlidir. Bunun yerine hidroksitleri amfoterik davranış sergiler, bu da asit veya baz gibi davranabilecekleri anlamına gelir. Bu nedenle berilyum aynı gruba ait olmasına rağmen toprak alkali metal sayılmaz.)
Tüm alkali toprak metallerinde ortak olan nedir?
Alkali toprak metalleri birçok ortak özelliğe sahiptir.
Örneğin her ikisinin de en dış enerji seviyelerinde iki değerlik elektronu vardır, bu da onları oldukça reaktif kılar.
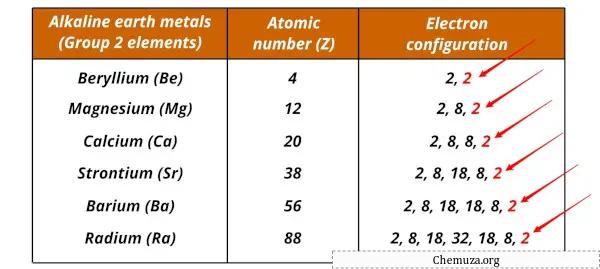
Bu reaktivite, kimyasal reaksiyonlar sırasında bu elektronları kaybetme eğilimi nedeniyle +2 yüklü katyonların oluşumuyla sonuçlanır.
Ayrıca tüm alkalin toprak metalleri parlak, gümüşi beyaz bir görünüme sahiptir.

Yani bunlar alkalin toprak metallerinin iki ana ortak noktasıdır.
Alkali metallerin listesi ve elektronik konfigürasyonları
Alkali toprak metaller ve elektronik konfigürasyonları aşağıda gösterilmiştir.
| Öğe | Elektronik konfigürasyon |
| Berilyum (Be) | [O] 2s 2 |
| Magnezyum (Mg) | [Yap] 3s 2 |
| Kalsiyum (Ca) | [Ar] 4s 2 |
| Stronsiyum (Sr) | [Kr] 5s 2 |
| Baryum (Ba) | [Xe] 6s 2 |
| Radyum (Ra) | [Rn] 7s 2 |
Alkali Toprak Metallerdeki Periyodik Eğilimler
Periyodik tablonun alkali toprak metal grubunda aşağıya doğru gidildikçe aşağıdaki eğilimler gözlemlenebilir:
- Değerlik: Tüm alkalin toprak metalleri aynı +2 değerine sahiptir. Yani grupta aşağıya doğru inildikçe değerlikte bir değişiklik olmaz.
- Atom büyüklüğü: Alkali toprak metallerin atom büyüklüğü grupta aşağıya doğru inildikçe artar. Bunun nedeni, elektronik katmanların (veya yörüngelerin ) sayısının artması ve iç elektronların koruyucu etkisinin, çekirdek ile en dıştaki elektronlar arasındaki çekimin azalmasıdır.
- Metalik Karakter: Toprak alkali metallerin metalik karakteri grupta aşağıya doğru gidildikçe artar. Bunun nedeni, atomların büyümesi ve daha fazla elektron içermesi, böylece elektronları daha kolay kaybetmeleri ve pozitif iyonlar oluşturmalarıdır.
- Elektronegatiflik: Toprak alkali metallerin elektronegatifliği grupta aşağı doğru inildikçe azalır. Bunun nedeni, atomların büyümesi ve daha fazla elektron kabuğuna sahip olması, elektronları kendilerine çekmelerinin daha zor hale gelmesidir.
- Elektronik Afinite: Toprak alkali metallerin elektronik afinitesi genellikle düşüktür ve grupta aşağı doğru gidildikçe azalır.
- İyonlaşma Enerjisi: Toprak alkali metallerin iyonlaşma enerjisi grupta aşağıya doğru inildikçe azalır. Bunun nedeni, daha büyük atomların daha fazla elektron kabuğuna sahip olması ve en dıştaki elektronların çekirdekten daha uzakta olması ve bunların uzaklaştırılmasının daha kolay olmasıdır.
Özet
Alkali toprak metalleri arasında berilyum, magnezyum, kalsiyum, stronsiyum, baryum ve radyum bulunur. En dış kabuklarında iki elektron bulunur, bu da onları reaktif yapar ancak alkali metallerden daha az reaktif yapar.
Bu metaller suyla reaksiyona girdiklerinde alkali hidroksitler üretirler ve ısıya dayanıklı oksitlenmiş mineraller içerirler. Tüm alkalin toprak metallerinin ortak temel özellikleri, iki değerlik elektronuna sahip olmaları, gümüşi beyaz ve parlak olmaları ve +2 yüklü katyonlar oluşturmalarıdır.
Grupta aşağıya doğru gidildikçe değerlik aynı kalır, ancak atom boyutu ve metalik karakter artarken elektronegatiflik, elektron ilgisi ve iyonlaşma enerjisi azalır.
