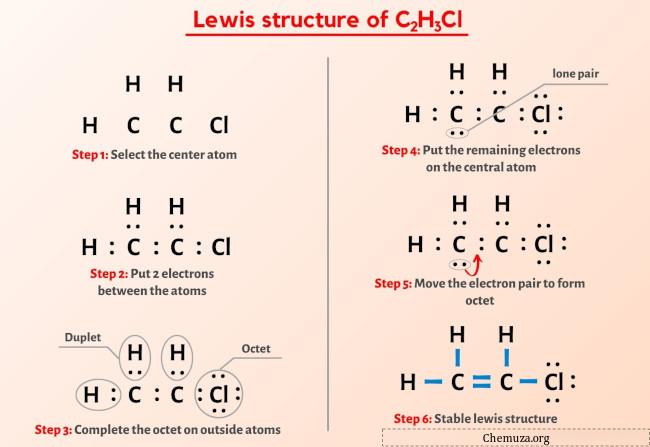
Yukarıdaki görseli zaten gördünüz değil mi?
Yukarıdaki görseli kısaca açıklayayım.
Lewis yapısı C2H3Cl, karbon-karbon atomları arasında bir çift bağa ve karbon-hidrojen atomları ile karbon-klor atomları arasında tek bir bağa sahiptir. Klor (Cl) atomunda 3 yalnız çift vardır.
C2H3Cl’nin Lewis yapısının yukarıdaki görüntüsünden hiçbir şey anlamadıysanız, benimle kalın ve C2H3Cl’nin Lewis yapısının çizilmesine ilişkin ayrıntılı adım adım açıklamayı alacaksınız.
O halde C2H3Cl’nin Lewis yapısını çizme adımlarına geçelim.
C2H3Cl’nin Lewis Yapısını Çizim Adımları
Adım 1: C2H3Cl molekülündeki toplam değerlik elektronu sayısını bulun
Bir C2H3Cl molekülündeki değerlik elektronlarının toplam sayısını bulmak için öncelikle karbon atomunda, hidrojen atomunda ve klor atomunda bulunan değerlik elektronlarını bilmeniz gerekir.
(Değerlik elektronları herhangi bir atomun en dış yörüngesinde bulunan elektronlardır.)
Burada size periyodik tabloyu kullanarak karbon, hidrojen ve klorun değerlik elektronlarını nasıl kolayca bulacağınızı anlatacağım.
C2H3Cl molekülündeki toplam değerlik elektronları
→ Karbon atomunun verdiği değerlik elektronları:
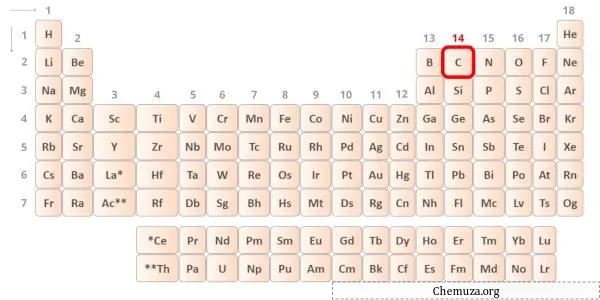
Karbon periyodik tablonun 14. grubunda yer alan bir elementtir. [1] Bu nedenle karbonda bulunan değerlik elektronları 4’tür .
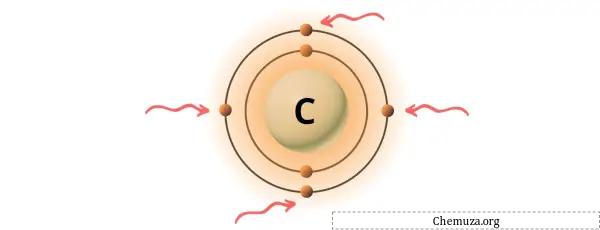
Yukarıdaki resimde gösterildiği gibi karbon atomunda bulunan 4 değerlik elektronunu görebilirsiniz.
→ Hidrojen atomunun verdiği değerlik elektronları:
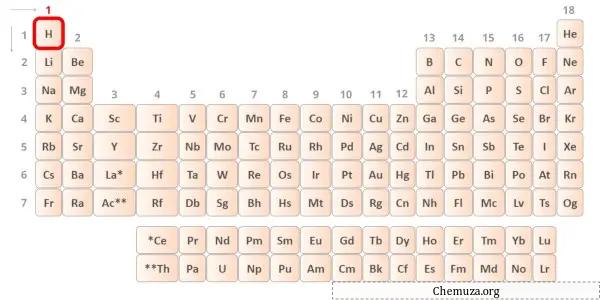
Hidrojen periyodik tablonun 1. grup elementidir. [2] Bu nedenle hidrojende bulunan değerlik elektronu 1’dir .

Yukarıdaki resimde gösterildiği gibi hidrojen atomunda yalnızca bir değerlik elektronunun bulunduğunu görebilirsiniz.
→ Klor atomunun verdiği değerlik elektronları:

Klor periyodik tablonun 17. grubunda yer alan bir elementtir. [3] Bu nedenle klorda bulunan değerlik elektronları 7’dir .
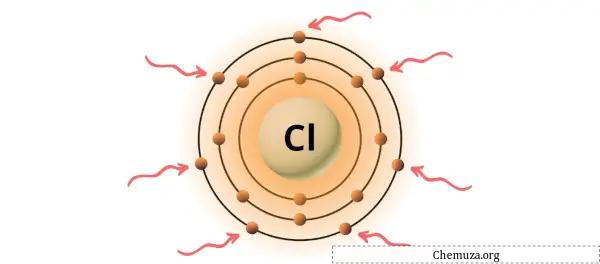
Yukarıdaki resimde gösterildiği gibi klor atomunda bulunan 7 değerlik elektronunu görebilirsiniz.
Bu yüzden,
C2H3Cl molekülündeki toplam değerlik elektronları = 2 karbon atomu tarafından bağışlanan değerlik elektronları + 3 hidrojen atomu tarafından bağışlanan değerlik elektronları + 1 klor atomu tarafından bağışlanan değerlik elektronları = 4(2) + 1(3) + 7 = 18 .
Adım 2: Merkez atomu seçin
Merkez atomu seçmek için en az elektronegatif atomun merkezde kaldığını unutmamalıyız.
(Unutmayın: eğer verilen molekülde hidrojen varsa, daima hidrojeni dışarıya koyun.)
Şimdi burada verilen molekül C2H3Cl’dir ve karbon atomu (C), hidrojen atomları (H) ve klor atomu (Cl) içerir.
Yani kurala göre hidrojeni dışarıda tutmalıyız.
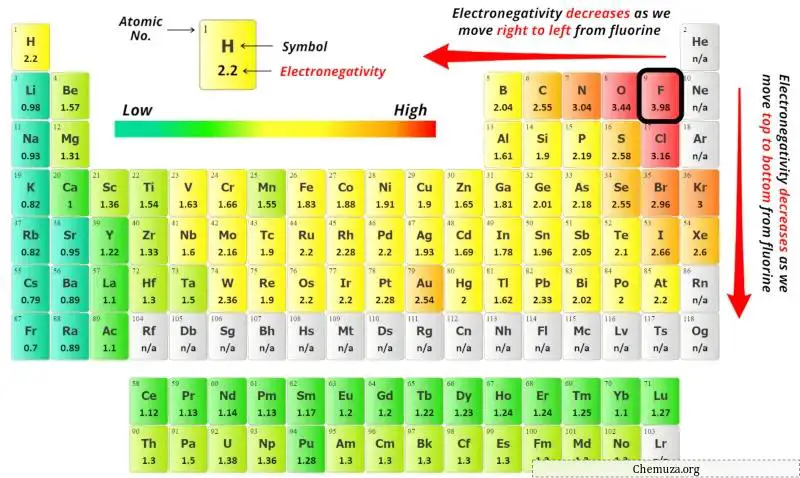
Artık yukarıdaki periyodik tabloda karbon (C) atomu ve klor (Cl) atomunun elektronegatiflik değerlerini görebilirsiniz.
Karbon (C) ve klorun (Cl) elektronegatiflik değerlerini karşılaştırırsak, karbon atomu daha az elektronegatiftir.
Burada karbon (C) atomu merkez atom, klor (Cl) atomu ise dış atomdur.

Adım 3: Her atomu aralarına bir çift elektron yerleştirerek bağlayın
Şimdi C2H3Cl molekülünde elektron çiftlerini karbon (C) ve klor (Cl) atomları arasına ve karbon (C) ve hidrojen (H) atomları arasına yerleştirmeniz gerekiyor.
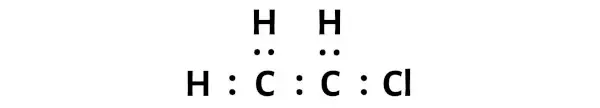
Bu, bu atomların bir C2H3Cl molekülünde birbirine kimyasal olarak bağlandığını gösterir.
Adım 4: Dış Atomları Kararlı Hale Getirin
Bu adımda dış atomların kararlılığını kontrol etmeniz gerekir.
Burada C2H3Cl molekülünün çiziminde dıştaki atomların hidrojen atomları ve klor atomları olduğunu görebilirsiniz.
Bu hidrojen ve klor atomları sırasıyla bir ikili ve bir oktet oluşturur ve bu nedenle stabildir.
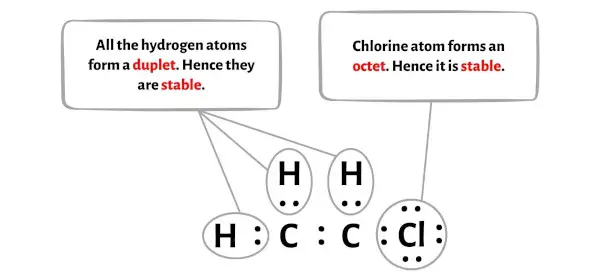
Ek olarak 1. adımda C2H3Cl molekülünde bulunan toplam değerlik elektron sayısını hesapladık.
C2H3Cl molekülünde toplam 18 değerlik elektronu vardır ve yukarıdaki diyagramda bunlardan sadece 16 değerlik elektronu kullanılmıştır.
Yani kalan elektron sayısı = 18 – 16 = 2 .
Bu 2 elektronu yukarıdaki diyagramda C2H3Cl molekülünün karbon atomlarından birinin üzerine yerleştirmeniz gerekiyor.
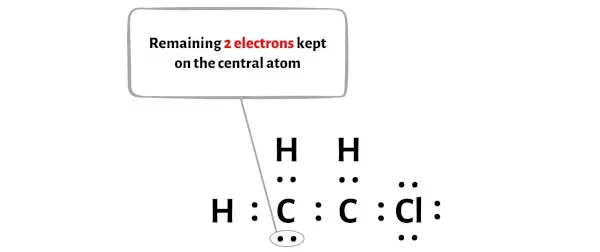
Şimdi bir sonraki adıma geçelim.
Adım 5: Merkezi atomdaki sekizliyi kontrol edin. Okteti yoksa yalnız çifti çift bağ veya üçlü bağ oluşturacak şekilde hareket ettirin.
Bu adımda merkezi karbon atomlarının (C) kararlı olup olmadığını kontrol etmeniz gerekir.
Merkezi karbon (C) atomlarının kararlılığını kontrol etmek için bunların bir oktet oluşturup oluşturmadığını kontrol etmemiz gerekir.
Maalesef karbon atomlarından biri burada bir oktet oluşturmuyor.
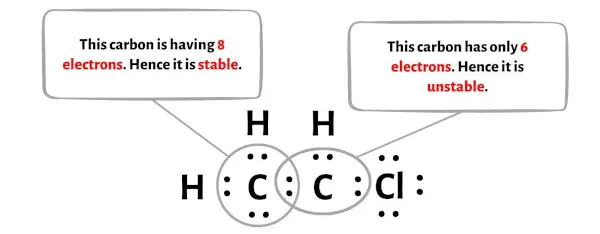
Şimdi, bu karbon atomunu kararlı hale getirmek için, yalnız çifti bir çift bağa dönüştürmeniz gerekir, böylece karbon atomu 8 elektrona (yani bir oktete) sahip olabilir.
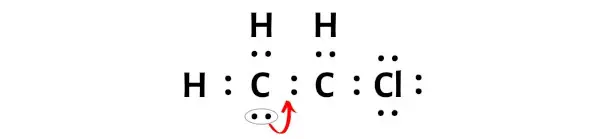
Bu elektron çifti ikili bağa dönüştürüldükten sonra merkezi karbon atomu 2 elektron daha alacak ve böylece toplam elektron sayısı 8 olacaktır.
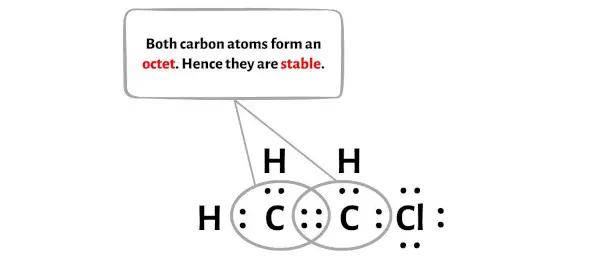
Yukarıdaki resimde iki karbon atomunun bir oktet oluşturduğunu görebilirsiniz.
Ve böylece bu karbon atomları kararlıdır.
Şimdi C2H3Cl’nin Lewis yapısının kararlı olup olmadığını kontrol etmek için son adıma geçelim.
Adım 6: Lewis yapısının kararlılığını kontrol edin
Artık C2H3Cl’nin Lewis yapısının stabilitesini kontrol etmeniz gereken son adıma geldiniz.
Lewis yapısının kararlılığı formal yük kavramı kullanılarak doğrulanabilir.
Kısacası artık C2H3Cl molekülünde bulunan karbon (C), hidrojen (H) ve klor (Cl) atomlarının formal yükünü bulmamız gerekiyor.
Resmi vergiyi hesaplamak için aşağıdaki formülü kullanmanız gerekir:
Resmi yük = Değerlik elektronları – (Bağ elektronları)/2 – Bağ yapmayan elektronlar
Aşağıdaki resimde C2H3Cl molekülünün her bir atomu için bağlanan elektronların ve bağlanmayan elektronların sayısını görebilirsiniz.
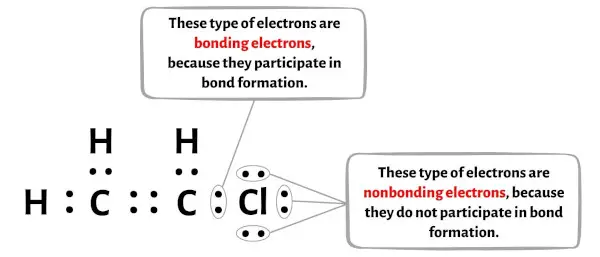
Karbon atomu (C) için:
Değerlik elektronları = 4 (çünkü karbon 14. gruptadır)
Bağ elektronları = 8
Bağlanmayan elektronlar = 0
Hidrojen atomu (H) için:
Değerlik elektronu = 1 (çünkü hidrojen grup 1’dedir)
Bağ elektronları = 2
Bağlanmayan elektronlar = 0
Klor atomu (Cl) için:
Değerlik elektronları = 7 (çünkü klor 17. gruptadır)
Bağ elektronları = 2
Bağlanmayan elektronlar = 6
| Resmi suçlama | = | değerlik elektronları | – | (Elektronların bağlanması)/2 | – | Bağlanmayan elektronlar | ||
| VS | = | 4 | – | 8/2 | – | 0 | = | 0 |
| H | = | 1 | – | 2/2 | – | 0 | = | 0 |
| Cl | = | 7 | – | 2/2 | – | 6 | = | 0 |
Yukarıdaki formal yük hesaplamalarından, karbon atomunun (C), hidrojen atomunun (H) ve klor atomunun (Cl) “sıfır” formal yüke sahip olduğunu görebilirsiniz.
Bu, C2H3Cl’nin yukarıdaki Lewis yapısının stabil olduğunu ve C2H3Cl’nin yukarıdaki yapısında başka bir değişiklik olmadığını gösterir.
C2H3Cl’nin yukarıdaki Lewis nokta yapısında, her bir bağ elektronu çiftini (:) tek bir bağ (|) olarak da temsil edebilirsiniz. Bunu yapmak C2H3Cl’nin aşağıdaki Lewis yapısına yol açacaktır.
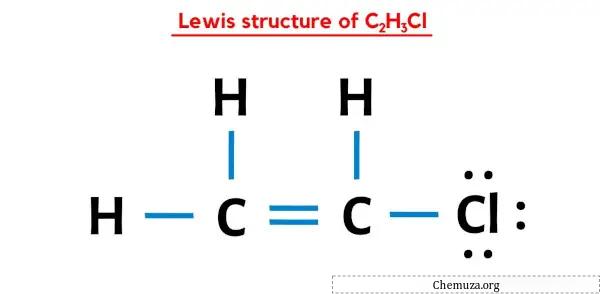
Umarım yukarıdaki tüm adımları tamamen anlamışsınızdır.
Daha fazla pratik yapmak ve daha iyi anlamak için aşağıda listelenen diğer Lewis yapılarını deneyebilirsiniz.
Daha iyi anlamak için şu Lewis yapılarını deneyin (veya en azından görün):
