Çinko klorür (ZnCl2) beyaz kristalli bir bileşiktir. Lehimleme fluxları, kimyasal sentez ve galvanizleme gibi çeşitli endüstriyel uygulamalarda kullanılır. Suda çok çözünür.
| IUPAC Adı | Çinko Klorür |
| Moleküler formül | ZnCl2 |
| CAS numarası | 7646-85-7 |
| Eş anlamlı | Çinko yağı; Çinko diklorür; Çinko(II) klorür; Çinko yağı; CI77043 |
| InChI | InChI=1S/2ClH.Zn/h2*1H;/q;;+2/p-2 |
Çinko klorürün özellikleri
Çinko Klorür Formülü
Çinko diklorürün kimyasal formülü ZnCl2’dir. Bir çinko atomu (Zn) ve iki klor atomundan (Cl) oluşur. Bu iyonik bileşik, farklı bir yapıya sahip beyaz kristalli bir katı oluşturur.
Çinko Klorür Molar Kütlesi
Çinko diklorürün molar kütlesi mol başına yaklaşık 136,29 gramdır (g/mol). Bir çinko atomu ve iki klor atomunun atomik kütlelerinin toplamından türetilir.
Çinko klorürün kaynama noktası
Çinko diklorürün yaklaşık 732 santigrat derece (C) veya 1.350 Fahrenheit (F) civarında nispeten yüksek bir kaynama noktası vardır. Bu sıcaklıkta sıvı halden gaz haline geçer.
Çinko klorürün erime noktası
Çinko diklorürün erime noktası yaklaşık 290 santigrat derece (C) veya 554 Fahrenheit derecedir (F). Bu sıcaklıkta katı çinko diklorür sıvı duruma geçer.
Çinko klorür yoğunluğu g/mL
Çinko diklorürün yoğunluğu, oda sıcaklığında mililitre başına yaklaşık 2,91 gramdır (g/mL). Bu özellik birim hacim başına kütlesini açıklar.
Çinko Klorür Molekül Ağırlığı
Çinko diklorürün kimyasal formülünden hesaplanan moleküler ağırlığı yaklaşık 136,29 g/mol’dür. Bu değer, onu oluşturan atomların atom ağırlıklarının toplamını temsil eder.
Çinko klorürün yapısı
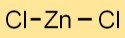
Çinko diklorür, iyonik bağlarla bir arada tutulan Zn2+ katyonları ve Klanyonlardan oluşan bir kristal kafes yapısına sahiptir. Düzenleme istikrarlı ve düzenli bir üç boyutlu ağ oluşturur.
Çinko klorürün çözünürlüğü
Çinko diklorür suda çok çözünür, yani su moleküllerinin varlığında kolayca çözünür. Bu özellik, çeşitli endüstriyel uygulamalarda ve kimyasal işlemlerde yaygın kullanımına katkıda bulunur.
| Dış görünüş | Beyaz kristal katı |
| Spesifik yer çekimi | 2,91 gr/ml |
| Renk | Renksiz |
| Koku | Kokusuz |
| Molar kütle | 136,29 gr/mol |
| Yoğunluk | 2,91 gr/cm³ |
| Füzyon noktası | 290°C (554°F) |
| Kaynama noktası | 732°C (1350°F) |
| Flaş noktası | Uygulanamaz |
| sudaki çözünürlük | Suda çok çözünür |
| çözünürlük | Alkol ve aseton gibi organik çözücülerde çözünür |
| Buhar basıncı | 359°C’de 1 mmHg |
| Buhar yoğunluğu | 5,4 (hava = 1) |
| pKa | -1,9 |
| pH | ~5 (suda 0,1 M çözelti) |
Çinko klorürün güvenliği ve tehlikeleri
Çinko diklorür dikkatli kullanım gerektiren belirli güvenlik riskleri oluşturur. Cilt veya gözlerle doğrudan temas tahrişe ve yanıklara neden olabilir. Buharlarının solunması solunum sistemini tahriş edebilir. Bileşiği kullanırken eldiven ve gözlük gibi koruyucu ekipman giymek önemlidir. Ayrıca iyi havalandırılmış, uyumsuz maddelerden uzak bir alanda saklanmalıdır. Yutulması veya kazara maruz kalması durumunda derhal tıbbi yardıma başvurun. Sudaki yaşama zararlı olabileceğinden çevreye salınmasından kaçının. Uygun güvenlik önlemleri ve yönergeleri takip ederek çinko diklorürle ilişkili riskler etkili bir şekilde en aza indirilebilir.
| Tehlike sembolleri | Aşındırıcı (C); Zararlı (Xn) |
| Güvenlik Açıklaması | Cilt ve gözlerle temasından kaçının. İyi havalandırılan bir ortamda kullanınız. Eldiven ve koruyucu gözlük takın. Temas veya yutulması halinde doktora başvurunuz. Çevreye salmayın. Uyumsuz maddelerden uzak tutun. |
| BM kimlik numaraları | UN No. 2331 (Susuz çinko diklorür); UN No. 2332 (Çinko diklorür, çözelti) |
| HS kodu | 28273990 |
| Tehlike sınıfı | 8 (Aşındırıcı maddeler) |
| Paketleme grubu | II (Orta tehlike) |
| Toksisite | Yutulması veya solunması halinde zararlıdır. |
Çinko klorür sentezi için yöntemler
Çeşitli yöntemler çinko diklorürün sentezine izin verir.
Yaygın bir yaklaşım çinko oksidin (ZnO) hidroklorik asit (HCl) ile reaksiyonunu içerir. Bu yöntemde bir kimyager, sürekli karıştırarak bir HCl çözeltisine yavaş yavaş ZnO ekler. Reaksiyon yan ürün olarak çinko diklorür ve su üretir. Diğer bir yöntem ise çinko metalini doğrudan klor gazı (Cl2) ile birleştirmektir. Bu reaksiyon, başarılı bir sonuç elde etmek için sıcaklığın ve basıncın dikkatli bir şekilde kontrol edilmesini gerektirir.
Alternatif bir işlem, çinko metalinin bir HC1 çözeltisi içinde çözülmesini içerir ve bunun sonucunda çinko diklorür ve hidrojen gazı (H2) oluşur. HCl’nin çinko karbonat (ZnCO3) veya çinko hidroksit (Zn(OH)2) ile işlenmesi, yan ürünler olarak çinko diklorür, su ve karbon dioksit (CO2) üretir.
Çinko sülfat (ZnSO4) ve baryum klorür (BaCl2), çinko diklorürün yanı sıra baryum sülfatın (BaSO4) oluşmasını sağlamak üzere çift ayrışma reaksiyonuna girer. Bu iki bileşiğin karıştırılmasıyla çinko diklorür çöker, baryum sülfat (BaSO4) ise çözeltide kalır.
Bu yöntemlerin her biri, çinko diklorürün sentezi için bir yol sağlar ve yöntemin seçimi, reaktiflerin mevcudiyeti, reaksiyon koşulları ve nihai ürünün istenen saflığı gibi faktörlere bağlıdır.
Çinko Klorürün Kullanım Alanları
Çinko diklorür, çok yönlü özelliklerinden dolayı çeşitli endüstrilerde geniş bir uygulama alanı bulmaktadır. Çinko diklorürün bazı önemli kullanım alanları şunlardır:
- Galvanizleme: Çinko diklorür, çelik ve demir gibi metallerin korozyonunu önlemek için galvanizleme işleminde önemli bir rol oynar. Koruyucu bir çinko kaplama oluşturarak ömrünü ve dayanıklılığını artırır.
- Lehimleme Akısı: Lehimleme operasyonlarında çinko diklorür, metal oksitleri metallerin yüzeyinden çıkarmak için bir fluks görevi görerek lehim ile metal arasında daha iyi yapışma ve güçlü bir bağ sağlar.
- Kimyasal sentez: Asilasyon ve Friedel-Crafts dehidrasyonu gibi birçok kimyasal reaksiyonda katalizör veya reaktif olarak görev yapar.
- Ahşabın Korunması: Ahşap koruyucu uygulamalarında ahşabı mantar çürümesinden ve böceklerden korumak ve ömrünü uzatmak için çinko diklorür kullanılır.
- Tekstil İşleme: Tekstil endüstrisinde, merserize pamuklu kumaşların üretimini kolaylaştırarak, artan parlaklık ve geliştirilmiş mukavemet gibi arzu edilen özellikleri kazandırır.
- Pil elektroliti: Çinko diklorür, çinko-karbon pil gibi bazı pillerde elektrolit görevi görerek elektrotlar arasındaki iyon akışını kolaylaştırmaya yardımcı olur.
- Deodorant ve terlemeyi önleyici: Ter üretimini azaltmaya ve vücut kokusunu kontrol etmeye yardımcı olan büzücü özellikleri nedeniyle terlemeyi önleyicilerde yaygın olarak kullanılan bir bileşendir.
- Farmasötikler: Çinko diklorür, çeşitli farmasötik formülasyonlarda, özellikle ağız gargaralarında, boğaz pastillerinde ve topikal antiseptik solüsyonlarda uygulama alanı bulur.
- Boyama Endüstrisi: Boya endüstrisi, kumaşların boyalarla renk haslığını arttırmak için boyama işleminde mordan olarak çinko diklorürü kullanır.
- Yapıştırıcı formülasyonları: Üreticiler, yapıştırıcıların ve çimentoların bağlanma özelliklerini geliştirmek için yapıştırıcı formülasyonlarına çinko diklorür katarlar.
Çinko diklorürün çok yönlülüğü, onu birçok endüstriyel süreçte ve günlük ürünlerde önemli bir bileşik haline getirerek birçok önemli endüstrinin ilerlemesine katkıda bulunur.
Sorular:
S: ZnCl2 suda çözünür mü?
C: Evet, ZnCl2 suda oldukça çözünür.
S: ZnCl2’nin NaOH ile reaksiyonunun net iyonik denklemi nedir?
A: Net iyonik denklem Zn²⁺(aq) + 2OH⁻(aq) → Zn(OH)₂(s)’dir.
S: ZnCl2 çözünür mü?
C: Evet, ZnCl2 suda çözünür.
S: ZnCl2 iyonik mi yoksa moleküler mi?
C: ZnCl2 iyonik bir bileşiktir.
S: Çinko(II) klorür, ZnCl2’de ne tür bir bağ oluşur?
C: ZnCl2’de iyonik bağ oluşur.
S: Hangi değişiklik ZnCl2 üretim oranını azaltabilir?
C: Reaksiyon sıcaklığının düşürülmesi ZnCl2 üretim hızını azaltabilir.
S: ZnCl2 katı mıdır?
C: Evet, ZnCl2 oda sıcaklığında katıdır.
S: ZnCl2 bir tuz mudur?
C: Evet, ZnCl2 bir tuz olarak kabul edilir.
S: Çinkodan çinko klorürü nasıl elde edeceksiniz?
C: Çinkonun hidroklorik asitle reaksiyonu çinko klorür üretecektir.
S: Çinko klorürün formülü nedir?
C: Çinko klorürün formülü ZnCl2’dir.
Soru: Çinko klorür piller dünyaya zararlı mıdır?
C: Evet, çinko klorür piller uygun şekilde atılmadığı takdirde çevreye zararlı olabilir.
S: Çinko klorürün molar kütlesi nedir?
A: Çinko klorürün molar kütlesi yaklaşık 136,29 g/mol’dür.
