Nikel nitrat (Ni(NO₃)₂), nikel ve nitrat iyonlarını içeren kimyasal bir bileşiktir. Suda çözünür ve sıklıkla katalizörlerde, elektrokaplamada ve diğer nikel bileşiklerinde öncü olarak kullanılır.
| IUPAC Adı | Nikel Dinitrat |
| Moleküler formül | Ni(NO₃)₂ |
| CAS numarası | 13138-45-9 |
| Eş anlamlı | Nikel (II) nitrat, nikel nitrat, Dinitronickel, nikel bis(nitrat) |
| InChI | InChI=1S/2NO3.Ni/c2 2-1(3)4;/q2 -1;+2 |
Nikel nitratın özellikleri
Nikel Nitrat Formülü
Nikel dinitratın kimyasal formülü Ni(NO₃)₂’dir. Nikel katyonları (Ni) ve nitrat anyonlarından (NO₃) oluşan bir bileşiği temsil eder. Formüldeki “2” alt indisi her Ni+2 katyonu için iki NO3- iyonunun bulunduğunu belirtir.
Nikel Nitrat Molar Kütlesi
Nikel dinitratın molar kütlesi, onu oluşturan elementlerin atomik kütleleri toplanarak hesaplanabilir. Nikel (Ni) yaklaşık 58,69 g/mol molar kütleye sahipken nitrat (NO₃) yaklaşık 62,00 g/mol molar kütleye sahiptir. Bunları bir araya topladığımızda nikel dinitratın molar kütlesi yaklaşık 182,69 g/mol olur.
Nikel nitratın kaynama noktası
Nikel dinitratın kaynama noktası, sıvıdan gaza dönüştüğü sıcaklığı ifade eder. Nikel dinitratın kaynama noktası yaklaşık 136,7 santigrat derecedir (278,06 Fahrenheit derece). Ancak bu değerin bileşiğin saflığına bağlı olarak biraz değişebileceğini unutmamak gerekir.
Nikel Nitrat Erime Noktası
Nikel dinitratın erime noktası, katı halden sıvı duruma geçtiği sıcaklıktır. Nikel dinitratın erime noktası yaklaşık 56,7 santigrat derecedir (134,06 Fahrenheit derece). Kaynama noktası gibi erime noktası da bileşiğin saflığından etkilenebilir.
Nikel nitratın yoğunluğu g/mL
Nikel dinitratın yoğunluğu, birim hacim başına kütlesinin bir ölçüsüdür. Nikel dinitratın yoğunluğu yaklaşık 1,68 g/mL’dir. Bu değer yoğunluğu 1 g/mL olan sudan daha yoğun olduğunu gösterir.
Nikel Nitrat Molekül Ağırlığı
Nikel dinitratın moleküler ağırlığı, kimyasal formülünde bulunan tüm atomların atom ağırlıklarının toplamıdır. Daha önce de belirtildiği gibi nikel dinitratın moleküler ağırlığı yaklaşık 182,69 g/mol’dür.
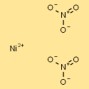
Nikel nitratın yapısı
Nikel dinitratın yapısı, katyon başına iki nitrat anyonu (NO₃⁻) ile çevrelenmiş nikel katyonları (Ni²⁺) olarak görselleştirilebilir. Nitrat iyonları, nikel katyonlarıyla koordineli bağlar oluşturarak kararlı bir iyonik bileşik oluşturur.
Nikel nitratın çözünürlüğü
Nikel dinitrat suda çok çözünür ve berrak yeşilimsi mavi bir çözelti oluşturur. Suda çözünürlüğü önemli bir özelliktir çünkü katalizörler, elektrokaplama ve diğer nikel bileşiklerinin üretimi gibi çeşitli uygulamalarda kolaylıkla kullanılmasına olanak sağlar.
| Dış görünüş | Yeşilimsi mavi katı |
| Spesifik yer çekimi | 1.68g/ml |
| Renk | yeşilimsi mavi |
| Koku | Kokusuz |
| Molar kütle | 182,69 gr/mol |
| Yoğunluk | 1.68g/ml |
| Füzyon noktası | 56,7°C |
| Kaynama noktası | 136,7°C |
| Flaş noktası | Uygulanamaz |
| sudaki çözünürlük | Çok çözünür |
| çözünürlük | Suda ve etanol gibi organik çözücülerde çözünür |
| Buhar basıncı | Müsait değil |
| Buhar yoğunluğu | Müsait değil |
| pKa | Müsait değil |
| pH | Nötr (7 civarı) |
Lütfen bazı özelliklerin nikel diitrat için mevcut veya ilgili olmayabileceğini unutmayın.
Nikel Nitratın Güvenliği ve Tehlikeleri
Nikel dinitrat bazı güvenlik riskleri taşır ve kullanılırken dikkatli olunmalıdır. Bileşik ile doğrudan temas, cilt ve göz tahrişine neden olabilir. Tozunun veya dumanının solunması solunum yolu tahrişine neden olabilir. Nikel dinitrat ile çalışırken eldiven ve koruyucu gözlük gibi uygun koruyucu ekipmanların kullanılması önemlidir. Sağlığa zararlı olabileceğinden yutmaktan kaçının. Kazara maruz kalma durumunda derhal tıbbi yardıma başvurun. Ayrıca, iyi havalandırılmış, uyumsuz maddelerden uzak bir alanda uygun depolama, potansiyel riskleri en aza indirmek ve güvenli kullanım sağlamak açısından çok önemlidir.
| Tehlike sembolleri | Aşındırıcı, Tahriş Edici, Sağlığa zararlı |
| Güvenlik Açıklaması | Cilt ve göz tahrişine neden olur. Solunması veya yutulması halinde zararlıdır. Dikkatli tutun. Doğrudan temastan kaçının. Koruyucu ekipman kullanın. |
| BM kimlik numaraları | UN2724 |
| HS kodu | 2834.2990 |
| Tehlike sınıfı | 5.1 (Yükseltgen maddeler) |
| Paketleme grubu | II |
| Toksisite | Orta derecede toksik |
Nikel nitratın sentezi için yöntemler
Nikel dinitratı sentezlemek için çeşitli yöntemler vardır. Yaygın bir yöntem, nikel oksit (NiO) veya nikel hidroksit (Ni(OH)₂) ile nitrik asit (HNO₃) arasındaki reaksiyonu içerir. Bu işlem sırasında nikel oksit veya nikel hidroksit, nitrik asitte çözünür ve yan ürünler olarak nikel dinitrat ve su oluşumuna yol açar.
Reaksiyon aşağıdaki temsili alabilir:
- Nikel oksit ile: NiO + 2HNO₃ → Ni(NO₃)₂ + H₂O
- Nikel hidroksit ile: Ni(OH)₂ + 2HNO₃ → Ni(NO₃)₂ + 2H₂O
Başka bir yaklaşım, metalik nikel ile konsantre nitrik asit arasındaki reaksiyonu içerir; bu reaksiyon, yan ürün olarak nikel dinitrat ve nitrojen dioksit gazının (NO₂) oluşmasıyla sonuçlanır:
- Nikel Metal ile: Ni + 4HNO₃ → Ni(NO₃)₂ + 2H₂O + 2NO₂
Bu reaksiyonların iyi kontrol edilen koşullar altında gerçekleştirilmesi önemlidir çünkü nitrik asit güçlü bir oksitleyici maddedir ve tehlikeli olabilir. Uygun güvenlik önlemlerini ve ekipmanlarını aktif olarak kullanarak sentez süreci sırasında güvenli ve başarılı bir sonuç elde edin. Ek olarak reaktiflerin ve reaksiyon koşullarının seçimi, nikel dinitrat ürününün spesifik uygulamasına ve istenen özelliklerine bağlı olarak değişebilir.
Nikel Nitrat Kullanım Alanları
Nikel dinitrat, benzersiz özellikleri nedeniyle çeşitli endüstrilerde birçok uygulama alanı bulmaktadır. İşte ana kullanımlarından bazıları:
- Elektrokaplama: Nikel dinitrat, çeşitli metaller üzerinde ince bir nikel tabakasının birikmesine izin vererek, elektrokaplama işlemleri sırasında korozyon direncini ve görünümünü iyileştirir.
- Katalizör: Kimyasal reaksiyonlarda katalizör olarak çok önemli bir rol oynar, özellikle organik sentezde reaktanların istenen ürünlere dönüştürülmesini kolaylaştırır.
- Seramik: Seramik endüstrisi, seramik malzemelerin performansını artırmak ve spesifik renk vermek için nikel dinitrat kullanır.
- Cam Endüstrisi: Cam endüstrisindeki üreticiler, arzu edilen optik özelliklere sahip renkli cam üretmek için nikel dinitrat kullanır.
- Pil üretimi: Üreticiler, nikel-metal hidrit (NiMH) piller de dahil olmak üzere nikel bazlı pillerin üretiminde nikel dinitrat kullanıyor.
- Yakıt Hücreleri: Nikel dinitrat, katı oksit yakıt hücreleri (SOFC’ler) için nikel oksit elektrotların üretiminde bir öncü görevi görür.
- Piroteknik: Piroteknikte nikel dinitrat, havai fişeklerde yeşil alevler üreten bir oksidan görevi görür.
- Kimyasal Reaktifler: Çeşitli kimyasal reaksiyonlarda, özellikle nikel komplekslerini içerenlerde reaktif olarak işlev görür.
- Gübreler: Tarımda nikel dinitrat, bazı mahsullerdeki nikel eksikliklerini gidermek için ara sıra gübrelerde nikel kaynağı olarak kullanılır.
Nikel dinitratın farklı endüstrilerdeki çeşitli uygulamaları, onun çok çeşitli pratik kullanımlara sahip çok yönlü bir bileşik olarak önemini vurgulamaktadır.
Sorular:
S: Amonyum fosfat ve nikel(ii) nitrat çözeltileri karıştırıldığında ne çöker?
C: Nikel(II) fosfat çöküyor.
Soru: 500 ml’de 5,8 gram nikel nitrat içeren bir çözeltinin molaritesi nedir?
C: Molarite 0,2 M’dir.
S: Nikel nitrat hangi dalga boylarını emer?
C: Nikel dinitrat, ultraviyole ve görünür bölgelerdeki dalga boylarını emer.
S: Nikel II nitrat çözünür mü?
C: Evet, nikel(II) dinitrat suda çözünür.
S: Nikel II nitratın formülü nedir?
C: Formül Ni(NO₃)₂’dir.
S: Nikel II nitratın rengi nedir?
C: Nikel(II) dinitratın rengi yeşilimsi mavidir.
S: Ni(NO₃)₂ kimyasal formülünde kaç tane nitrojen atomu vardır?
Cevap: Dört adet nitrojen atomu vardır.
S: Ni(NO₃)₂ suda çözünür mü?
C: Evet, Ni(NO₃)₂ suda çözünür.
S: C4H10, BaCl2, Ni(NO₃)₂, SF6 bileşiklerinden hangileri formül birimleri olarak bulunmalıdır?
C: C4H10 (bütan) ve SF6 (kükürt heksaflorür) formül birimleri olarak mevcut olmalıdır. BaCl2 ve Ni(NO₃)₂ iyonik bileşiklerdir.
