Bor triklorür (BCl3), bir bor atomuna bağlı üç klor atomundan oluşan bir bileşiktir. Katalizörler gibi çeşitli endüstriyel işlemlerde ve organik sentezde reaktif olarak kullanılır.
| IUPAC Adı | Bor triklorür |
| Moleküler formül | BCl3 |
| CAS numarası | 10294-34-5 |
| Eş anlamlı | Trikloroboran; Bor(III) klorür, trikloro-boran, triklorobor |
| InChI | InChI=1S/BCl3/c2-1(3)4 |
Bor triklorürün özellikleri
Bor Triklorür Formülü
Bor klorürün formülü BCl3’tür ve üç klor atomuna bağlı bir bor atomunu temsil eder. Bu, bu bileşiğin bileşimini açıklayan basit ve anlaşılır bir moleküler formüldür.
Bor Triklorür Molar Kütlesi
Bor klorürün molar kütlesi, onu oluşturan elementlerin atomik kütleleri toplanarak hesaplanabilir. Borun atom kütlesi mol başına yaklaşık 10,81 gramdır ve her klor atomunun atom kütlesi mol başına yaklaşık 35,45 gramdır. Bu nedenle BCl3’ün molar kütlesi mol başına yaklaşık 117,17 gramdır.
Bor triklorürün kaynama noktası
Bor klorür diğer birçok bileşiğe kıyasla nispeten düşük bir kaynama noktasına sahiptir. Yaklaşık -15,7 santigrat derece veya 3,77 Fahrenheit sıcaklıkta kaynar. Bu, bu noktanın üzerindeki sıcaklıklarda bor klorürün sıvı fazdan gaz fazına dönüştüğü anlamına gelir.
Bor triklorür Erime noktası
Bor klorürün erime noktası nispeten düşüktür. -107,5 santigrat derece veya -161,5 Fahrenheit civarında eriyor. Bu noktanın altındaki sıcaklıklarda bileşik katı halden sıvı duruma geçer.
Bor triklorürün yoğunluğu g/mL
Bor klorürün yoğunluğu mililitre başına yaklaşık 1,38 gramdır. Bu değer, bileşiğin birim hacim başına kütlesini gösterir. Bor klorürün çeşitli uygulamalardaki davranışını belirlemek ve fiziksel özelliklerini anlamak için faydalıdır.
Bor Triklorür Molekül Ağırlığı
Bor klorürün moleküler ağırlığı mol başına yaklaşık 117.17 gramdır. Bu değer, bileşiğin bir molekülündeki tüm atomların atomik kütlelerinin toplamını temsil eder ve belirli bir numunedeki bor klorür miktarının belirlenmesi gibi çeşitli hesaplamalar için faydalıdır.
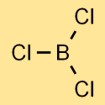
Bor triklorürün yapısı
Bor klorür trigonal düzlemsel bir moleküler yapıya sahiptir. Merkezde üçgen şeklinde düzenlenmiş üç klor atomuna bağlı bir bor atomundan oluşur. Bu yapı bileşiğin fiziksel ve kimyasal özelliklerine katkıda bulunur.
Bor triklorürün çözünürlüğü
Bor klorürün suda çözünürlüğü düşüktür. Az çözünür, yani sulu çözeltilerde yalnızca sınırlı bir ölçüde çözünür. Ancak benzen ve karbon tetraklorür gibi organik çözücülerde daha fazla çözünür. Bor klorürün çözünürlüğü, onun farklı kimyasal reaksiyonlardaki ve endüstriyel proseslerdeki davranışını etkiler.
| Dış görünüş | Renksiz gaz |
| Spesifik yer çekimi | 1.369 g/mL |
| Renk | Renksiz |
| Koku | Dönüm |
| Molar kütle | 117,17 gr/mol |
| Yoğunluk | 1,38 gr/ml |
| Füzyon noktası | -107,5°C |
| Kaynama noktası | -15,7°C |
| Flaş noktası | Uygulanamaz |
| sudaki çözünürlük | Tepki verir |
| çözünürlük | Benzen ve karbon tetraklorür gibi organik çözücülerde çözünür |
| Buhar basıncı | 20°C’de 623 mmHg |
| Buhar yoğunluğu | 3,24 (hava = 1) |
| pKa | Uygulanamaz |
| pH | Uygulanamaz |
Bor triklorürün güvenliği ve tehlikeleri
Bor klorür çeşitli güvenlik ve tehlike hususlarını gündeme getirmektedir. Aşındırıcıdır ve temas halinde ciltte, gözlerde ve solunum yollarında ciddi yanıklara neden olabilir. Buharlarının solunması solunum yolu tahrişine ve akciğer hasarına neden olabilir. Bileşik ayrıca suyla çok reaktiftir ve toksik hidrojen klorür gazı açığa çıkarır. Bor klorürün dikkatli bir şekilde kullanılması, uygun kişisel koruyucu ekipman kullanılması ve yeterli havalandırmanın sağlanması önemlidir. Kazara maruz kalma durumunda derhal tıbbi müdahale gereklidir. Ayrıca yangın, patlama ve tehlikeli gazların salınması riskini önlemek için uygun depolama ve taşıma prosedürlerine uyulmalıdır.
| Tehlike sembolleri | Aşındırıcı (C) |
| Güvenlik Açıklaması | Koruyucu eldiven/göz koruması/yüz koruması kullanın. Tozunu/dumanını/gazını/sisini/buharını/spreyini solumayın. İyi havalandırılmış bir alanda işlem yapın. |
| BM kimlik numaraları | UN1741 |
| HS kodu | 2827390000 |
| Tehlike sınıfı | 8 (Aşındırıcı maddeler) |
| Paketleme grubu | II |
| Toksisite | Yutulması veya solunması halinde çok toksiktir. Ciddi yanıklara ve solunum yolu tahrişine neden olabilir. Çok dikkatli davranın. |
Bor triklorürün sentezi için yöntemler
Bor klorürün sentezlenmesine yönelik bir yöntem , alüminyum klorür (AlCl3) gibi bir katalizörün varlığında bor oksit (B2O3 ) ile karbon tetraklorür (CCl4) arasındaki reaksiyonu içerir. B2O3 ve CCl4 yüksek sıcaklıklarda reaksiyona girerek yan ürünler olarak bor klorür ve karbondioksit üretir.
Diğer bir yaklaşım ise bor ve klor gazı arasındaki doğrudan reaksiyondur. Kontrollü koşullar altında bor, klor ile reaksiyona girerek bor klorür oluşumuna neden olur. Bu yöntem, tehlikeli yapısından dolayı klor gazının dikkatli bir şekilde kullanılmasını gerektirir.
Tiyonil klorür (SOCl2), borun yüksek sıcaklıklarda SOCl2 ile reaksiyona sokulması yoluyla bor klorürün sentezine izin verir, bu da bor klorür ve kükürt dioksit gazı üretimiyle sonuçlanır.
Bu sentez yöntemleri, hem laboratuvarda hem de endüstriyel ortamlarda bor klorür üretimi için uygun yollar sunar. Sentez sırasında iyi havalandırılmış alanlarda çalışmak ve uygun koruyucu ekipman kullanmak gibi uygun güvenlik önlemlerinin alınması çok önemlidir. Bu, proseste yer alan reaktiflerin ve ürünlerin tehlikeli doğasından dolayı önemlidir.
Bor triklorürün kullanım alanlarını yazınız
Bor klorür, benzersiz kimyasal özellikleri ve çok yönlülüğü nedeniyle katalizde, yarı iletken imalatında, malzeme sentezinde ve diğer çeşitli endüstrilerde yaygın olarak kullanılmaktadır.
- Bor klorür (BCl3), çeşitli kimyasal reaksiyonlarda, özellikle organik sentezlerde katalizör olarak uygulama alanı bulur. Farmasötiklerin, tarım kimyasallarının ve ince kimyasalların üretiminde karbon-karbon ve karbon-heteroatom bağlarının oluşumunu kolaylaştırır.
- BCl3, alev geciktirici ve yüksek sıcaklık kaplamalarında uygulamaları olan poliborazilen gibi bor bazlı polimerlerin sentezinde bir reaktif olarak hizmet eder.
- BCl3, yüksek sıcaklık uygulamalarında ve yağlayıcı olarak yaygın olarak kullanılan, olağanüstü termal ve kimyasal stabilitesiyle tanınan bir malzeme olan bor nitrürün üretimini kolaylaştırır.
- Yarı iletken endüstrisi, bor atomlarını silikon kristallerine dahil etmek, elektriksel özelliklerini geliştirmek ve elektronik cihazlarda kullanıma uygun hale getirmek için BCl3’ü katkı maddesi olarak kullanıyor.
- Metalurjide BCl3, metallerin rafine edilmesi sırasında oksit yabancı maddelerini uzaklaştırmak ve böylece saflıklarını arttırmak için bir eritici ajan olarak görev yapar.
- BCl3, seramik zırh ve kesici takımların üretiminde yaygın olarak kullanılan hafif ve güçlü bir malzeme olan bor karbürün üretiminde merkezi bir rol oynamaktadır.
- BCl3, bor esterleri, boronik asitler ve boranlar dahil olmak üzere birçok bor içeren bileşiğin sentezinde çok önemli bir rol oynar. Bu bileşiklerin kimyasal araştırmalarda ve endüstriyel işlemlerde birçok uygulaması vardır.
- Petrol endüstrisinde BCl3, benzinin oktan sayısını arttırmak için katkı maddesi olarak kullanılır.
İstenilen optik ve termal özelliklere sahip olan bor içeren cam üretiminde bor kaynağı olarak görev yapar.
Sorular:
S: Bor triklorürün formülü nedir?
A: Bor klorürün formülü BCl3’tür.
S: Bor triklorür polar mıdır?
C: Evet, bor klorür, bor atomunda serbest bir çiftin bulunması ve klor atomlarının asimetrik düzenlenmesi nedeniyle polar bir moleküldür.
S: Bor triklorürde (BCl3) bor hibridizasyonu nedir?
A: BCl3’teki borun hibridizasyonu sp2’dir.
S: Bir bor triklorür molekülünün kütlesi nedir?
C: Bir bor klorür (BCl3) molekülünün kütlesi, mol başına yaklaşık 117,17 gramdır.
S: Bor triklorür hibridizasyonu nedir?
A: Bor klorürde (BCl3) borun hibridizasyonu sp2’dir.
S: Bor triklorür ile hidrojeni karıştırdığınızda ne olur?
C: Bor klorür (BCl3) hidrojen (H2) ile karıştırıldığında reaksiyona girerek bor ve hidrojen klorür gazı (HCl) oluştururlar.
S: Boron triklorür neden monomer olarak varken alüminyum triklorür dimer olarak var?
C: Bor ve alüminyum atomları arasındaki boyut ve elektron yoğunluğu farkı, bor klorürün (BCl3) bir monomer olarak bulunmasına neden olurken, alüminyum klorür (AlCl3) koordinat bağlantıları oluşturma yeteneğinden dolayı bir dimer oluşturur.
S: BCl3 bir Lewis asidi midir?
C: Evet, BCl3 bir Lewis asididir çünkü bir Lewis bazından bir çift elektron kabul edebilir.
S: BCl3 iyonik mi yoksa kovalent mi?
C: BCl3 kovalent bir bileşiktir.
S: BCl3 kovalent bir bağ mıdır?
C: Evet, BCl3 bor ve klor atomları arasındaki kovalent bağlardan oluşur.
S: BCl3 bir gaz mıdır?
C: Evet, BCl3 standart sıcaklık ve basınç (STP) gazıdır.
S: BCl3 polar mı yoksa polar olmayan bir molekül mü?
C: BCl3, bor atomu etrafındaki klor atomlarının asimetrik düzenlenmesinden kaynaklanan elektron yoğunluğunun eşit olmayan dağılımı nedeniyle polar bir moleküldür.
