Nikel(II) oksit, NiO formülüne sahip kimyasal bir bileşiktir. Yaygın olarak katalizör olarak ve seramik ve pigment üretiminde kullanılan siyah bir katıdır.
| IUPAC Adı | Nikel(II) oksit |
| Moleküler formül | NiO |
| CAS numarası | 1313-99-1 |
| Eş anlamlı | Nikel oksit, nikel monoksit, Ni(II) oksit |
| InChI | InChI=1S/Ni.O |
Nikel(II) oksidin özellikleri
Nikel(II) Oksit Formülü
Nikel monoksitin kimyasal formülü NiO’dur. Bir nikel (Ni) atomu ve bir oksijen (O) atomundan oluşur, bu da basit ve anlaşılır bir formül sağlar.
Nikel(II) Oksit Molar Kütlesi
Nikel monoksitin molar kütlesi, onu oluşturan elementlerin atomik kütleleri toplanarak hesaplanabilir. NiO için molar kütle, mol başına yaklaşık 74,69 gramdır (g/mol).
Nikel (II) oksidin kaynama noktası
Nikel monoksitin kaynama noktasına ulaşmadan önce ayrışmaya uğraması nedeniyle belirgin bir kaynama noktası yoktur. Isıtıldığında, kendisini oluşturan elementler olan nikel ve oksijene ayrışır.
Nikel(II) oksit Erime noktası
Nikel monoksitin erime noktası yaklaşık 1984 santigrat derecedir (1984 °C). Bu sıcaklıkta katı NiO sıvı duruma dönüşür.
Nikel(II) oksit yoğunluğu g/mL
Nikel monoksitin yoğunluğu mililitre başına yaklaşık 6,67 gramdır (g/mL). Bu değer, belirli bir hacimde paketlenmiş kütle miktarını gösterir ve bu da onu maddenin kompaktlığının bir ölçüsü yapar.
Nikel(II) Oksit Molekül Ağırlığı
Nikel monoksitin moleküler ağırlığı, onu oluşturan elementlerin atom ağırlıkları toplanarak hesaplanır. NiO için molekül ağırlığı mol başına yaklaşık 74,69 gramdır (g/mol).
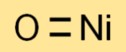
Nikel(II) oksidin yapısı
Nikel monoksit kübik kristal yapıya sahiptir. Düzenli, tekrarlanan bir düzende düzenlenmiş nikel iyonlarından (Ni2+) ve oksit iyonlarından (O2-) oluşur. Bu yapı onun karakteristik özelliklerine ve davranışına katkıda bulunur.
Nikel(II) oksidin çözünürlüğü
Nikel monoksit suda çok az çözünür. Sınırlı bir çözünürlüğe sahiptir, yani suda yalnızca küçük bir oranda çözünür. Ancak asitlerle reaksiyona girerek çözünebilir nikel tuzları oluşturabilir ve belirli bir derecede kimyasal reaktivite sergileyebilir.
| Dış görünüş | Katı Siyah |
| Spesifik yer çekimi | 6.67g/ml |
| Renk | Siyah |
| Koku | Kokusuz |
| Molar kütle | 74,69 gr/mol |
| Yoğunluk | 6.67g/ml |
| Füzyon noktası | 1984°C |
| Kaynama noktası | ayrıştırılmış |
| Flaş noktası | Uygulanamaz |
| sudaki çözünürlük | Az çözünür |
| çözünürlük | Asitlerde çözünür, çözünür nikel tuzları oluşturur |
| Buhar basıncı | Müsait değil |
| Buhar yoğunluğu | Müsait değil |
| pKa | Uygulanamaz |
| pH | Doğal |
Parlama noktası, buhar basıncı ve pKa gibi bazı özelliklerin nikel monoksit için geçerli olmadığını veya mevcut olmadığını lütfen unutmayın.
Nikel(ii) Oksit Güvenliği ve Tehlikeleri
Nikel monoksit belirli güvenlik hususlarını ve tehlikeleri sunar. Dikkatli bir şekilde ele alınması önemlidir. Ciltle, gözlerle doğrudan temastan veya toz veya buharının solunmasından kaçınılmalıdır. Bu, bazı kişilerde cilt tahrişine ve alerjik reaksiyonlara neden olabilir. Yutulması veya solunması halinde derhal tıbbi müdahale gereklidir. Nikel monoksit son derece yanıcı olarak kabul edilmez ancak yanıcı maddelere maruz kalması durumunda yangına katkıda bulunabilir. İyi havalandırılmış bir alanda saklamak ve taşımak önemlidir. Potansiyel riskleri en aza indirmek için nikel monoksit ile çalışırken eldiven ve gözlük gibi uygun kişisel koruyucu ekipmanlar giyilmelidir.
| Tehlike sembolleri | Hiçbiri |
| Güvenlik Açıklaması | Dikkatli tutun. Doğrudan temastan ve solumaktan kaçının. Uygun koruyucu ekipman kullanın. Gerekirse tıbbi yardım alın. |
| BM kimlik numaraları | Uygulanamaz |
| HS kodu | 2825.70.10 |
| Tehlike sınıfı | sınıflandırılmamış |
| Paketleme grubu | sınıflandırılmamış |
| Toksisite | Yutulması veya solunması halinde zararlı olduğu kabul edilir. Ciltte tahrişe ve alerjik reaksiyonlara neden olabilir. |
Lütfen nikel monoksitin belirli tehlike simgeleri, BM tanımlayıcıları, tehlike sınıfı veya paketleme grubu taşımadığını unutmayın. Sağlanan güvenlik bilgileri, nikel monoksitin taşınması ve kullanımına ilişkin genel bilgi ve önlemlere dayanmaktadır. Doğru ve ayrıntılı bilgi için özel güvenlik veri sayfalarına (SDS) başvurmak ve önerilen güvenlik uygulamalarını takip etmek önemlidir.
Nikel(ii) oksit sentezine yönelik yöntemler
Nikel monoksitin sentezlenmesi için çeşitli yöntemler vardır. Yaygın bir yaklaşım, nikel karbonat veya nikel hidroksit gibi nikel bileşiklerinin termal ayrışmasıdır. Bu yöntemde, nikel monoksit oluşturmak için oksijen yokluğunda belirli bir öncü bileşiğin ısıtılması.
Başka bir yöntem metalik nikelin oksidasyonunu içerir. Metalik nikel, yüksek sıcaklıklarda oksijen veya hava ile reaksiyona girerek nikel monoksit üretebilir. Bu işlemi, nikel monoksit üretmek için nikel metalini hava veya oksijen atmosferinde kalsine ederek veya kavurarak gerçekleştirin.
Nikel klorür veya nikel nitrat gibi nikel tuzlarını, sodyum hidroksit veya amonyum hidroksit gibi alkalin bir çözeltiyle reaksiyona sokarak nikel monoksiti sentezlemek için çökeltme reaksiyonlarını kullanın. Bu reaksiyon bir nikel monoksit çökeltisi oluşturur.
Sol-jel sentezi başka bir uygulanabilir yöntemdir. Bu, nikel alkoksitler gibi uygun nikel öncüllerinin bir çözelti içinde hidrolizini ve yoğunlaşmasını içerir. Çökelme reaksiyonu sırasında oluşan jeli kurutup kalsine ederek nikel monoksit elde edin.
Nikel monoksitin sentezi için elektrodepozisyon tekniklerini kullanın. Bir elektrolit çözeltisine batırılmış bir nikel elektrota elektrik akımı uygulandığında, elektrotun yüzeyinde nikel monoksit oluşabilir.
Bir sentez yöntemi seçerken, her yöntem kendi avantajlarını sunduğundan istenen saflık, ölçeklenebilirlik ve özel uygulama gereksinimleri gibi faktörler dikkate alınmalıdır.
Nikel(ii) Oksit Kullanımı
Nikel monoksit, benzersiz özellikleri nedeniyle farklı endüstrilerde çeşitli kullanım alanları bulur. Yaygın uygulamalarından bazıları şunlardır:
- Katalizör: Nikel monoksit, hidrojenasyon ve oksidasyon işlemleri gibi çeşitli kimyasal reaksiyonları aktif olarak katalize ederek reaktanların istenen ürünlere dönüştürülmesini kolaylaştırır.
- Seramik: Seramik malzemelerin üretiminde nikel monoksit, aktif olarak renklendirici bir madde olarak işlev görür ve seramik sırlarında ve pigmentlerde belirli renk ve desenlerin elde edilmesine aktif olarak katkıda bulunur.
- Piller: Şarj edilebilir nikel-kadmiyum (NiCd) ve nikel-metal hidrit (NiMH) piller, pozitif elektrot malzemesi olarak aktif olarak nikel monoksit kullanarak elektrik enerjisinin depolanmasını ve serbest bırakılmasını aktif olarak sağlar.
- Gaz sensörleri: Nikel monoksit, ona dayalı sensörlerde kullanıldığında gaz algılama uygulamalarında karbon monoksit (CO) ve nitrojen dioksit (NO2) gibi gazları aktif olarak algılar.
- Cam İmalatı: Cam endüstrisi, cam ürünlere çeşitli renkler kazandırmak için aktif olarak nikel monoksit kullanmakta ve böylece yeşil, kahverengi ve siyah tonları da dahil olmak üzere renkli cam üretimine aktif olarak katkıda bulunmaktadır.
- İletken Kaplamalar: Nikel monoksit, iletken kaplamalarda aktif bir bileşen olarak işlev görür ve cam veya plastik gibi malzemeleri kendilerine uygulandığında aktif olarak iletken hale getirir.
- Yakıt Hücreleri: Nikel monoksit aktif olarak katı oksit yakıt hücrelerinin (SOFC’ler) bir bileşeni olarak işlev görür, aktif olarak katot malzemesi olarak görev yapar ve yakıt hücresi içindeki elektrokimyasal reaksiyonlara katılır.
- Katalizör Desteği: Nikel monoksit diğer katalizörler için aktif olarak destek malzemesi görevi görür ve kararlılıklarını ve performanslarını aktif olarak artırır.
Nikel monoksitin çeşitli uygulama yelpazesi, onun çeşitli endüstrilerdeki önemini vurgulayarak kullanışlılığını ve çok yönlülüğünü vurgulamaktadır.
Sorular:
S: Nikel(II) oksidin formülü nedir?
C: Nikel(II) oksidin formülü NiO’dur.
S: Nikel(II) oksit nitrik asitle reaksiyona girdiğinde hangi tuz oluşur?
C: Nikel(II) oksidin nitrik asitle reaksiyonu nikel(II) nitratı (Ni(NO3)2) oluşturur.
S: Nikel(II) hangi voltajda nikel(III)’e oksitlenir?
C: Nikel(II), yaklaşık +1,63V voltajda nikel(III)’e oksitlenir.
S: Ni(ler) resimde gösterildiği gibi nikel(II) iyonuna oksitlendiğinde ne olur?
C: Ni(s)’nin nikel(II) iyonuna oksidasyonu sırasında elektronlar kaybolur, bu da Ni2+ iyonlarının oluşmasına neden olur.
S: 13,3 g nikel üretmek için hangi kütlelerde nikel(II) oksit ve alüminyum kullanılmalıdır?
C: 13,3 g nikel üretmek için gereken nikel(II) oksit ve alüminyum kütleleri, ilgili spesifik reaksiyona ve stokiyometriye bağlıdır.
