1-Butanol (C4H9OH), hafif tatlı bir kokuya sahip, renksiz bir alkoldür. Çözücü olarak, organik sentezlerde ve yakıt kaynağı olarak kullanılır. Kozmetik ve kişisel bakım ürünlerinde de kullanılabilir.
| IUPAC Adı | Butan-1-ol |
| Moleküler formül | C4H10O |
| CAS numarası | 71-36-3 |
| Eş anlamlı | n-bütil alkol, bütanol, bütil alkol, 1-bütil alkol, 1-bütanol, bütanolen, bütilen hidrat, bütil hidrat |
| InChI | InChI=1S/C4H10O/c1-2-3-4-5/h5H,2-4H2,1H3 |
1-bütanolün özellikleri
Formül 1-Butanol
1-Bütanolün moleküler formülü C4H10O’dur. Bu, dört karbon atomu, on hidrojen atomu ve bir oksijen atomu içerdiği anlamına gelir. İlk karbon atomuna bağlı hidroksil grubu (-OH) ile doğrusal bir yapıya sahiptir.
1-Butanol Molar Kütle
C4H9OH’nin molar kütlesi 74,12 g/mol’dür. Bu, bir mol C4H9OH’nin 74,12 gram ağırlığında olduğu anlamına gelir. Molar kütle bir maddenin önemli bir özelliğidir çünkü belirli bir numunede bulunan madde miktarının belirlenmesine yardımcı olur.
1-bütanolün kaynama noktası
C4H9OH’nin kaynama noktası 117,7°C’dir (243,9°F). Bu, bu sıcaklıkta sıvıdan gaza geçeceği anlamına gelir. C4H9OH’un kaynama noktası, fazladan bir karbon atomunun varlığı nedeniyle etanolün kaynama noktasından daha yüksektir.
1-Butanol Erime Noktası
C4H9OH’nin erime noktası -90,6°C’dir (-131,1°F). Bu, bu sıcaklıkta katıdan sıvıya geçeceği anlamına gelir. C4H9OH’un erime noktası, benzer molekül ağırlığına sahip olan bütanoik asidin erime noktasından daha düşüktür.
1-Butanol Yoğunluğu g/ml
C4H9OH’nin yoğunluğu 0,81 g/mL’dir. Bu, bir mililitre C4H9OH’nin 0,81 gram ağırlığında olduğu anlamına gelir. C4H9OH’un yoğunluğu, yoğunluğu 1 g/mL olan suyunkinden daha düşüktür.
1-Butanol Molekül Ağırlığı
C4H9OH’nin moleküler ağırlığı 74,12 g/mol’dür. Molekül formülündeki tüm atomların atom ağırlıklarının toplamıdır. Molekül ağırlığı bir maddenin önemli bir özelliğidir çünkü fiziksel ve kimyasal özelliklerinin belirlenmesine yardımcı olur.
1-bütanolün yapısı
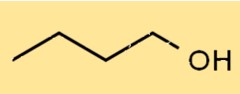
C4H9OH’nin yapısı, ilk karbon atomuna hidroksil grubunun (-OH) bağlı olduğu düz zincirli bir alkoldür. Dört karbon atomu, on hidrojen atomu ve bir oksijen atomundan oluşan doğrusal bir yapıya sahiptir. Yapısı diğer moleküllerle hidrojen bağları oluşturmasını sağlar.
1-bütanolün çözünürlüğü
C4H9OH su ve organik çözücülerde çözünür. Sıcaklık arttıkça sudaki çözünürlüğü azalır. Ayrıca etanol ve metanol gibi polar çözücülerde de çözünür. C4H9OH’nin benzen ve eter gibi organik çözücülerdeki çözünürlüğü sudakinden daha yüksektir. Bu, onu organik sentezde bir çözücü olarak faydalı kılar.
| Dış görünüş | Renksiz sıvı |
| Spesifik yer çekimi | 25°C’de 0,810 g/mL |
| Renk | Renksiz |
| Koku | Biraz tatlı |
| Molar kütle | 74,12 gr/mol |
| Yoğunluk | 0.81g/ml |
| Füzyon noktası | -90,6°C (-131,1°F) |
| Kaynama noktası | 117,7°C (243,9°F) |
| Flaş noktası | 35°C (95°F) |
| sudaki çözünürlük | 20°C’de 79 g/L |
| çözünürlük | Etanol, dietil eter, aseton, benzen, kloroformda çözünür |
| Buhar basıncı | 20°C’de 1,16 kPa |
| Buhar yoğunluğu | 2,55 (havaya göre) |
| pKa | 16.06 |
| pH | Nötr (7) |
1-Butanolün güvenliği ve tehlikeleri
C4H9OH çeşitli güvenlik riskleri taşır, bu da onu dikkatli bir şekilde ele almayı çok önemli hale getirir. Isıya veya kıvılcımlara maruz kaldığında kolayca tutuşabilen yanıcı bir sıvıdır. Ayrıca gözlerde, solunum sisteminde ve ciltte tahrişe ve hasara neden olabilecek zararlı buharlar yayar. Yutulduğunda baş dönmesi, kafa karışıklığı ve hatta koma gibi ciddi sağlık sorunlarına neden olabilir. Bu nedenle C4H9OH ile çalışırken eldiven, gözlük ve solunum cihazı gibi koruyucu ekipmanların kullanılması önemlidir. Cilt veya gözlerle teması halinde suyla yıkayın ve hemen bir doktora başvurun. Kazaları önlemek ve güvenliği sağlamak için C4H9OH’nin uygun şekilde depolanması, taşınması ve imha edilmesi gereklidir.
| Tehlike sembolleri | F, Xi |
| Güvenlik Açıklaması | Isıdan/kıvılcımdan/açık alevden/sıcak yüzeylerden uzak tutun. Koruyucu eldiven/göz koruması/yüz koruması kullanın. CİLT (veya saç) İLE TEMAS HALİNDE İSE: Kirlenmiş tüm giysileri derhal çıkarın. Cildi su/duş ile durulayın. GÖZ İLE TEMASI HALİNDE: Su ile birkaç dakika dikkatlice durulayın. Varsa ve yapılması kolaysa kontakt lensleri çıkarın. Durulamaya devam edin. Uyumsuz maddelerden uzakta, serin, kuru ve iyi havalandırılan bir alanda saklayın. |
| BM kimlik numaraları | BM 1120 |
| HS kodu | 2905.16.00 |
| Tehlike sınıfı | 3 |
| Paketleme grubu | III |
| Toksisite | LD50 (oral, sıçan) 2,46 g/kg; LC50 (soluma, sıçan) 37.800 ppm/4 saat |
1-butanol sentezi için yöntemler
C4H9OH, bütiraldehit indirgemesi, okso işleme veya fermantasyon dahil olmak üzere çeşitli yöntemlerle sentezlenebilir.
Fermantasyon, biyokütleden C4H9OH üretmek için yaygın bir yöntemdir. Fermantasyon sürecinde Clostridium acetobutylicum gibi mikroorganizmalar, şekerleri, nişastaları veya selülozu fermente ederek C4H9OH dahil organik asitler ve alkollerden oluşan bir karışım üretmekten sorumludur.
Hidroformilasyon olarak da bilinen okso işlemi, propenin kobalt veya rodyum gibi bir katalizör varlığında karbon monoksit ve hidrojen ile reaksiyonunu içerir. Butiraldehitin hidrojenasyonu C4H9OH üretir. Butiraldehit hidrojenasyona uğradığında C4H9OH bileşiğini oluşturur.
C4H9OH’yi sentezlemenin başka bir yöntemi, paladyum veya nikel gibi bir katalizörün varlığında bütiraldehitin hidrojenle indirgenmesini içerir. Bu reaksiyon, yan ürün olarak su ile C4H9OH üretir.
Fischer-Tropsch süreci, fosil yakıtlardan C4H9OH üretme yöntemidir. Bu, karbon monoksit ve hidrojenin reaksiyona girmesini sağlamak için bir katalizör kullanılmasını ve bunun sonucunda C4H9OH dahil çeşitli hidrokarbonların üretilmesini içerir.
1-bütanolün kullanım alanları
C4H9OH benzersiz özelliklerinden dolayı çeşitli endüstrilerde birçok kullanıma sahiptir. C4H9OH’un bazı yaygın kullanımları şunlardır:
- Çözücü: Reçineler, yağlar, yağlar ve mumlar dahil olmak üzere çeşitli maddeler için çözücü olarak kullanılır.
- Ara Ürün: Butil akrilat ve butil asetat gibi diğer kimyasalların üretiminde ara ürün olarak kullanılır.
- Katkı Maddesi: Benzin ve dizel yakıtlarda oktan sayısını arttırmak ve emisyonları azaltmak amacıyla katkı maddesi olarak kullanılır.
- Ekstraktan: Antibiyotik, vitamin ve hormon üretiminde ekstraktan olarak kullanılır.
- Kozmetik ve Kişisel Bakım Ürünleri: Losyon, krem, parfüm gibi çeşitli kozmetik ve kişisel bakım ürünlerinin üretiminde kullanılır.
- Aroma ve Kokular: Yiyecek ve içecek endüstrisinde lezzet ve koku arttırıcı olarak kullanılır.
- Farmasötikler: Sedatifler ve hipnotikler de dahil olmak üzere çeşitli farmasötik ürünlerin üretiminde kullanılır.
- Pestisitler: Çeşitli pestisit ve herbisitlerin üretiminde bileşen olarak kullanılır.
Sorular:
S: Butanol polar mı?
C: Evet, bütanol, ona dipol momenti veren hidroksil grubunun (-OH) varlığı nedeniyle polardır.
S: 1-bütanol suda çözünür mü?
C: Evet, C4H9OH, su molekülleriyle hidrojen bağları oluşturmasını sağlayan hidroksil grubunun varlığı nedeniyle suda kısmen çözünür.
S: 1-bütanolün hidrojen bağı var mı?
C: Evet, C4H9OH, diğer C4H9OH molekülleri veya su molekülleri ile hidrojen bağları oluşturabilen hidroksil grubunun (-OH) varlığı nedeniyle bir hidrojen bağına sahiptir.
S: Bu çözünenin 0,350 m’lik sulu çözeltisinin 725 ml’sini hazırlamak için kaç ml 1-butanol gereklidir?
C: Hesaplama, C4H9OH’nin molar kütlesinin 74,12 g/mol olmasını gerektirir. 0,350 M’lik bir C4H9OH çözeltisi hazırlamak için 26,12 g C4H9OH gereklidir. Mol = konsantrasyon x hacim formülünü kullanarak ihtiyaç duyulan C4H9OH hacmini şu şekilde hesaplayabiliriz: hacim = mol / konsantrasyon. Böylece 725 ml 0,350 m’lik çözelti hazırlamak için gereken C4H9OH hacmi (26,12/0,350) = 74,6 ml olur.
S: Hangi alkol en çok suya benzer? c2h5oh c4h9oh c10h21oh c7h15oh
C: Verilen seçeneklerden etanol (C2H5OH), küçük moleküler boyutu ve su molekülleriyle güçlü hidrojen bağları oluşturmasına olanak tanıyan hidroksil grubunun (-OH) varlığı nedeniyle en çok suya benzer davranacaktır.
S: c4h9oh’un yanması için dengeli denklemin ürünleri nelerdir?
A: C4H9OH’nin yanması için dengeli denklem şu şekildedir: C4H9OH + 6O2 → 4CO2 + 5H2O. Reaksiyon ürünleri karbondioksit (CO2) ve sudur (H2O).
S: Bütanolün molar kütlesi (c4h9oh) nedir?
A: Bütanolün (C4H9OH) molar kütlesi 74,12 g/mol’dür.
S: C4h9oh’da hidrojen bağı var mı?
C: Evet, C4H9OH, diğer C4H9OH molekülleri veya su molekülleri ile hidrojen bağları oluşturmasını sağlayan hidroksil grubunun (-OH) varlığı nedeniyle bir hidrojen bağına sahiptir.
S: 2500 ml’lik bir çözeltide veya 2,22 m2’de kaç gram bütil alkol (c4h9oh) vardır?
C: Çözeltideki bütil alkolün gram sayısını hesaplamak için şu formülü kullanmamız gerekir: mol = konsantrasyon x hacim. Çözeltinin konsantrasyonu 2,22 mol/L ve hacmi 2,5 L’dir (2500 ml, L’ye dönüştürülür). Yani çözeltideki bütil alkolün mol sayısı: 2,22 x 2,5 = 5,55 mol. Bütil alkolün kütlesini hesaplamak için mol sayısını molar kütlesiyle (74,12 g/mol) çarpın: 5,55 x 74,12 = 411,4 g. Bu nedenle 2.500 ml’lik bir çözeltide veya 2.22 M’de 411.4 gram bütil alkol bulunur.
