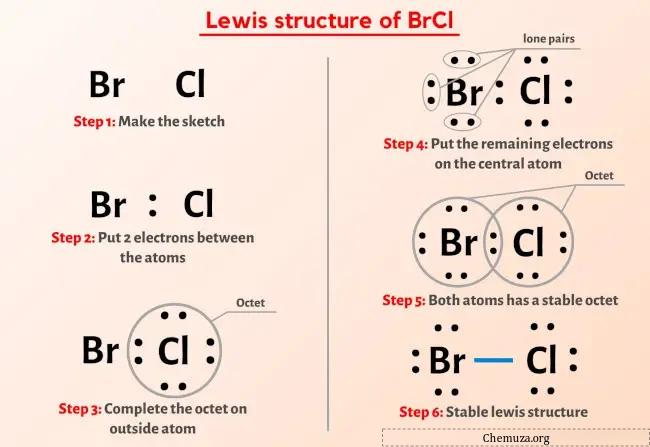
Vous avez donc déjà vu l’image ci-dessus, n’est-ce pas ?
Laissez-moi vous expliquer brièvement l’image ci-dessus.
La structure BrCl Lewis a un atome de brome (Br) et un atome de chlore (Cl) qui contiennent une simple liaison entre eux. Il y a 3 paires isolées sur l’atome de brome (Br) ainsi que sur l’atome de chlore (Cl).
Si vous n’avez rien compris de l’image ci-dessus de la structure de Lewis de BrCl, alors restez avec moi et vous obtiendrez l’explication détaillée étape par étape sur le dessin d’une structure de Lewis de BrCl .
Passons donc aux étapes de dessin de la structure de Lewis de BrCl.
Étapes de dessin de la structure BrCl Lewis
Étape 1 : Trouver le nombre total d’électrons de valence dans la molécule BrCl
Afin de trouver le nombre total d’électrons de valence dans une molécule BrCl, vous devez tout d’abord connaître les électrons de valence présents dans l’atome de brome ainsi que dans l’atome de chlore.
(Les électrons de valence sont les électrons présents sur l’ orbite la plus externe de tout atome.)
Ici, je vais vous expliquer comment trouver facilement les électrons de valence du brome ainsi que du chlore à l’aide d’un tableau périodique.
Total des électrons de valence dans la molécule BrCl
→ Électrons de Valence donnés par l’atome de brome :
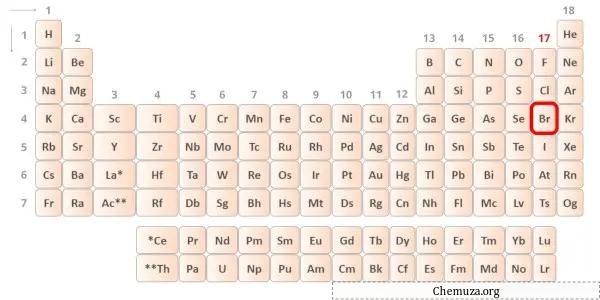
Le brome est un élément du groupe 17 du tableau périodique. [1] Par conséquent, les électrons de valence présents dans le brome sont 7 .
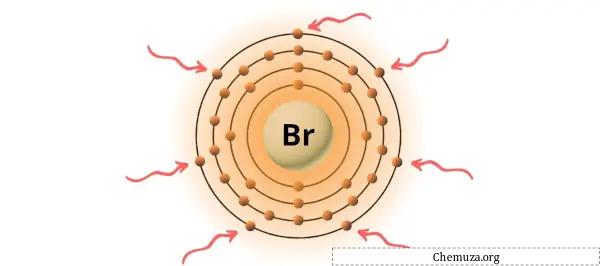
Vous pouvez voir les 7 électrons de valence présents dans l’atome de brome, comme le montre l’image ci-dessus.
→ Électrons de Valence donnés par l’atome de chlore :

Le chlore est un élément du groupe 17 du tableau périodique. [2] Par conséquent, les électrons de valence présents dans le chlore sont 7 .
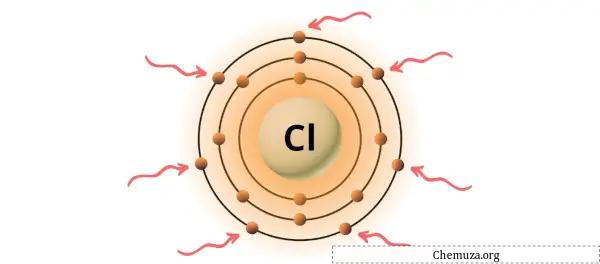
Vous pouvez voir les 7 électrons de valence présents dans l’atome de chlore, comme le montre l’image ci-dessus.
Ainsi,
Total des électrons de valence dans la molécule BrCl = électrons de valence donnés par 1 atome de brome + électrons de valence donnés par 1 atome de chlore = 7 + 7 = 14 .
Étape 2 : Sélectionnez l’atome central
Pour sélectionner l’atome central, il faut se rappeler que l’atome le moins électronégatif reste au centre.
Maintenant, ici, la molécule donnée est BrCl. Il n’a que deux atomes, vous pouvez donc sélectionner n’importe lequel d’entre eux comme atome central.

Supposons que l’atome de brome soit l’atome central.
(Vous devez considérer l’atome le moins électronégatif comme atome central).
Étape 3 : Connectez chaque atome en plaçant une paire d’électrons entre eux
Maintenant, dans la molécule BrCl, vous devez mettre les paires d’électrons entre l’atome de brome (Br) et l’atome de chlore (Cl).

Cela indique que le brome (Br) et le chlore (Cl) sont chimiquement liés les uns aux autres dans une molécule BrCl.
Étape 4 : Rendre les atomes externes stables. Placez la paire d’électrons de valence restante sur l’atome central.
Dans cette étape, vous devez vérifier la stabilité de l’atome externe.
Ici, dans le schéma de la molécule BrCl, nous avons supposé que l’atome de brome était l’atome central. Le chlore est donc l’atome externe.
Il faut donc rendre l’atome de chlore stable.
Vous pouvez voir dans l’image ci-dessous que l’atome de chlore forme un octet et qu’il est donc stable.
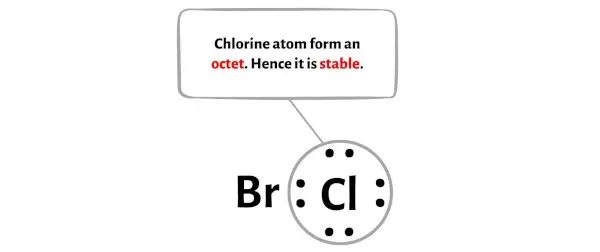
De plus, à l’étape 1, nous avons calculé le nombre total d’électrons de valence présents dans la molécule BrCl.
La molécule BrCl possède un total de 14 électrons de valence et parmi ceux-ci, seuls 8 électrons de valence sont utilisés dans le schéma ci-dessus.
Donc le nombre d’électrons restants = 14 – 8 = 6 .
Vous devez mettre ces 6 électrons sur l’atome de brome dans le schéma ci-dessus de la molécule BrCl.
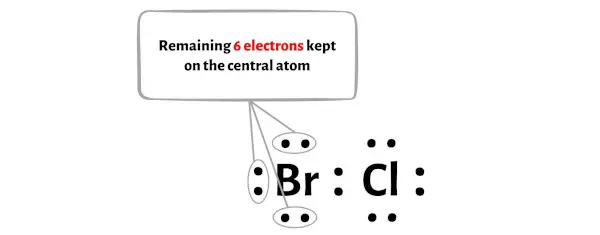
Passons maintenant à l’étape suivante.
Étape 5 : Vérifier la stabilité de la structure Lewis
Vous êtes maintenant arrivé à la dernière étape dans laquelle vous devez vérifier la stabilité de la structure de Lewis de BrCl.
La stabilité de la structure Lewis peut être vérifiée en utilisant un concept de charge formelle .
Bref, il faut maintenant trouver la charge formelle des atomes de brome (Br) ainsi que des atomes de chlore (Cl) présents dans la molécule BrCl.
Pour calculer la taxe formelle, vous devez utiliser la formule suivante :
Charge formelle = Électrons de Valence – (Électrons de liaison)/2 – Électrons non liants
Vous pouvez voir le nombre d’ électrons liants et d’électrons non liants pour chaque atome de la molécule BrCl dans l’image ci-dessous.
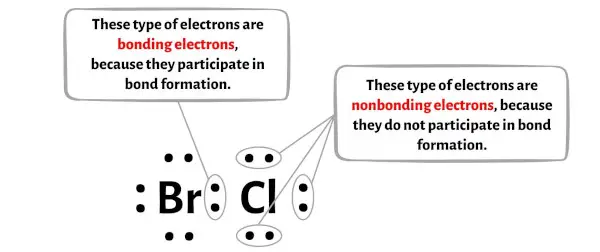
Pour l’atome de brome (Br) :
Électrons de Valence = 7 (car le brome est dans le groupe 17)
Électrons de liaison = 6
Électrons non liants = 4
Pour l’atome de chlore (Cl) :
Électrons de Valence = 7 (car le chlore est dans le groupe 17)
Électrons de liaison = 2
Électrons non liants = 6
| Accusation formelle | = | électrons de valence | – | (Electrons de liaison)/2 | – | Électrons non liants | ||
| Br | = | 7 | – | 6/2 | – | 4 | = | 0 |
| Cl | = | 7 | – | 2/2 | – | 6 | = | 0 |
À partir des calculs de charge formelle ci-dessus, vous pouvez voir que l’atome de brome (Br) ainsi que l’atome de chlore (Cl) ont une charge formelle « nulle » .
Cela indique que la structure de Lewis ci-dessus de BrCl est stable et qu’il n’y a aucun autre changement dans la structure ci-dessus de BrCl.
Dans la structure de points de Lewis ci-dessus de BrCl, vous pouvez également représenter chaque paire d’électrons de liaison (:) comme une liaison simple (|). Ce faisant, vous obtiendrez la structure de Lewis suivante de BrCl.
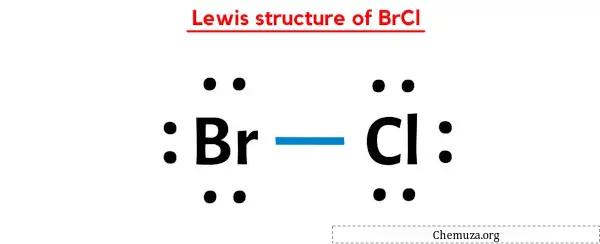
J’espère que vous avez complètement compris toutes les étapes ci-dessus.
Pour plus de pratique et une meilleure compréhension, vous pouvez essayer d’autres structures de Lewis répertoriées ci-dessous.
Essayez (ou au moins voyez) ces structures de Lewis pour une meilleure compréhension :
