Этиленгликоль (C2H6O2) представляет собой прозрачную жидкость со сладким вкусом без запаха, обычно используемую в антифризах и других промышленных применениях. При попадании в организм он токсичен и может вызвать серьезные проблемы со здоровьем.
| Название ИЮПАК | Этан-1,2-диол |
| Молекулярная формула | C2H6O2 |
| Количество CAS | 107-21-1 |
| Синонимы | 1,2-Этандиол, гликоль, моноэтиленгликоль, МЭГ, этиленовый спирт, гиподикарбоновая кислота, дигидрат этилена. |
| ИнЧИ | ИнЧИ=1S/C2H6O2/c3-1-2-4/h3-4H,1-2H2 |
Свойства этиленгликоля
Этиленгликоль Молярная масса
Моноэтиленгликоль (МЭГ) имеет молярную массу 62,07 г/моль. Молярная масса – это масса одного моля вещества, выраженная в граммах. Молярную массу моноэтиленгликоля можно использовать для определения количества моноэтиленгликоля, необходимого для конкретного применения, например, в качестве антифриза для автомобиля.
Формула этиленгликоля
Химическая формула этиленгликоля: C2H6O2. Формула представляет количество атомов каждого элемента в молекуле этиленгликоля. Формула этиленгликоля важна для определения его свойств, таких как температура кипения, температура плавления и плотность. Формулу также можно использовать для расчета количества этиленгликоля, необходимого для конкретного применения.
Температура кипения этиленгликоля
Моноэтиленгликоль имеет температуру кипения 197,3°C (387,1°F) при атмосферном давлении. Точка кипения – это температура, при которой вещество переходит из жидкого состояния в газообразное. Высокая температура кипения моноэтиленгликоля делает его эффективной охлаждающей жидкостью и антифризом для использования в автомобилях и других устройствах.
Температура плавления этиленгликоля
Моноэтиленгликоль имеет температуру плавления -12,9°C (8,8°F). Точка плавления – это температура, при которой вещество переходит из твердого состояния в жидкое. Низкая температура плавления моноэтиленгликоля позволяет ему оставаться жидким при низких температурах, что делает его эффективной охлаждающей жидкостью для использования в холодном климате.
Плотность этиленгликоля г/мл
Плотность моноэтиленгликоля составляет 1,11 г/мл при 20°C (68°F). Плотность – это мера количества массы, содержащейся в определенном объеме. Высокая плотность моноэтиленгликоля делает его эффективной охлаждающей жидкостью и антифризом для использования в автомобилях и других устройствах, где пространство ограничено.
Молекулярный вес этиленгликоля
Молекулярная масса моноэтиленгликоля составляет 62,07 г/моль. Молекулярная масса – это сумма атомных весов всех атомов молекулы. Молекулярная масса моноэтиленгликоля важна при определении количества моноэтиленгликоля, необходимого для конкретного применения, например, в качестве антифриза для автомобиля.
Структура этиленгликоля
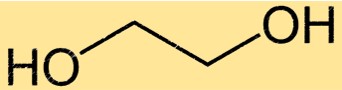
Моноэтиленгликоль имеет простую химическую структуру, состоящую из двух гидроксильных групп, присоединенных к двухуглеродной цепи. Молекулярная формула моноэтиленгликоля — C2H6O2, а его название IUPAC — этан-1,2-диол. Простая структура моноэтиленгликоля делает его эффективным растворителем и антифризом для использования в различных областях применения.
| Появление | Прозрачная жидкость без запаха |
| Удельный вес | 1,113 при 20°С |
| Цвет | Бесцветный |
| Запах | Без запаха |
| Молярная масса | 62,07 г/моль |
| Плотность | 1,11 г/см³ |
| Точка плавления | -12,9°С (8,8°Ф) |
| Точка кипения | 197,3°С (387,1°Ф) |
| Мигающая точка | 111°С (232°Ф) |
| Растворимость в воде | смешивается |
| Растворимость | Растворим в ацетоне, спиртах, бензоле и эфире. |
| Давление газа | 0,08 мм рт.ст. при 25°C |
| Плотность пара | 2,14 (воздух = 1) |
| пКа | 14,0 (первый), 13,2 (второй) |
| рН | Нейтральный |
Безопасность и опасность этиленгликоля
Хотя моноэтиленгликоль имеет множество практических применений, он также представляет ряд рисков для здоровья человека и окружающей среды. Моноэтиленгликоль очень токсичен при проглатывании и может вызвать серьезные проблемы со здоровьем, включая почечную недостаточность и даже смерть. Вдыхание паров моноэтиленгликоля может вызвать раздражение дыхательных путей и центральной нервной системы. Моноэтиленгликоль также легко воспламеняется и может бурно реагировать с некоторыми химическими веществами. Поэтому с ним необходимо обращаться осторожно и правильно хранить. Кроме того, моноэтиленгликоль вреден для водной флоры и фауны, и его нельзя сбрасывать в водные пути или окружающую среду. При обращении с моноэтиленгликолем необходимо принимать соответствующие меры безопасности, чтобы избежать несчастных случаев и защитить здоровье человека и окружающую среду.
| Символы опасности | Череп и скрещенные кости, коррозийные |
| Описание безопасности | Не глотать. Избегайте контакта с кожей и глазами. Используйте при достаточной вентиляции. Надевайте защитные перчатки и защитные очки. |
| Идентификационные номера ООН | ООН 3082 |
| код ТН ВЭД | 2905.32.00 |
| Класс опасности | 6.1 (токсичный) |
| Группа упаковки | II |
| Токсичность | Очень токсичен при проглатывании. Может вызвать почечную недостаточность и другие серьезные проблемы со здоровьем. Вдыхание паров может вызвать раздражение дыхательных путей и воздействие на центральную нервную систему. |
Методы синтеза этиленгликоля
Существует несколько методов синтеза моноэтиленгликоля, ключевого элемента во многих промышленных процессах.
Распространенным методом является каталитическая гидратация оксида этилена , которая включает реакцию оксида этилена с водой в присутствии катализатора, такого как сильная кислота или оксид металла.
Другой метод заключается в гидролизе этиленкарбоната, который образуется в результате реакции оксида этилена с диоксидом углерода.
Другой способ синтеза моноэтиленгликоля — окисление этилена. В этом процессе используется катализатор на основе оксида серебра для окисления этилена с образованием оксида этилена , который затем подвергается гидролизу с образованием моноэтиленгликоля.
Для синтеза моноэтиленгликоля щавелевую кислоту можно восстановить водородом, в результате чего образуется гликолевая кислота. В дальнейшем при дегидратации гликолевой кислоты образуется моноэтиленгликоль.
Использование этиленгликоля
Моноэтиленгликоль имеет множество промышленных и коммерческих применений благодаря своим уникальным свойствам и универсальности. Некоторые из его основных применений включают в себя:
- Антифриз: используется в качестве охлаждающей жидкости и антифриза в автомобильной и промышленной технике. Низкая температура замерзания и высокая температура кипения делают его идеальным выбором для предотвращения повреждения двигателя от замерзания или перегрева.
- Противообледенительный агент: используется в качестве противообледенительного средства для самолетов, дорог и тротуаров благодаря своей способности снижать температуру замерзания воды.
- Растворитель: очень эффективный растворитель для широкого спектра веществ, включая смолы, масла и красители. Производители обычно используют его при производстве красок, покрытий и клеев.
- Увлажнитель: используется в качестве увлажнителя в косметической промышленности и индустрии личной гигиены, чтобы предотвратить потерю влаги в таких продуктах, как лосьоны и шампуни.
- Химический промежуточный продукт: используется в качестве ключевого промежуточного продукта в производстве широкого спектра химикатов, включая полиэфирные волокна и пленки, полиуретаны и пластификаторы.
- Теплоноситель: используется в качестве теплоносителя в различных промышленных применениях, включая системы отопления, вентиляции и кондиционирования, солнечные коллекторы и геотермальные системы.
Вопросы:
Вопрос: Что такое этиленгликоль?
Ответ: Моноэтиленгликоль представляет собой прозрачную бесцветную жидкость без запаха и сладкого вкуса, которая обычно используется в качестве охлаждающей жидкости и антифриза в автомобильной и промышленной технике. Он также используется в качестве растворителя, увлажнителя и химического промежуточного продукта в различных отраслях промышленности.
Вопрос: Каково давление пара этиленгликоля при его нормальной температуре кипения?
A: Давление паров моноэтиленгликоля при его нормальной температуре кипения 197,3°C (387,1°F) составляет 0,00131 атм.
Вопрос: Полярен ли этиленгликоль?
Ответ: Да, моноэтиленгликоль является полярной молекулой из-за наличия двух функциональных групп -OH, которые создают дипольный момент и позволяют ему растворяться в полярных растворителях.
Вопрос: Как измерить pH этиленгликоля?
Ответ: pH моноэтиленгликоля можно измерить с помощью pH-метра или индикаторных полосок pH, специально разработанных для использования с неводными растворителями. Важно отметить, что моноэтиленгликоль – это не нейтральное вещество, а слабая кислота с pH около 6,5.
Вопрос: Как этиленгликоль влияет на организм?
Ответ: Моноэтиленгликоль может быть токсичным при проглатывании или всасывании через кожу, поскольку он метаболизируется в печени до токсичных побочных продуктов, которые могут вызвать почечную недостаточность, судороги и даже смерть. Симптомы отравления моноэтиленгликолем включают головную боль, головокружение, тошноту, рвоту и спутанность сознания.
Вопрос: Какую формулу представляет 1,2-этандиол?
Ответ: Формула 1,2-этандиола, также известного как моноэтиленгликоль, — C2H6O2.
Вопрос: Каковы прогнозы Ньюмана по 1,2-этандиолу?
A: Проекции Ньюмана для 1,2-этандиола показывают две смещенные конформации, при этом группы -OH ориентированы в затменном или смещенном положении относительно друг друга.
