Цианид натрия – высокотоксичное соединение, используемое в различных отраслях промышленности. Он выделяет ионы цианида, которые мешают клеточному дыханию, вызывая серьезные риски для здоровья и даже смерть.
| Название ИЮПАК | Цианид натрия |
| Молекулярная формула | NaCN |
| Количество CAS | 143-33-9 |
| Синонимы | Цианогран, цианид натрия, цианидная соль, цианид натрия |
| ИнЧИ | InChI=1S/CN.Na/c1-2;/h1H;/q-1;+1 |
Свойства цианида натрия
Формула цианида натрия
Формула цианида натрия — NaCN. Он состоит из катиона Na+ и аниона CN. Это химическое соединение широко используется в различных промышленных процессах.
цианид натрия Молярная масса
Молярная масса NaCN рассчитывается путем сложения атомных масс составляющих его элементов: натрия (Na) и углерода (C) плюс азота (N). Молярная масса NaCN составляет примерно 49,01 грамм на моль.
Температура кипения цианида натрия
NaCN имеет температуру кипения около 1496 градусов Цельсия. При этой температуре соединение претерпевает фазовый переход из жидкости в газ. Крайне важно обращаться с NaCN с осторожностью из-за его токсичности.
Цианид натрия Температура плавления
Температура плавления NaCN составляет около 564 градусов Цельсия. При этой температуре твердое соединение переходит в жидкое состояние. Следует соблюдать осторожность при обращении с NaCN, поскольку он представляет серьезную опасность для здоровья.
Плотность цианида натрия г/мл
Плотность NaCN составляет примерно 1,6 грамма на миллилитр. Это значение плотности указывает на массу вещества в единице объема. Высокая плотность NaCN способствует его стабильности и облегчает его использование в различных приложениях.
Цианид натрия Молекулярный вес
Молекулярная масса NaCN составляет примерно 49,01 грамма на моль. Это значение представляет собой сумму атомных весов составляющих его элементов. Молекулярная масса NaCN имеет решающее значение для определения количества соединения, необходимого для химических реакций.
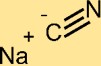
Структура цианида натрия
NaCN имеет кристаллическую структуру, состоящую из катионов Na+ и анионов CN-. Цианид-ион состоит из атома углерода, связанного с атомом азота. Структура NaCN играет важную роль в его реакционной способности и химическом поведении.
Растворимость цианида натрия
NaCN хорошо растворим в воде, его растворимость составляет примерно 46 граммов на 100 миллилитров при комнатной температуре. Такая высокая растворимость позволяет эффективно растворять и использовать NaCN в различных процессах.
| Появление | Белое кристаллическое твердое вещество |
| Удельный вес | 1,6 г/мл |
| Цвет | Белый |
| Запах | Без запаха |
| Молярная масса | 49,01 г/моль |
| Плотность | 1,6 г/мл |
| Точка плавления | 564°С |
| Точка кипения | 1496°С |
| Мигающая точка | Непригодный |
| Растворимость в воде | Растворимый |
| Растворимость | Растворим в воде, аммиаке, метаноле, этаноле. |
| Давление газа | Нет в наличии |
| Плотность пара | Нет в наличии |
| пКа | Нет в наличии |
| рН | Щелочной |
Безопасность и опасность цианида натрия
NaCN представляет значительные риски и опасности для безопасности из-за своей токсичной природы. Воздействие этого соединения может вызвать серьезные последствия для здоровья. Он мешает клеточному дыханию, препятствуя доставке кислорода к жизненно важным органам, что может привести к дыхательной недостаточности, остановке сердца и даже смерти. Вдыхание или проглатывание NaCN может вызвать быстрые и потенциально смертельные симптомы. Обращение с NaCN требует особой осторожности, включая использование соответствующих средств индивидуальной защиты (СИЗ) и соблюдение протоколов безопасности. Крайне важно правильно хранить, транспортировать и утилизировать NaCN, чтобы избежать случайного выброса или загрязнения. Регулярное обучение и осведомленность необходимы для минимизации рисков, связанных с NaCN.
| Символы опасности | Череп и кости |
| Описание безопасности | Очень токсичен |
| Идентификационные номера ООН | 1689 год |
| код ТН ВЭД | 2837.11.00 |
| Класс опасности | 6.1 |
| Группа упаковки | я |
| Токсичность | Смертельно опасен для человека. Он выделяет цианистый водород, высокотоксичное химическое удушающее вещество, которое мешает организму использовать кислород. |
Методы синтеза цианида натрия
Существует несколько методов синтеза NaCN, каждый из которых предполагает реакцию соответствующих реагентов. Распространенным методом является процесс Кастнера. В этом процессе расплавленная смесь карбоната натрия , углерода и газообразного азота подвергается воздействию электрического тока, генерируя NaCN. Затем соберите затвердевший NaCN.
В другом методе гидроксид натрия реагирует с газообразным HCN. Смешайте воду с гидроксидом натрия , чтобы получить раствор, и подвергните раствор воздействию газообразного HCN. Следовательно, NaCN и вода образуют побочные продукты.
Кроме того, синтез NaCN включает реакцию между металлом Na и газообразным цианистым водородом. Вводят газ в металлический натрий, вызывая бурную реакцию с образованием NaCN и газообразного водорода.
Важно отметить, что синтез NaCN должен проводиться только обученными специалистами в хорошо оборудованных помещениях. Процесс требует строгого соблюдения протоколов безопасности из-за высокотоксичной природы соединения.
Использование цианида натрия
NaCN имеет различные применения в различных отраслях промышленности благодаря своим уникальным свойствам. Вот некоторые распространенные варианты использования:
- Добыча золота: В добыче золота широко используется NaCN для извлечения драгоценных металлов из руд. Он образует комплекс с золотом, облегчая разделение и очистку металла.
- Металлическое покрытие: в процессах гальваники используется NaCN для нанесения слоя металла на поверхности. Позволяет сформировать защитно-декоративное покрытие, улучшающее долговечность и внешний вид.
- Химический синтез: NaCN служит прекурсором для синтеза различных органических соединений при производстве фармацевтических препаратов, пластмасс, красителей и других химикатов.
- Борьба с вредителями: NaCN действует как фумигант для борьбы с вредителями в определенных условиях сельского хозяйства. Он уничтожает грызунов и вредителей, которые могут нанести ущерб посевам и хранимой продукции.
- Науглероживание: NaCN способствует науглероживанию — процессу, который повышает твердость поверхности стальных предметов. Он образует твердый внешний слой, повышающий устойчивость к износу и коррозии.
- Изготовление ювелирных изделий: В ювелирном производстве используется NaCN для очистки, полировки и травления металлов. Это помогает добиться желаемого качества поверхности и удалить загрязнения.
- Лабораторные исследования: NaCN находит применение в различных лабораторных экспериментах и исследованиях, особенно в области химии, биохимии и металлургии.
Вопросы:
Вопрос: Для чего используется цианид натрия?
Ответ: NaCN используется в добыче золота, металлизации, химическом синтезе, борьбе с вредителями, цементации, производстве ювелирных изделий и лабораторных исследованиях.
Вопрос: Как сделать цианид натрия?
Ответ: NaCN можно синтезировать такими методами, как процесс Кастнера, реакция с гидроксидом натрия и газообразным HCN или реакция металлического натрия с газообразным HCN.
Вопрос: Сколько всего атомов содержится в 9,203 е-22 молях цианида натрия?
A: В 9,203 е-22 моль NaCN общее количество атомов можно рассчитать на основе числа Авогадро, которое составляет примерно 6,022 x 10^23 атома/моль.
Вопрос: Растворяется ли цианид натрия в воде?
Ответ: Да, NaCN хорошо растворяется в воде.
Вопрос: Цианид натрия образует Sn2?
Ответ: NaCN может участвовать в реакциях SN2 (бимолекулярного нуклеофильного замещения).
Вопрос: Смертелен ли цианид натрия?
Ответ: Да, NaCN очень токсичен и может быть смертельным при неправильном обращении.
Вопрос: Как цианид натрия используется в горнодобывающей промышленности?
Ответ: NaCN используется в горнодобывающей промышленности для добычи золота, где он образует комплекс с золотом, что облегчает его отделение от руды.
Вопрос: Как потушить цианид натрия?
Ответ: NaCN можно деактивировать, добавив подходящий дезактивирующий агент, например перекись водорода или гипохлорит натрия, чтобы превратить его в менее токсичные вещества.
Вопрос: Какой основной продукт образуется при обработке (R)1-бром-4-метилгексана цианидом натрия?
Ответ: Основным продуктом, образующимся при обработке (R)1-бром-4-метилгексана NaCN, является (R)4-метилгексаннитрил.
Вопрос: Что из перечисленного медленнее всего реагирует с NaCN?
Ответ: Реакционная способность с NaCN может варьироваться, но первичные алкилгалогениды обычно реагируют медленнее, чем вторичные или третичные алкилгалогениды.
Вопрос: Ингибирует ли цианид работу насоса Na-K?
Ответ: Да, CN ингибирует натриево-калиевый насос, который имеет решающее значение для поддержания правильной клеточной функции.
