Фосфат магния (Mg3(PO4)2) представляет собой соединение, состоящее из ионов магния и фосфата. Он играет жизненно важную роль во многих биологических процессах, таких как синтез ДНК, функция нервов и сокращение мышц.
| Название ИЮПАК | фосфат магния |
| Молекулярная формула | Mg3(PO4)2 |
| Количество CAS | 7757-87-1 |
| Синонимы | Фосфат тримагния, ортофосфат тримагния, ортофосфат магния, третичный фосфат магния, трехосновный фосфат магния |
| ИнЧИ | InChI=1S/2Mg.3H3O4P/c;;3 1-5(2,3)4/h;;3 (H3,1,2,3,4)/q2*+2;;;/p-6 |
Свойства фосфата магния
Формула фосфата магния
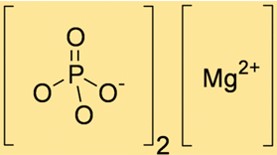
Химическая формула фосфата магния — Mg3(PO4)2, что указывает на то, что он содержит три иона Mg+2 и два иона PO43-. Формула важна для стехиометрических расчетов и помогает определить правильное количество реагентов и продуктов химических реакций с участием Mg3(PO4)2.
Молярная масса фосфата магния
Mg3(PO4)2 имеет молярную массу 262,86 г/моль. Эта величина представляет собой массу одного моля соединения Mg3(PO4)2, которое представляет собой комбинацию трех ионов Mg+2 и двух ионов PO4-. Молярная масса — важнейшее свойство, используемое в стехиометрических расчетах для определения количества Mg3(PO4)2, необходимого в различных химических реакциях.
Температура кипения фосфата магния
Mg3(PO4)2 не имеет определенной температуры кипения, поскольку он разлагается, не достигнув точки кипения. При высоких температурах Mg3(PO4)2 разлагается на оксид магния и пятиокись фосфора, температуры кипения которых составляют 3600°С и 300°С соответственно. Температура разложения Mg3(PO4)2 зависит от различных факторов, таких как концентрация, скорость нагрева и давление.
Температура плавления фосфата магния
Mg3(PO4)2 имеет температуру плавления 1188°С. При этой температуре соединение претерпевает фазовый переход из твердого состояния в жидкое. На температуру плавления Mg3(PO4)2 влияют различные факторы, включая давление, примеси и кристаллическую структуру.
Плотность фосфата магния г/мл
Плотность Mg3(PO4)2 варьируется в зависимости от кристаллической структуры и условий ее измерения. Наиболее распространенная форма Mg3(PO4)2, три-Mg3(PO4)2, имеет плотность 2,195 г/мл. Значение плотности важно для определения массы Mg3(PO4)2, необходимой для достижения определенного объема в различных применениях.
Молекулярный вес фосфата магния
Mg3(PO4)2 имеет молекулярную массу 262,86 г/моль. Это значение рассчитывается путем сложения атомных масс ионов Mg и PO43-, присутствующих в соединении. Молекулярная масса Mg3(PO4)2 полезна для определения количества Mg3(PO4)2, необходимого в различных химических реакциях.
Структура фосфата магния
Mg3(PO4)2 имеет кристаллическую структуру, меняющуюся в зависимости от способа и условий получения. Наиболее распространенной формой является три-Mg3(PO4)2, кристаллическая структура которого состоит из ионов Mg+2 и ионов PO43-, расположенных в гексагональной решетке. Кристаллическая структура влияет на физические и химические свойства Mg3(PO4)2.
| Появление | Белый кристаллический порошок |
| Удельный вес | 2.195 |
| Цвет | Белый |
| Запах | Без запаха |
| Молярная масса | 262,86 г/моль |
| Плотность | 2195 г/мл |
| Точка плавления | 1188°С |
| Точка кипения | Разлагается до точки кипения |
| Мигающая точка | Непригодный |
| Растворимость в воде | нерастворимый |
| Растворимость | Растворим в кислотах |
| Давление газа | Непригодный |
| Плотность пара | Непригодный |
| пКа | 7.2 |
| рН | 8-9 (10% раствор) |
Безопасность и опасность фосфата магния
Mg3(PO4)2 обычно считается безопасным и нетоксичным. Он не классифицируется как опасный материал и не представляет существенного риска для здоровья человека и окружающей среды. Однако длительное воздействие высоких концентраций пыли Mg3(PO4)2 может вызвать раздражение дыхательных путей. Проглатывание большого количества Mg3(PO4)2 может вызвать раздражение желудочно-кишечного тракта и тошноту. Важно обращаться с Mg3(PO4)2 осторожно и носить соответствующие средства индивидуальной защиты при работе с большими количествами соединения. Любые разливы или утечки следует немедленно убирать, чтобы избежать риска поскользнуться или упасть.
| Символы опасности | Никто |
| Описание безопасности | Не классифицируется как опасный |
| Идентификационные номера ООН | Непригодный |
| код ТН ВЭД | 2835.29.10 |
| Класс опасности | Неклассифицированный |
| Группа упаковки | Непригодный |
| Токсичность | Нетоксичен при нормальных концентрациях. |
Методы синтеза фосфата магния
Mg3(PO4)2 можно синтезировать несколькими методами, включая осаждение, реакцию оксида магния с фосфорной кислотой и реакцию гидроксида магния с фосфорной кислотой.
Процесс осаждения включает добавление растворимой фосфатной соли, такой как Na3PO4, к раствору, содержащему растворимую соль Mg+2, такую как MgCl2 или сульфат магния. Затем при смешивании двух растворов образуется осадок Mg3(PO4)2, который можно собрать и высушить.
Реакция включает добавление оксида магния к раствору фосфорной кислоты и нагревание смеси до завершения реакции. Затем в процессе собираются и промываются образующийся Mg3(PO4)2 для удаления любых примесей.
Реакция включает добавление гидроксида магния к раствору фосфорной кислоты и нагревание смеси до завершения. Затем соберите образовавшийся Mg3(PO4)2 и тщательно промойте его от всех примесей.
В зависимости от качества сырья и условий реакции этими методами можно получать Mg3(PO4)2 различной степени чистоты.
Использование фосфата магния
Mg3(PO4)2 находит применение в различных отраслях промышленности, в том числе:
- Пищевая промышленность: используется в качестве пищевой добавки для регулирования уровня кислотности и улучшения текстуры и качества хлебобулочных изделий, молочных продуктов и напитков.
- Сельское хозяйство: используется в качестве удобрения для обеспечения растений необходимыми питательными веществами, такими как магний и фосфор.
- Фармацевтическая промышленность: используется в качестве активного ингредиента в антацидах и слабительных средствах, помогающих облегчить симптомы расстройства желудка и запора.
- Водоочистка: используется в качестве химиката для очистки воды для контроля образования накипи в котлах и трубах, а также для предотвращения коррозии.
- Керамическая промышленность: используется в качестве керамического связующего для повышения прочности и долговечности керамических изделий.
- Огнезащитный состав: используется в качестве огнезащитного средства в строительных материалах, таких как изоляция, гипсокартон и сайдинг.
- Косметика: используется в косметике и средствах личной гигиены в качестве загустителя и эмульгатора.
Вопросы:
Вопрос: Какова правильная формула соединения, образующегося между ионами Mg+2 и PO43-?
Ответ: Правильная формула соединения, образующегося между ионами Mg+2 и ионами PO43-, — Mg3(PO4)2.
Вопрос: Какова формула фосфата магния?
Ответ: Формула фосфата магния: Mg3(PO4)2.
Вопрос: Сколько ионов составляет одну формульную единицу фосфата магния?
Ответ: Одна формульная единица Mg3(PO4)2 содержит 11 ионов: три иона Mg+2 и два иона PO43-.
Вопрос: Растворим ли фосфат магния?
A: Mg3(PO4)2 плохо растворяется в воде, его растворимость составляет примерно 0,1 г/100 мл при комнатной температуре.
Вопрос: Кислота (x) реагирует с основанием (y) с образованием Mg3(PO4)2. Что такое х и у?
A: Кислота (x) — фосфорная кислота (H3PO4), а основание (y) — гидроксид магния (Mg(OH)2).
Вопрос: Какова молярная масса Mg3(PO4)2, вещества, ранее использовавшегося в медицине в качестве антацида?
A: Молярная масса Mg3(PO4)2 составляет 262,86 г/моль.
Вопрос: Растворим ли Mg3(PO4)2 в воде?
A: Mg3(PO4)2 плохо растворяется в воде, его растворимость составляет примерно 0,1 г/100 мл при комнатной температуре.
Вопрос: Сколько молей атомов кислорода содержится в одном моле Mg3(PO4)2?
Ответ: Один моль Mg3(PO4)2 содержит 8 молей атомов кислорода.
