Силикат натрия (Na2SiO3) представляет собой соединение натрия, кремния и кислорода. Он имеет множество применений, в том числе в качестве моющего средства, клея и при производстве силикагеля.
| Название ИЮПАК | Метасиликат натрия |
| Молекулярная формула | Na2SiO3 |
| Количество CAS | 6834-92-0 |
| Синонимы | Жидкое стекло, жидкое стекло, растворимое стекло, ортосиликат натрия, силикат натрия, метасиликат натрия. |
| ИнЧИ | InChI=1S/2Na.O3Si/c;;1-4(2)3/q2*+1;-2 |
Свойства силиката натрия
Формула силиката натрия
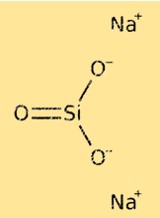
Формула силиката натрия — Na2SiO3, что указывает на то, что каждая единица соединения содержит два атома натрия, один атом кремния и три атома кислорода. Силикат натрия также известен под другими формулами, такими как Na2O·nSiO2 и Na2SiO4, в зависимости от количества звеньев SiO2 в полимерном анионе. Формула силиката натрия имеет решающее значение для понимания его химических свойств и расчета его молярной и молекулярной массы.
Силикат натрия Молярная масса
Na2SiO3 имеет молярную массу примерно 122,06 г/моль. Это рассчитывается путем сложения атомных масс натрия (22,99 г/моль), кремния (28,09 г/моль) и кислорода (16,00 г/моль), присутствующих в соединении. Молярная масса является важнейшим свойством Na2SiO3, поскольку она помогает определить количество соединения, необходимое для реакции.
Температура кипения силиката натрия
Температура кипения Na2SiO3 — это не отдельная величина, а диапазон температур. Растворы Na2SiO3, обычно используемые в промышленности, имеют температуру кипения от 100 до 110°C. Температура кипения Na2SiO3 зависит от таких факторов, как его концентрация, чистота и наличие примесей.
Температура плавления силиката натрия
Na2SiO3 не имеет четкой температуры плавления, поскольку при нормальных условиях он не существует в виде твердого соединения. Обычно он находится в твердом состоянии в виде порошков, гранул или комков. Эти твердые формы Na2SiO3 имеют разные температуры плавления, которые варьируются в зависимости от их состава и способа получения.
Плотность силиката натрия г/мл
Плотность растворов Na2SiO3 меняется в зависимости от их концентрации. Растворы Na2SiO3 с концентрацией 20 % имеют плотность около 1,14 г/мл, а с концентрацией 40 % — около 1,34 г/мл. Плотность твердого Na2SiO3 может варьироваться от 2,3 г/мл до 2,6 г/мл в зависимости от его чистоты и размера частиц.
Силикат натрия Молекулярный вес
Молекулярная масса Na2SiO3, также известная как формула веса, представляет собой сумму атомных весов всех атомов, присутствующих в соединении. Молекулярная масса Na2SiO3 составляет примерно 122,06 г/моль. Знание молекулярной массы соединения необходимо для определения количества соединения, необходимого для конкретной реакции.
Структура силиката натрия
Силикат натрия представляет собой неорганическое соединение, состоящее из катионов натрия и полимерных силикат-анионов. Структура силиката натрия может меняться в зависимости от его состава и способа получения. Обычно это выражается формулой Na2O.nSiO2, где n представляет собой количество звеньев SiO2 в полимерном анионе. Полимерные силикатные анионы имеют трехмерную сетчатую структуру, в которой атомы кремния тетраэдрически координированы с атомами кислорода.
| Появление | Бесцветное или белое твердое вещество, жидкость или порошок. |
| Удельный вес | 1,4-1,6 |
| Цвет | Бесцветный |
| Запах | Без запаха |
| Молярная масса | 122,06 г/моль |
| Плотность | 1,14-1,34 г/мл (раствор); 2,3–2,6 г/мл (твердый) |
| Точка плавления | Нет четкой точки плавления |
| Точка кипения | 100-110°С (раствор) |
| Мигающая точка | Непригодный |
| Растворимость в воде | Растворимый |
| Растворимость | Растворим в воде и этаноле; слабо растворим в метаноле и ацетоне |
| Давление газа | Непригодный |
| Плотность пара | Непригодный |
| пКа | ~9,8 |
| рН | 11-12 (решение) |
Безопасность и вред силиката натрия
Na2SiO3 может быть опасен при неправильном обращении. Это едкое соединение, которое при контакте может вызвать сильное раздражение кожи и глаз. Вдыхание пыли или тумана Na2SiO3 может вызвать раздражение дыхательных путей и повреждение легких. Растворы Na2SiO3 также очень щелочные и могут вызвать химические ожоги кожи и слизистых оболочек. При работе с Na2SiO3 следует использовать соответствующие средства индивидуальной защиты, такие как перчатки и средства защиты глаз. В случае попадания на кожу или в глаза необходимо немедленно промыть водой. Na2SiO3 также следует хранить в прохладном, сухом, хорошо проветриваемом помещении вдали от несовместимых материалов.
| Символы опасности | Коррозионное, Раздражающее |
| Описание безопасности | Храните в недоступном для детей месте. Избегайте контакта с глазами, кожей и одеждой. Надевайте защитные перчатки/защитную одежду/защиту глаз/лица. ПРИ ПОПАДАНИИ НА КОЖУ: Промыть большим количеством воды. ПРИ ПОПАДАНИИ В ГЛАЗА: осторожно промыть водой в течение нескольких минут. Снимите контактные линзы, если они есть и это легко сделать. Продолжайте полоскание. ПРИ ПРОГЛАТЫВАНИИ: Прополоскать рот. Не вызывает рвоту. Если вы плохо себя чувствуете, позвоните в ТОКСИКОЛОГИЧЕСКИЙ ЦЕНТР или к врачу. |
| Идентификационные номера ООН | ООН2922, ООН1824 |
| код ТН ВЭД | 2839.90.90 |
| Класс опасности | 8 |
| Группа упаковки | III |
| Токсичность | LD50 (перорально, крыса) = 1,280 мг/кг; LC50 (при вдыхании, крыса) >2,28 мг/л/4 часа |
Методы синтеза силиката натрия
Существует несколько методов синтеза Na2SiO3.
Распространенным методом является сплавление кремнезема с карбонатом натрия при высоких температурах, в результате чего в качестве побочных продуктов образуются Na2SiO3 и диоксид углерода.
Другой метод включает реакцию гидроксида натрия с кремнеземом в сосуде высокого давления при высоких температурах. Для получения нужной концентрации разбавьте высококонцентрированный раствор Na2SiO3 водой.
Третий метод включает растворение силикагеля в растворе гидроксида натрия , затем нагревание и перемешивание смеси для ускорения реакции. Этот метод дает прозрачный бесцветный раствор Na2SiO3.
Микроволновое излучение способно нагревать реагенты, синтезируя Na2SiO3.
Эти методы позволяют получить Na2SiO3 с более высокой чистотой и выходом, чем традиционные методы синтеза.
Кроме того, в некоторых исследованиях изучалось использование возобновляемых ресурсов, таких как зола рисовой шелухи и зола жома сахарного тростника, в качестве источников кремнезема для синтеза Na2SiO3, что обеспечивает более устойчивый подход к производству.
Использование силиката натрия
Na2SiO3 — универсальное соединение, имеющее множество применений в различных отраслях промышленности. Некоторые из распространенных применений Na2SiO3:
- Клеи и связующие: используются в качестве связующего в различных областях применения, таких как картон, гофрированные коробки и фанера.
- Моющие средства и мыло: используется в стиральных порошках в качестве щелочного буфера и средства, препятствующего повторному осаждению.
- Водоочистка: используется при очистке воды в качестве коагулянта и ингибитора коррозии.
- Конструкция: Также используется в качестве упрочнителя бетона и стабилизатора грунта.
- Керамика: используется в качестве связующего при производстве керамики.
- Текстиль и бумага: используется в качестве проклеивающего вещества при производстве бумаги и в качестве антипирена в текстиле.
- Автомобильная промышленность: используется в качестве герметика и присадки к охлаждающей жидкости в автомобильной промышленности.
- Сельское хозяйство: используется в качестве опрыскивания листьев для улучшения роста растений и в качестве удобрения для уменьшения уплотнения почвы и увеличения удержания воды.
- Противопожарная защита: используется в качестве антипирена в различных материалах, таких как дерево, ткань и бумага.
- Средства личной гигиены: используется в некоторых зубных пастах и дезодорантах в качестве связующего вещества и агента контроля вязкости.
Вопросы:
Вопрос: Является ли силикат натрия токсичным?
Ответ: Na2SiO3 может быть токсичным при проглатывании или вдыхании в больших количествах. Он может раздражать глаза, кожу и дыхательную систему. Однако при использовании в соответствии с правилами техники безопасности, например при ношении соответствующих средств индивидуальной защиты, обращение с Na2SiO3, как правило, безопасно.
Вопрос: Как вылечить Na2SiO3?
Ответ: Na2SiO3 затвердевает под воздействием углекислого газа, в результате чего жидкий Na2SiO3 затвердевает в твердое, похожее на стекло вещество. Время отверждения зависит от концентрации раствора Na2SiO3, а также температуры и влажности среды отверждения. Обычно для полного затвердевания Na2SiO3 требуется несколько дней.
Вопрос: Можно ли красить бетон, обработанный силикатом натрия?
О: Да, можно красить бетон, обработанный Na2SiO3, но поверхность должна быть правильно подготовлена. Na2SiO3 должен полностью затвердеть, затем перед нанесением краски поверхность необходимо очистить и загрунтовать подходящей грунтовкой.
Вопрос: Где купить силикат натрия рядом со мной?
О: Na2SiO3 можно приобрести у поставщиков химической продукции, промышленных поставщиков и интернет-магазинов. Важно убедиться, что поставщик пользуется хорошей репутацией, а Na2SiO3 имеет высокое качество и подходит для предполагаемого применения. Также важно соблюдать правила обращения и безопасности при покупке и использовании Na2SiO3.
