Перманганат калия (KMnO4) представляет собой кристаллическое соединение пурпурного цвета, используемое для различных целей, таких как дезинфекция воды, лечение кожных заболеваний и в качестве лабораторного реагента. Его также можно использовать в качестве мощного окислителя.
| Название ИЮПАК | Перманганат калия |
| Молекулярная формула | КМnO4 |
| Количество CAS | 7722-64-7 |
| Синонимы | Перманганат калия, кристаллы Конди, минерал хамелеон, гиперманган, калий гиперманганикум. |
| ИнЧИ | InChI=1S/K.Mn.4O/q+1;;;;-1 |
Свойства марганцовки
Формула перманганата калия
Химическая формула перманганата калия — KMnO4. Он состоит из иона калия (К+), иона марганца (MnO4^-) и четырех атомов кислорода (О). В формуле указывается тип и количество атомов, входящих в состав соединения. Он используется для написания химических уравнений и для расчета массы и количества атомов, присутствующих в заданном количестве вещества.
Молярная масса перманганата калия
KMnO4 имеет молярную массу 158 034 г/моль. Это означает, что один моль KMnO4, что эквивалентно 6,022 х 10^23 молекул, имеет массу 158,034 грамма. Молярная масса соединения рассчитывается путем сложения атомных масс всех элементов, присутствующих в соединении. В случае KMnO4 молярная масса рассчитывается путем сложения атомных масс калия, марганца и кислорода.
Температура кипения марганцовки
KMnO4 не имеет определенной температуры кипения, поскольку он разлагается до достижения точки кипения. При атмосферном давлении KMnO4 начинает разлагаться около 240°C. При нагревании он сначала выделяет кислород и образует манганат калия, который затем разлагается на оксид калия и оксид марганца.
Температура плавления перманганата калия
KMnO4 имеет высокую температуру плавления 240°C. Это означает, что при температуре ниже 240°С KMnO4 будет существовать в твердом состоянии. При нагревании KMnO4 претерпевает ряд химических изменений, включая выделение кислорода и образование различных оксидов марганца.
Плотность перманганата калия г/мл
Плотность KMnO4 составляет 2,703 г/мл при комнатной температуре. Это означает, что один миллилитр KMnO4 весит 2,703 грамма. Плотность вещества – это отношение его массы к объему. В случае KMnO4 его высокая плотность делает его полезным для отделения его от других веществ путем фильтрации.
Молекулярный вес перманганата калия
Молекулярная масса KMnO4 составляет 158,034 г/моль. Это значение представляет собой среднюю массу молекулы KMnO4. Его рассчитывают путем сложения атомных масс калия, марганца и кислорода, входящих в состав соединения.
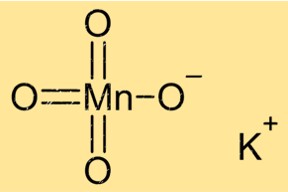
Структура перманганата калия
KMnO4 имеет кристаллическую структуру с моноклинной кристаллической системой. Его кристаллы фиолетового цвета и имеют призматическую форму. Соединение имеет октаэдрическую координационную геометрию с шестью атомами кислорода, окружающими центральный атом марганца. Ионы калия располагаются между слоями атомов марганца и кислорода.
| Появление | Кристаллическое твердое вещество темно-фиолетового цвета |
| Удельный вес | 2703 г/см³ |
| Цвет | Темно фиолетовый |
| Запах | Без запаха |
| Молярная масса | 158 034 г/моль |
| Плотность | 2703 г/см³ |
| Точка плавления | 240°С |
| Точка кипения | Разлагается перед кипячением |
| Мигающая точка | Непригодный |
| Растворимость в воде | 6,38 г/л при 20°C |
| Растворимость | Растворим в воде, этаноле, ацетоне. |
| Давление газа | Непригодный |
| Плотность пара | Непригодный |
| пКа | 2.17 |
| рН | 7,2 – 8,9 (1% раствор) |
Безопасность и вред марганцовки
KMnO4 может быть опасен при неправильном обращении. Это сильный окислитель, который может бурно реагировать с восстановителями, органическими соединениями и другими химическими веществами. Он может вызвать раздражение кожи и глаз и может быть вредным при проглатывании или вдыхании. Соединение может также оставлять пятна на коже и одежде. При работе с KMnO4 следует соблюдать соответствующие меры безопасности, включая ношение защитной одежды, очков и перчаток. Его следует хранить в прохладном, сухом, хорошо проветриваемом помещении вдали от несовместимых материалов. При попадании или проглатывании немедленно обратитесь за медицинской помощью.
| Символы опасности | О, Хн |
| Описание безопасности | С22, С26, С36/37/39, С45 |
| Идентификационные номера ООН | ООН 1490 |
| код ТН ВЭД | 28416100 |
| Класс опасности | 5.1 |
| Группа упаковки | II |
| Токсичность | Токсично при проглатывании или вдыхании. Может вызвать раздражение кожи и глаз. |
Методы синтеза перманганата калия
Синтезировать KMnO4 можно различными методами.
Один метод включает взаимодействие диоксида марганца с гидроксидом калия и окислителем, таким как хлор или перекись водорода.
Другой метод включает реакцию манганата калия с газообразным хлором .
Еще один метод включает взаимодействие гидроксида калия с диоксидом марганца и последующее окисление полученной смеси окислителем.
Процесс синтеза обычно включает нагрев реагентов до определенной температуры и поддержание температуры в течение определенного времени. Процесс заключается в фильтровании полученной смеси и получении KMnO4 кристаллизацией.
Использование перманганата калия
KMnO4 находит различное применение в ряде отраслей промышленности благодаря своим сильным окислительным свойствам. Вот некоторые распространенные варианты использования KMnO4:
- Водоочистка: используется для очистки воды в коммунальных и промышленных целях, поскольку позволяет удалять примеси и устранять неприятные запахи.
- Медицинское применение: применяется местно для лечения кожных заболеваний (экзема, дерматит и грибковые инфекции).
- Лабораторное использование: используется в качестве окислителя в различных лабораторных экспериментах и в качестве красителя в биологии для выделения клеток и тканей.
- Сельское хозяйство: используется в качестве фунгицида и бактерицида для защиты сельскохозяйственных культур от вредных вредителей и болезней.
- Химия: используется в аналитической химии для определения концентрации определенных химических веществ и в органической химии в качестве реагента в химических реакциях.
- Пожаротушение: используется в качестве антипирена и для тушения определенных типов пожаров.
- Промышленное применение: Используется в производстве химикатов, текстиля и аккумуляторов.
Вопросы:
Вопрос: Какой газ выделяется при расщеплении перманганата калия?
Ответ: При расщеплении KMnO4 выделяется газообразный кислород (O2).
Вопрос: Что такое перманганат калия?
Ответ: Перманганат калия — мощный окислитель с химической формулой KMnO4.
Вопрос: Какова химическая формула перманганата калия?
Ответ: Химическая формула перманганата калия — KMnO4.
Вопрос: Где купить кристаллы перманганата калия?
Ответ: Кристаллы KMnO4 можно приобрести у поставщиков химикатов, компаний, занимающихся поставками лабораторных материалов, и в интернет-магазинах.
Вопрос: Что такое KMnO4?
Ответ: KMnO4 — химическая формула перманганата калия.
Вопрос: Какова степень окисления марганца в KMnO4?
Ответ: Степень окисления марганца в KMnO4 равна +7.
Вопрос: Какова степень окисления кислорода в KMnO4?
Ответ: Степень окисления кислорода в KMnO4 равна -2.
Вопрос: Сколько молей в 25,0 граммах KMnO4?
Ответ: Чтобы рассчитать количество молей в 25,0 граммах KMnO4, нам нужно полученную массу разделить на молярную массу KMnO4. Молярная масса KMnO4 составляет 158,034 г/моль. Следовательно, в 25,0 граммах содержится примерно 0,158 моля KMnO4.
