Нитрат серебра (AgNO3) представляет собой химическое соединение, состоящее из серебра, азота и кислорода. Его широко используют в фотографии, медицине и в качестве лабораторного реагента для различных реакций.
| Название ИЮПАК | Нитрат серебра |
| Молекулярная формула | AgNO3 |
| Количество CAS | 7761-88-8 |
| Синонимы | Мононитрат серебра, соль азотной кислоты серебра (1+), нитрат серебра (I) |
| ИнЧИ | InChI=1S/Ag.NO3/c;2-1(3)4/q+1;-1 |
Свойства нитрата серебра
Формула нитрата серебра
Формула мононитрата серебра: AgNO3. Он состоит из одного атома серебра (Ag), одного атома азота (N) и трех атомов кислорода (О). Формула представляет соотношение атомов в молекуле мононитрата серебра.
Нитрат серебра Молярная масса
Молярную массу мононитрата серебра рассчитывают путем сложения атомных масс составляющих его элементов. Серебро имеет атомную массу 107,87 г/моль, азот имеет массу 14,01 г/моль и каждый атом кислорода имеет массу 16,00 г/моль. Их добавление дает молярную массу мононитрата серебра примерно 169,87 г/моль.
Температура кипения нитрата серебра
Мононитрат серебра имеет температуру кипения около 440 градусов по Цельсию (824 градуса по Фаренгейту). При этой температуре соединение претерпевает фазовый переход из жидкого состояния в газообразное. Точка кипения указывает на температуру, при которой давление паров вещества равняется атмосферному давлению.
Нитрат серебра Температура плавления
Температура плавления мононитрата серебра составляет примерно 209 градусов Цельсия (408 градусов по Фаренгейту). Это температура, при которой твердая форма мононитрата серебра превращается в жидкость. Температура плавления является характерным свойством вещества и помогает определить его физическое поведение в различных условиях.
Плотность нитрата серебра г/мл
Плотность мононитрата серебра составляет примерно 4,35 г/мл. Плотность – это мера количества массы, содержащейся в данном объеме. Его рассчитывают путем деления массы вещества на его объем. Плотность мононитрата серебра указывает на то, насколько он компактен или насколько сконцентрирован в конкретном пространстве.
Молекулярный вес нитрата серебра
Молекулярная масса мононитрата серебра, также называемая молярной массой, составляет примерно 169,87 г/моль. Он представляет собой сумму атомных масс всех атомов в молекуле мононитрата серебра. Молекулярная масса используется в различных расчетах и преобразованиях, включающих количества соединения.
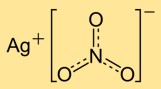
Структура нитрата серебра
Мононитрат серебра имеет кристаллическую структуру, состоящую из катионов серебра (Ag+) и нитрат-анионов (NO3-). Ионы серебра окружены нитрат-ионами, образуя регулярную сетку. Эта ионная структура способствует стабильности и свойствам соединения.
Растворимость нитрата серебра
Мононитрат серебра хорошо растворим в воде. Он легко растворяется в воде, образуя прозрачный бесцветный раствор. Растворимость мононитрата серебра в воде является важной характеристикой и играет решающую роль в различных приложениях, например, в медицине, фотографии и химических реакциях.
| Появление | Белое кристаллическое твердое вещество |
| Удельный вес | 4,35 г/мл |
| Цвет | Бесцветный |
| Запах | Без запаха |
| Молярная масса | 169,87 г/моль |
| Плотность | 4,35 г/мл |
| Точка плавления | 209°С (408°Ф) |
| Точка кипения | 440°С (824°Ф) |
| Мигающая точка | Непригодный |
| Растворимость в воде | Растворимый |
| Растворимость | Растворим в воде и органических растворителях, таких как этанол. |
| Давление газа | 0,26 мм рт.ст. при 25°C (77°F) |
| Плотность пара | Непригодный |
| пКа | – |
| рН | Кислый (приблизительно pH 5-6 в водном растворе) |
Безопасность и опасность нитрата серебра
Мононитрат серебра представляет некоторую угрозу безопасности, поэтому при обращении с ним следует соблюдать осторожность. Он считается вредным при проглатывании, вдыхании или при попадании на кожу или в глаза. Следует использовать защитные меры, такие как перчатки, защитные очки и лабораторные халаты. Это может вызвать раздражение, ожоги и пятна на коже и других поверхностях. При нагревании он может выделять токсичные оксиды азота. Его следует хранить в прохладном, сухом месте вдали от несовместимых веществ. Разливы следует оперативно устранять, а утилизацию отходов следует проводить в соответствии с соответствующими правилами во избежание загрязнения окружающей среды.
| Символы опасности | Коррозионное, Окисляющее |
| Описание безопасности | Вызывает серьезные ожоги кожи и повреждения глаз. |
| Идентификаторы Организации Объединенных Наций | ООН 1493 (мононитрат серебра твердый) |
| код ТН ВЭД | 2843.10.00 |
| Класс опасности | Класс 5.1 (Окисляющие материалы) |
| Группа упаковки | GE II (средний уровень) |
| Токсичность | Токсичен для водной флоры и фауны с долгосрочными последствиями. |
Методы синтеза нитрата серебра
Существуют различные методы синтеза мононитрата серебра.
Распространенный метод включает реакцию между металлическим серебром и азотной кислотой . В этом процессе разбавленная азотная кислота растворяет серебро с образованием мононитрата серебра. Другой метод включает реакцию оксида или карбоната серебра с азотной кислотой, в результате которой образуется мононитрат серебра.
Кроме того, реакция между хлоридом серебра и азотной кислотой также может привести к образованию мононитрата серебра. Азотная кислота растворяет хлорид серебра, вытесняя ионы хлорида и образуя мононитрат серебра.
Кроме того, реакция сульфата серебра с растворимой нитратной солью, такой как нитрат натрия, позволяет получить мононитрат серебра. Сульфат серебра реагирует с нитратной солью в водном растворе, приводя к образованию мононитрата серебра и растворимой сульфатной соли.
При реализации этих синтетических методов важно соблюдать соответствующие меры предосторожности и использовать агрессивные кислоты и потенциально токсичные соединения. Также следует соблюдать лабораторные протоколы и рекомендации для обеспечения точного приготовления и обращения с мононитратом серебра.
Применение нитрата серебра
Мононитрат серебра находит множество применений в различных областях. Вот некоторые распространенные приложения:
- Фотография. В традиционной черно-белой фотографии мононитрат серебра используется в качестве светочувствительного соединения, которое реагирует со светом, образуя частицы серебра и проявляя фотографические изображения.
- Медицина: В медицинских целях мононитрат серебра используется из-за его антисептических свойств при лечении ран. Его местное применение предотвращает инфекции, стимулирует заживление и лечит ожоги, язвы и другие кожные раны.
- Лабораторный реагент: мононитрат серебра служит универсальным лабораторным реагентом, позволяющим проводить различные химические реакции и использоваться в аналитической химии для обнаружения присутствия галогенидов и других соединений.
- Серебрение: в процессах гальваники используется мононитрат серебра для активного нанесения тонкого слоя серебра на различные поверхности. Такое использование обычно используется в декоративных целях и для обеспечения устойчивости к коррозии.
- Окрашивание и окрашивание: в гистологии и микроскопии мононитрат серебра используется в качестве красителя для активного улучшения видимости определенных структур в биологических образцах. Текстильная промышленность использует его для окраски тканей.
- Гравировка: Коррозионная природа мононитрата серебра позволяет его активно использовать при травлении узоров на стекле и зеркалах. Он выборочно удаляет поверхностные слои, создавая сложные узоры.
- Химическое образование: Образовательные учреждения активно используют мононитрат серебра для проведения химических экспериментов и демонстраций из-за его различных реакций и визуальных эффектов.
- Серебряный катализатор. В некоторых химических реакциях мононитрат серебра активно действует как катализатор, способствуя превращению реагентов в желаемые продукты.
Вопросы:
Вопрос: Растворим ли AgNO3 в воде?
О: Да, AgNO3 растворим в воде.
Вопрос: Что такое AgNO3?
Ответ: AgNO3 — это мононитрат серебра, химическое соединение, состоящее из серебра, азота и кислорода.
Вопрос: Каковы ионы-спектаторы в реакции между KCl(водный раствор) и AgNO3(водный раствор)?
A: В реакции между KCl(водн.) и AgNO3(водн.) ионами-спектаторами являются K+ и NO3-.
Вопрос: Какие ионы, если таковые имеются, являются ионами-спектаторами в реакции AgNO3(водн) + NaCl(водн) → AgCl(тв) + NaNO3(водн)?
Ответ: В реакции AgNO3(водн.) + NaCl(водн.) → AgCl(тв.) + NaNO3(водн.) ионами-спектаторами являются Na+ и NO3-.
Вопрос: Сколько молей меди необходимо для реакции с 5,8 молями AgNO3?
Ответ: Сбалансированное уравнение необходимо для определения количества молей Cu, необходимых для реакции с 5,8 молями AgNO3.
Вопрос: Какое из следующих соединений будет образовывать осадок с AgNO3?
A: Соединения, содержащие ионы Cl-, Br- или I-, образуют осадок AgNO3.
Вопрос: Является ли AgNO3 ионным соединением?
Ответ: Да, AgNO3 — ионное соединение.
Вопрос: Является ли AgNO3 сильным электролитом?
О: Да, AgNO3 — мощный электролит.
Вопрос: Проводит ли AgNO3 электричество?
О: Да, AgNO3 проводит электричество при растворении в воде.
Вопрос: Является ли нитрат серебра солью?
Ответ: Да, мононитрат серебра — это соль.
Вопрос: Могу ли я купить нитрат серебра?
О: Да, мононитрат серебра имеется в продаже.
Вопрос: Является ли нитрат серебра решением?
Ответ: Мононитрат серебра может существовать в твердой форме или в виде раствора, в зависимости от его состояния.
Вопрос: Как удалить пятно от нитрата серебра?
Ответ: Пятна мононитрата серебра можно удалить, обработав пораженный участок мягким восстановителем, например перекисью водорода или тиосульфатом натрия.
Вопрос: Растворяется ли нитрат серебра в воде?
Ответ: Да, мононитрат серебра растворим в воде.
Вопрос: Какой осадок образуется при смешивании растворов нитрата серебра и хромата калия?
А: При смешивании растворов мононитрата серебра и хромата калия образуется желтый осадок хромата серебра (Ag2CrO4).
Вопрос: Какова молярная масса нитрата серебра?
A: Молярная масса мононитрата серебра (AgNO3) составляет примерно 169,87 г/моль.
Вопрос: Металлическое серебро добавляют в раствор нитрата свинца(II). Что такое сбалансированная химическая реакция?
A: Сбалансированная химическая реакция: 2Ag + Pb(NO3)2 → 2AgNO3 + Pb.
