Сульфат железа (ii) представляет собой химическое соединение, содержащее ионы железа и сульфата. Его обычно используют при очистке воды и в качестве питательной добавки для растений.
| Название ИЮПАК | Сульфат железа(II) |
| Молекулярная формула | FeSO4 |
| Количество CAS | 7720-78-7 |
| Синонимы | Сернокислое железо, сернокислое железо, зеленый купорос, мелантерит, шомольнокит |
| ИнЧИ | InChI=1S/Fe.H2O4S/c;1-5(2,3)4/h;(H2,1,2,3,4)/q+2;/p-2 |
Свойства сульфата железа(ii)
Формула сульфата железа(II)
Химическая формула сульфата железа(II) — FeSO4. Эта формула указывает на то, что сульфат железа состоит из одного атома железа, одного атома серы и четырех атомов кислорода. Формула сульфата железа является важным параметром для расчета различных физических и химических свойств соединения, таких как молярная масса и молекулярная масса.
Сульфат железа(II) Молярная масса
Молярная масса сульфата железа составляет 151,91 г/моль. Эта величина представляет собой массу одного моля сульфата железа, который содержит 1 атом железа, 1 молекулу серы и 4 молекулы кислорода. Молярная масса является важным параметром для расчета различных физических и химических свойств сульфата железа, таких как плотность и концентрация.
Температура кипения сульфата железа(II)
Сульфат железа не имеет определенной температуры кипения, поскольку он подвергается разложению до достижения точки кипения. При атмосферном давлении он начинает разлагаться около 300°С. Это разложение включает потерю воды и триоксида серы, в результате чего остается оксид железа (III). Такое поведение разложения ограничивает использование сульфата железа при высоких температурах.
Сульфат железа(II) Температура плавления
Температура плавления сернокислого железа зависит от степени гидратации. Безводный сульфат железа плавится при 695°С, а образующийся гептагидрат плавится при 64°С. Сульфат железа может существовать в нескольких различных гидратированных формах, каждая из которых имеет разную температуру плавления. Температура плавления сульфата железа является важным параметром при определении наилучших условий для приготовления и обращения с соединением.
Плотность сульфата железа (II) г/мл
Плотность железного купороса варьируется в зависимости от степени гидратации. Безводный сульфат железа имеет плотность 3,65 г/мл, а гептагидратная форма — 1,897 г/мл. Плотность сульфата железа является важным параметром для расчета объема заданной массы соединения.
Сульфат железа(II) Молекулярный вес
Молекулярная масса сульфата железа составляет 151,91 г/моль. Это значение представляет собой сумму атомных весов составляющих атомов молекулы сульфата железа. Молекулярная масса является важным параметром для расчета различных физических и химических свойств сульфата железа, таких как температура кипения и растворимость.
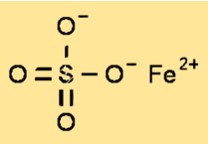
Структура сульфата железа(II)
Сульфат железа имеет кристаллическую структуру, относящуюся к моноклинной системе. Кристаллическая структура сульфата железа состоит из катионов железа (II), окруженных шестью молекулами воды и сульфат-анионами. Кристаллическая структура сульфата железа является важным параметром для понимания физических и химических свойств соединения.
| Появление | Белый или бледно-зеленый кристаллический порошок. |
| Удельный вес | 3,65 г/см3 (безводный) |
| Цвет | Бледно-зеленый |
| Запах | Без запаха |
| Молярная масса | 151,91 г/моль |
| Плотность | 3,65 г/см3 (безводный), 1,89 г/см3 (гептагидрат) |
| Точка плавления | 695°С (безводный), 64°С (гептагидрат) |
| Точка кипения | Разлагается до достижения точки кипения |
| Мигающая точка | Непригодный |
| Растворимость в воде | Очень растворим |
| Растворимость | Растворим в воде, нерастворим в этаноле. |
| Давление газа | Непригодный |
| Плотность пара | Непригодный |
| пКа | Непригодный |
| рН | 4 (0,1М раствор) |
Безопасность и опасность сульфата железа (ii)
Сульфат железа может представлять определенную опасность для здоровья и безопасности человека. При попадании он может вызвать раздражение и покраснение кожи и глаз, а вдыхание его пыли может вызвать раздражение дыхательных путей. Проглатывание может вызвать боль в животе, тошноту, рвоту и диарею. Кроме того, воздействие сульфата железа может вызвать профессиональную астму и пневмонит гиперчувствительности у восприимчивых людей. Важно соблюдать надлежащие процедуры обращения и хранения, носить соответствующие средства индивидуальной защиты и избегать вдыхания или проглатывания соединения. В случае случайного воздействия немедленно обратитесь за медицинской помощью и обратитесь за советом к паспорту безопасности.
| Символы опасности | Хн,Н |
| Описание безопасности | Беречь от влаги, кислот и окислителей. Избегайте контакта с кожей, глазами и одеждой. Не глотать. Используйте при достаточной вентиляции. Тщательно вымойте руки после работы. |
| Идентификационные номера ООН | ООН3077, ООН1376 |
| код ТН ВЭД | 2833.29.90 |
| Класс опасности | 9 (разные опасные грузы) |
| Группа упаковки | III |
| Токсичность | Вреден при проглатывании, вызывает раздражение кожи и глаз, может вызвать раздражение дыхательных путей. Может вызвать сенсибилизацию при вдыхании или контакте с кожей. |
Методы синтеза сульфата железа(ii)
Существует несколько методов синтеза сульфата железа.
Распространенный метод включает реакцию железных отложений с серной кислотой в присутствии воды и кислорода. В результате получается раствор гептагидрата сульфата железа, который можно дополнительно очистить кристаллизацией.
Другой метод предполагает реакцию оксида железа с серной кислотой при высокой температуре с последующим охлаждением и фильтрованием полученного раствора.
Восстановитель, такой как порошок железа или диоксид серы, может восстановить сульфат железа (III) до сульфата железа. При этом образуется сульфат железа и серная кислота . Чтобы получить сульфат железа, железо можно реагировать с диоксидом серы и кислородом в присутствии воды.
Другой метод включает реакцию железа с разбавленной серной кислотой в присутствии перекиси водорода . При этом образуется сульфат железа и вода.
Использование сульфата железа (ii)
Сульфат железа(II) имеет широкий спектр применения в различных отраслях промышленности, в том числе:
- Водоочистка: обычно используется при очистке воды для удаления из воды примесей, таких как сероводород.
- Удобрения: используются при производстве удобрений для обеспечения растений необходимыми питательными веществами, содержащими железо.
- Производство пигментов: используется в качестве прекурсора для производства различных железооксидных пигментов, таких как желтые и коричневые пигменты.
- Пищевые добавки: используется в качестве пищевой добавки для лечения железодефицитной анемии у людей и животных.
- Очистка сточных вод: используется при очистке сточных вод для удаления фосфатов и других загрязнений.
- Производство чернил: используется в производстве чернил в качестве черняющего агента.
- Консерванты для древесины: используются в качестве консервантов для древесины для защиты древесины от грибков и насекомых.
- Лабораторный реагент: используется в качестве лабораторного реагента в различных химических реакциях и анализах.
Вопросы:
Растворяется ли сульфат железа в воде?
Ответ: Сульфат железа, также известный как сульфат железа, умеренно растворим в воде.
Вопрос: Какова формула соединения сульфата железа (ii)?
Ответ: Формула сульфата железа — FeSO4.
Вопрос: Какова химическая формула сульфата железа (ii)?
Ответ: Химическая формула сульфата железа — FeSO4.
Вопрос: Каков процент серы в сульфате железа (ii)?
О: Процент серы в сернокислом железе составляет 18,5%.
Вопрос: Растворим ли сульфат железа(ii) в воде?
Ответ: Да, сульфат железа II, также известный как сульфат железа, растворим в воде.
Вопрос: Что такое сульфат железа?
Ответ: Сульфат железа — это другое название сульфата железа, химического соединения, обычно используемого в различных отраслях промышленности.
Вопрос: Для чего используется сульфат железа?
Ответ: Сульфат железа используется для различных целей, включая очистку воды, производство удобрений, производство пигментов, пищевых добавок, производство чернил, консервантов для древесины и красящих реагентов. лаборатория.
