1-Бромбутан представляет собой бесцветное жидкое органическое соединение с молекулярной формулой C4H9Br. Используется как алкилирующий агент в органическом синтезе и как растворитель в промышленности.
| Название ИЮПАК | Бутилбромид |
| Молекулярная формула | C4H9Br |
| Количество CAS | 109-65-9 |
| Синонимы | 1-бромбутан, н-бутилбромид, бутилбромид, бромбутан, бутан, 1-бром-, 109-65-9, 1-бромбутан, 1-бромбутан, н-C4H9Br |
| ИнЧИ | ИнЧИ=1S/C4H9Br/c1-2-3-4-5/h2-4H2.1H3 |
1-бромбутан Молярная масса
Молярная масса 1-бромбутана составляет 137,03 г/моль. Чтобы получить молярную массу 1-бромбутана, сложим атомные массы углерода, водорода и брома в одной молекуле. Химические расчеты часто требуют преобразования массы вещества в его количество молей, и для этого преобразования необходима молярная масса.
Плотность 1-бромбутана г/мл
Плотность 1-бромбутана составляет 1,27 г/мл при 25°C (77°F). Это масса единицы объема вещества. Плотность 1-бромбутана больше, чем у воды, что позволяет легко отделять его от водных растворов.
Температура кипения 1-бромбутана
Температура кипения 1-бромбутана составляет 101°C (214°F). Это температура, при которой давление паров жидкости равняется внешнему давлению. Это мера силы межмолекулярных сил в жидкости. Температура кипения 1-бромбутана делает его полезным растворителем и реагентом в органической химии.
Температура плавления C4H9Br
Температура плавления C4H9Br составляет -112°C (-170°F). Это температура, при которой твердая и жидкая фазы вещества находятся в равновесии. Температура плавления зависит от силы межмолекулярных сил, присутствующих в твердом теле. Низкая температура плавления C4H9Br делает его жидким при комнатной температуре и позволяет легко обращаться с ним.
Молекулярный вес C4H9Br
Молекулярная масса C4H9Br составляет 137,03 г/моль. Это сумма атомных весов всех атомов молекулы. Молекулярная масса используется для расчета количества вещества, необходимого для реакции, или для определения количества полученного продукта.
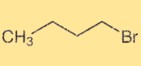
Структура 1-бромбутана
1-Бромбутан имеет неразветвленную алкильную структуру с атомом брома, присоединенным к четвертому атому углерода. Это органическое соединение с химической формулой C4H9Br. Структура 1-бромбутана определяет его физические и химические свойства, а также реакционную способность в органических реакциях.
Формула 1-Бромбутан
Формула 1-бромбутана: C4H9Br. Это показывает количество и тип атомов, присутствующих в молекуле. Формула 1-бромбутана важна для определения его реакционной способности и поведения в химических реакциях.
| Появление | Бесцветная жидкость |
| Удельный вес | 1,27 при 25°С |
| Цвет | Бесцветный |
| Запах | Характерный и сладкий запах |
| Молярная масса | 137,03 г/моль |
| Плотность | 1,27 г/мл при 25°C |
| Точка плавления | -112°С |
| Точка кипения | 101°С |
| Мигающая точка | 25°С |
| Растворимость в воде | Слегка растворим |
| Растворимость | Растворим в этаноле, эфире, хлороформе. |
| Давление газа | 10 мм рт.ст. при 25°C |
| Плотность пара | 4.6 |
| пКа | 16,5 |
| рН | Нейтральный |
1-Бромбутан Безопасность и опасности
1-Бромбутан — опасное химическое вещество, с которым следует обращаться с осторожностью. Он токсичен при проглатывании или вдыхании и может вызвать раздражение кожи и глаз при контакте. Химическое вещество также легко воспламеняется и может представлять опасность возгорания при воздействии тепла, искр или пламени. При работе с 1-бромбутаном важно носить соответствующие защитные средства, такие как перчатки, очки и лабораторный халат. Химическое вещество следует хранить в прохладном, сухом, хорошо проветриваемом помещении вдали от источников возгорания. В случае случайного воздействия немедленно промойте пораженный участок водой и обратитесь за медицинской помощью.
| Символы опасности | Т, Ф |
| Описание безопасности | Беречь от тепла, искр и пламени. Надевайте защитные перчатки/защиту глаз/лица. ПРИ ВДЫХАНИИ: Вынесите пострадавшего на свежий воздух и обеспечьте покой в удобном для дыхания положении. ПРИ ПРОГЛАТЫВАНИИ: Если вы плохо себя чувствуете, позвоните в ТОКСИКОЛОГИЧЕСКИЙ ЦЕНТР или к врачу. Прополощите рот. Хранить в хорошо проветриваемом помещении. Сохранять спокойствие. Утилизируйте содержимое/контейнер в соответствии с местными/региональными/национальными/международными правилами. |
| Идентификаторы сети | ООН1126 |
| код ТН ВЭД | 290339 |
| Класс опасности | 3 |
| Группа упаковки | II |
| Токсичность | Токсично при проглатывании или вдыхании. Может вызвать раздражение кожи и глаз. |
Методы синтеза 1-бромбутана
C4H9Br можно синтезировать реакцией 1-бутанола и бромистоводородной кислоты (HBr) в присутствии серной кислоты (H2SO4) в качестве катализатора. Это называется реакцией галогенирования, катализируемой кислотой. Реакция протекает следующим образом:
- HBr добавляют к 1-бутанолу в присутствии серной кислоты.
- HBr протонирует гидроксильную группу 1-бутанола, создавая хорошую уходящую группу (воду).
- Уходящая группа (вода) заменяется бромид-ионом (Br-) HBr, образуя C4H9Br.
- Затем реакционную смесь нагревают для отгонки C4H9Br.
Другой метод синтеза C4H9Br включает взаимодействие бутена с бромистым водородом в присутствии пероксидного инициатора, такого как пероксид бензоила или пероксид трет-бутила. Это называется реакцией свободнорадикального галогенирования. Реакция протекает следующим образом:
- Бутен добавляют к смеси бромистого водорода и пероксидного инициатора.
- Пероксидный инициатор подвергается гомолитическому расщеплению с образованием двух реакционноспособных радикалов.
- Радикалы атакуют двойную связь бутена, образуя бромидный радикал и углеродцентрированный радикал.
- Затем бромидный радикал реагирует с углеродцентрированным радикалом, образуя C4H9Br.
Оба эти метода широко используются для синтеза C4H9Br и могут быть оптимизированы для получения высоких выходов продукта. Однако важно соблюдать надлежащие меры предосторожности при работе с опасными химическими веществами, такими как HBr и пероксиды.
Использование 1-бромбутана
C4H9Br — универсальный химикат, используемый в различных промышленных и лабораторных применениях.
- Химики-органики используют C4H9Br в качестве сырья для синтеза других органических соединений, особенно для производства фармацевтических препаратов и агрохимикатов.
- Химические реакции требуют C4H9Br в качестве растворителя и действуют как реагент в органическом синтезе.
- Производители включают C4H9Br в ароматизаторы, ароматизаторы и другие ароматические соединения. Кроме того, он является компонентом поверхностно-активных веществ, широко используемых в чистящих средствах, таких как моющие средства и мыло.
- C4H9Br действует как средство повышения октанового числа в присадках к бензину и используется в производстве хладагентов и полимеров.
- Аналитические методы, такие как газовая хроматография, требуют C4H9Br в качестве стандартного лабораторного эталонного материала. Учебные и исследовательские лаборатории органической химии используют его в качестве сырья для различных экспериментов.
В целом, универсальные свойства C4H9Br делают его важным химическим веществом в химической, фармацевтической и промышленной областях, с широким спектром применений в органическом синтезе, производстве и исследованиях.
Вопросы:
Ваша задача — превратить 2-бромбутан в 1-бутен с максимальным выходом. Какие реагенты вы бы использовали?
Чтобы превратить 2-бромбутан в 1-бутен с наибольшим выходом, я бы использовал в качестве реагента сильное основание, такое как этоксид натрия (NaOEt) в этаноле. Реакция будет протекать как реакция элиминирования, известная как реакция дегидрогалогенирования.
Реакция будет следующей:
- 2-Бромбутан добавляют к раствору этилата натрия в этаноле.
- Сильное основание извлекает протон из бета-углерода, соседнего с бромом, образуя промежуточный алкоксид-ион.
- Промежуточный алкоксид-ион подвергается отщеплению уходящей группы (брома), что приводит к образованию алкена (1-бутена) и бромида натрия.
- Реакционную смесь затем перегоняют для удаления продукта 1-бутена.
При использовании сильного основания, такого как NaOEt, реакцию можно довести до образования 1-бутена, а при использовании этанола в качестве растворителя реакцию можно провести относительно безопасно и экономически эффективно. Кроме того, использование сильного основания и этанола в качестве растворителя может привести к высоким выходам 1-бутена.
Зачем начинать с 1-бромбутана в качестве альтернативы тесту с ацетоном?
Начиная с C4H9Br для NAI в тесте с ацетоном, это полезный способ определить, содержит ли данное органическое соединение атом галогена. Тест включает добавление йодида натрия (NaI) к органическому соединению, растворенному в ацетоне, с последующим добавлением небольшого количества хлора или йода.
Реакция протекает по следующему механизму:
- NaI добавляется к органическому соединению, растворенному в ацетоне, что приводит к образованию соли галогенида натрия и соответствующего органического галогенида.
- Добавление небольшого количества хлора или йода приводит к образованию небольшого количества газообразного галогена, который реагирует с галогенидом натрия с образованием соответствующего газообразного галогена.
- Затем газообразный галоген реагирует с органическим галогенидом с образованием окрашенного осадка, что указывает на присутствие галогена в исходном органическом соединении.
C4H9Br — часто используемое соединение для этого теста, поскольку это простое и легкодоступное органическое соединение, содержащее атом галогена (брома). Он также легко реагирует с йодидом натрия и газообразным галогеном с образованием окрашенного осадка, что делает его полезным тестовым соединением для обнаружения присутствия галогена в других органических соединениях.
