Бутан (C₄H₁₀) — легковоспламеняющийся углеводородный газ. Его обычно используют в качестве топлива для зажигалок и походных печей из-за его эффективных свойств горения и портативности.
| Название ИЮПАК | Бутан |
| Молекулярная формула | С₄H₁₀ |
| Количество CAS | 106-97-8 |
| Синонимы | н-Бутан, бутилгидрид, метилэтилметан, диэтил |
| ИнЧИ | ИнЧИ=1S/C4H10/c1-3-4-2/h3-4H2.1-2H3 |
Свойства бутана
Формула бутана
Формула бутана — C₄H₁₀, что указывает на то, что он состоит из четырёх атомов углерода и десяти атомов водорода. Формула предоставляет ценную информацию о химическом составе бутана, позволяя ученым изучать его свойства и поведение.
бутан Молярная масса
Молярную массу бутилгидрида можно рассчитать путем сложения атомных масс составляющих его элементов. Молярная масса бутилгидрида (C₄H₁₀) составляет примерно 58,12 грамма на моль. Молярная масса является важнейшим параметром в различных химических расчетах и играет важную роль в определении физических и химических свойств бутилгидрида.
Температура кипения бутана
Бутилгидрид имеет относительно низкую температуру кипения, около -1°C (30°F). Это означает, что при этой температуре или выше бутилгидрид легко переходит из жидкой фазы в газовую фазу. Низкая температура кипения делает бутилгидрид идеальным топливом для таких применений, как зажигалки и портативные походные печи.
Температура плавления бутана
Температура плавления бутилгидрида составляет примерно -138,4°C (-217,12°F). При этой температуре или ниже твердый бутилгидрид претерпевает фазовый переход и переходит в жидкость. Однако в нормальных атмосферных условиях бутилгидрид обычно встречается в газообразной форме.
Плотность бутана г/мл
Плотность бутилгидрида составляет примерно 2,48 грамма на миллилитр. Это указывает на то, что бутилгидрид легче воды, плотность которой составляет 1 г/мл. Плотность бутилгидрида является важнейшим свойством, определяющим его поведение при хранении или транспортировке, а также характеристики горения.
Бутан Молекулярный вес
Молекулярная масса бутилгидрида составляет примерно 58,12 грамма на моль. Он представляет собой сумму атомных весов всех атомов в одной молекуле бутилгидрида. Молекулярный вес является важным параметром для различных научных расчетов и помогает понять свойства и поведение бутилгидрида.
Структура бутана
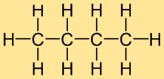
Структура бутилгидрида состоит из прямой цепи из четырех атомов углерода, к которой присоединены десять атомов водорода. Атомы углерода расположены в виде непрерывной линии, и каждый атом углерода образует одинарные связи с двумя соседними атомами углерода и тремя атомами водорода. Эта линейная структура влияет на физические и химические свойства бутилгидрида.
Растворимость бутана
Бутилгидрид считается относительно нерастворимым в воде. Он обладает низкой растворимостью из-за своей неполярной природы и слабых межмолекулярных взаимодействий с молекулами воды. Однако бутилгидрид хорошо растворим в органических растворителях, таких как этанол и ацетон. Такое поведение растворимости важно в различных приложениях, таких как процессы экстракции и реакции на основе растворителей.
| Появление | Бесцветный газ |
| Удельный вес | 2,48 |
| Цвет | Н/Д |
| Запах | Без запаха |
| Молярная масса | 58,12 г/моль |
| Плотность | 2,48 г/мл |
| Точка плавления | -138,4°C (-217,12°F) |
| Точка кипения | -1°C (30°F) |
| Мигающая точка | -60°С (-76°Ф) |
| Растворимость в воде | нерастворимый |
| Растворимость | Растворим в органических растворителях |
| Давление газа | 2,4 банкомата при 20°C |
| Плотность пара | 2,07 (воздух = 1) |
| пКа | Н/Д |
| рН | Н/Д |
Бутан: безопасность и опасности
Бутилгидрид представляет определенные риски для безопасности, которые необходимо учитывать. Это легковоспламеняющийся газ, который легко воспламеняется при наличии источника возгорания. Следует принять меры предосторожности, чтобы избежать случайного возгорания или взрыва. Важно хранить и обращаться с бутилгидридом в хорошо проветриваемых помещениях, чтобы избежать накопления легковоспламеняющихся паров. Прямое вдыхание бутилгидрида может быть вредным, поскольку он вытесняет кислород и может вызвать удушье. Кроме того, воздействие высоких концентраций бутилгидрида может вызвать головокружение, сонливость и тошноту. Очень важно соблюдать надлежащие меры предосторожности, такие как использование бутилгидрида в правильно спроектированном и одобренном оборудовании и избегать контакта с открытым огнем или искрами.
| Символы опасности | Горючий газ |
| Описание безопасности | Беречь от открытого огня и искр. Хранить в хорошо проветриваемом помещении. Избегайте вдыхания и прямого контакта. |
| Идентификаторы Организации Объединенных Наций | ООН 1011 |
| код ТН ВЭД | 2711.12.20 |
| Класс опасности | Класс 2.1 (Горючий газ) |
| Группа упаковки | Группа упаковки II |
| Токсичность | Бутилгидрид обычно считается малотоксичным. Однако вдыхание высоких концентраций может вызвать головокружение, сонливость и тошноту. Он также может вытеснять кислород в закрытых помещениях, что приводит к удушью. Для обеспечения безопасности необходимо соблюдать надлежащие процедуры вентиляции и обращения. |
Методы синтеза бутана
Различные методы синтеза бутилгидрида, в первую очередь связанные с добычей нефти или природного газа.
Фракционная перегонка: во время фракционной перегонки сырой нефти или нефтепродуктов в качестве побочного продукта образуется бутилгидрид. В процессе нефтепереработки происходит разделение различных фракций углеводородов в зависимости от их температуры кипения, и бутилгидрид является одним из компонентов, которые можно выделить.
Переработка природного газа. При переработке природного газа также производится бутилгидрид. Природный газ содержит различные углеводороды, включая метан и высшие углеводороды, такие как бутилгидрид. Смесь природного газа подвергается таким процессам, как абсорбция или криогенное разделение для отделения бутилгидрида.
Крекинг углеводородов. В процессе крекинга большие углеводородные цепи разбиваются на более мелкие, в результате чего образуется бутилгидрид. Это включает в себя обработку более тяжелых углеводородов высокими температурами или использование катализаторов для получения бутилгидрида в качестве продукта.
Изомеризация: Изомеризация перестраивает молекулярную структуру углеводородов, позволяя синтезировать бутилгидрид путем изомеризации других углеводородов, таких как пентан или гексан , в его изомеры. Конкретные катализаторы катализируют этот процесс в соответствующих условиях.
Процесс синтеза: В лаборатории ученые могут синтезировать бутилгидрид синтетическими способами. Они могут использовать различные химические реакции, такие как гидрирование или восстановление, для получения бутилгидрида из соединений-предшественников.
Эти методы позволяют производить бутилгидрид как в крупномасштабных промышленных процессах, так и в небольших лабораториях. Выбор метода зависит от наличия сырья, желаемой чистоты и конкретных требований применения.
Использование бутана
Бутилгидрид находит применение в различных отраслях промышленности и быту благодаря своим полезным свойствам. Вот некоторые распространенные применения бутилгидрида:
- Топливо: бутилгидрид используется в качестве топлива в портативных плитах, походных обогревателях и зажигалках благодаря его высокому энергетическому содержанию и эффективным свойствам горения.
- Аэрозольный вытеснитель: Бутилгидрид распыляет аэрозольные продукты, такие как лаки для волос, освежители воздуха и аэрозольные краски, позволяя им выделяться в виде мелкого тумана или аэрозоля.
- Хладагент: Бутилгидрид охлаждает и поддерживает низкие температуры в небольших холодильных системах, таких как бытовые холодильники и морозильники, выступая в качестве хладагента.
- Жидкость для зажигалок: бутилгидрид приводит в действие зажигалки и фонарики, создавая пламя, которое является ключевым компонентом жидкостей для зажигалок.
- Экстракция: Бутилгидрид действует как растворитель при экстракции эфирных масел и растительных соединений из растительных материалов, эффективно растворяя нужные соединения.
- Лабораторное использование: Лаборатории используют бутилгидрид в качестве топлива для горелок Бунзена и газовой хроматографии.
- Калибровочный газ: бутилгидрид служит калибровочным газом для детекторов газа и датчиков, обеспечивая четко определенные и легко измеряемые свойства.
- Сварка и пайка: Бутилгидридные горелки облегчают сварку и пайку благодаря своим высоким температурам, точности и удобству в использовании.
- Отдых: бутилгидрид питает портативные походные печи и фонарики, улучшая развлекательные мероприятия на свежем воздухе, такие как кемпинг, походы и приготовление пищи.
- Источник потребления: Бутилгидрид служит источником тепла в различных областях применения, включая нагревательные инструменты, небольшие нагреватели и приложения на основе пламени в определенных отраслях.
Универсальная природа бутилгидрида и диапазон его применения делают его ценным соединением в ряде отраслей промышленности, в предметах домашнего обихода и в сфере отдыха.
Вопрос:
Вопрос: Где я могу купить бутан рядом со мной?
Ответ: Обычно бутилгидрид можно найти в местных хозяйственных магазинах, супермаркетах или магазинах повседневного спроса, где продаются товары для кемпинга.
Вопрос: Является ли бутан природным газом?
О: Нет, бутилгидрид не считается природным газом. Это углеводородный газ, получаемый в результате переработки нефти или природного газа.
Вопрос: Что такое бутан?
A: Бутилгидрид представляет собой газообразный углеводород с химической формулой C₄H₁₀. Это легковоспламеняющийся газ без цвета и запаха, обычно используемый в качестве топлива и в различных применениях.
Вопрос: Как производят бутан?
Ответ: Бутилгидрид в основном производится с помощью таких процессов, как фракционная перегонка нефти или природного газа, крекинг более тяжелых углеводородов или изомеризация других углеводородов.
Вопрос: Как заправить бутановую зажигалку?
О: Чтобы заправить бутилгидридную зажигалку, сначала найдите заправочный клапан, обычно расположенный внизу. Вставьте насадку для бутилгидрида в клапан и сильно нажмите, чтобы бутилгидрид попал в просвет до тех пор, пока он не заполнится.
Вопрос: Какое из следующих соединений является структурным изомером бутана?
A: Пентан (C₅H₁₂) представляет собой структурный изомер бутилгидрида, поскольку оба соединения содержат четыре атома углерода, но имеют разное расположение.
Вопрос: Как заправить бутановую зажигалку?
A: Чтобы заправить бутилгидридную зажигалку, переверните зажигалку, совместите сопло заправочного картриджа бутилгидрида с заправочным клапаном зажигалки и сильно нажмите на картридж, чтобы выпустить гидрид из бутила в зажигалку.
Вопрос: Где я могу купить бутан рядом со мной?
О: Вы можете приобрести бутилгидрид в местных хозяйственных магазинах, супермаркетах или магазинах повседневного спроса, где продаются товары для кемпинга или предметы домашнего обихода.
Вопрос: Где купить бутан?
Ответ: Бутилгидрид можно приобрести в различных источниках, включая интернет-магазины, хозяйственные магазины, магазины товаров для кемпинга и некоторые супермаркеты.
Вопрос: Какое утверждение лучше всего сравнивает температуру плавления бутана (C₄H₁₀) с температурой плавления октана (C₈H₁₈)?
Ответ: Октан с более крупной и сложной молекулярной структурой обычно имеет более высокую температуру плавления, чем бутилгидрид.
Вопрос: Какова молярная масса бутана, C₄H₁₀?
A: Молярная масса бутилгидрида (C₄H₁₀) составляет примерно 58,12 грамма на моль.
Вопрос: Сколько изомеров возможно у C₄H₁₀?
A: Бутилгидрид (C₄H₁₀) имеет два изомера: н-бутан (нормальный бутан) и изобутан (2-метилпропан).
Вопрос: Какие из соединений C₄H₁₀, SrCl₂, Cr(NO₃)₃, OF₂ должны существовать в виде молекул?
A: Ожидается, что C₄H₁₀ (бутилгидрид) и OF₂ (дифторид кислорода) существуют в виде молекул, тогда как SrCl₂ и Cr(NO₃)₃ являются ионными соединениями.
