ЭДТА – это поликарбоновая аминокислота, которая может хелатировать ионы металлов. Он имеет формулу [CH2N(CH2CO2H)2]2. Он способствует выведению тяжелых металлов из организма. ЭДТА также сохраняет образцы крови и пищевые продукты.
| Имя Юпак | 2,2′,2″,2″‘-(этан-1,2-диилдиаммоний)тетраацетат динатрия |
| Молекулярная формула | C10H14N2Na2O8 |
| Количество CAS | 139-33-3 |
| Синонимы | Динатриевая соль (этилендинитрило)тетрауксусной кислоты, динатрий эдетат, динатриевая ЭДТА, динатриевая соль ЭДТА, динатриевая соль ЭДТА, динатриевая соль ЭДТА, динатриевая соль этиленбиса (иминодиуксусной кислоты), N,N’-1,2-этандиилбис [N-(карбоксиметил) )глицин], динатриевая соль, Na2-ЭДТА, Na2H2EDTA |
| Инчи | InChI=1S/C10H16N2O8.2Na/c13-7(14)3-11(4-8(15)16)1-2-12(5-9(17)18)6-10(19)20;;/ h1-6H2,(H,13,14)(H,15,16)(H,17,18)(H,19,20);;/q;2*+1/p-2 |
Свойства ЭДТА
формула ЭДТА
ЭДТА означает этилендиаминтетрауксусную кислоту, которая представляет собой синтетическое органическое соединение, способное хелатировать ионы металлов. Формула ЭДТА — C10H16N2O8, что означает, что в ее молекуле содержится 10 атомов углерода, 16 атомов водорода, 2 атома азота и 8 атомов кислорода.
ЭДТА Молярная масса
Молярная масса динатрия эдетата представляет собой сумму атомных масс всех атомов в его формуле. Атомные массы углерода, водорода, азота и кислорода составляют 12,01 г/моль, 1,01 г/моль, 14,01 г/моль и 16,00 г/моль соответственно. . Следовательно, молярная масса динатрия эдетата равна (10 х 12,01) + (16 х 1,01) + (2 х 14,01) + (8 х 16,00) = 292,24 г/моль.
Точка кипения ЭДТА
Точка кипения вещества – это температура, при которой оно переходит из жидкого состояния в газообразное. Точку кипения динатрия эдетата измерить непросто, поскольку он разлагается, не достигнув точки кипения. Однако некоторые источники оценивают температуру кипения динатрия эдетата примерно в 614,2 ° C при давлении 760 мм рт. ст.
ЭДТА Точка плавления
Температура плавления вещества – это температура, при которой оно переходит из твердого состояния в жидкое. Температура плавления динатрия эдетата зависит от степени гидратации и кристаллизации. Безводная форма динатрия эдетата имеет температуру плавления примерно 240°С, тогда как дигидратная форма имеет температуру плавления примерно 248°С.
ЭДТА Плотность г/мл
Плотность вещества – это масса единицы объема. Плотность динатрия эдетата также варьируется в зависимости от степени гидратации и кристаллизации. Безводная форма динатрия эдетата имеет плотность примерно 0,86 г/мл, тогда как дигидратная форма имеет плотность примерно 1,6 г/мл.
ЭДТА Молекулярный вес
Молекулярная масса вещества — это еще один термин, обозначающий его молярную массу, которая равна массе одного моля вещества. Как упоминалось выше, молярная масса динатрия эдетата составляет 292,24 г/моль, поэтому его молекулярная масса также равна 292,24 г/моль.
Структура ЭДТА
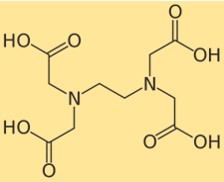
Структура динатрия эдетата показывает, как его атомы расположены и связаны в молекуле. Динатриевый эдетат имеет центральную этилендиаминовую группу, к которой присоединены четыре группы карбоновой кислоты. Каждая группа карбоновой кислоты может потерять протон и образовать отрицательный заряд, который может связываться с ионом металла. Строение динатрия эдетата можно представить следующей схемой:
Растворимость ЭДТА
Растворимость вещества – это количество, которое может раствориться в данном растворителе при данной температуре и давлении. Растворимость динатрия эдетата зависит от pH и присутствия ионов металлов в растворе. Динатрий эдетат более растворим в щелочных растворах, чем в кислых, поскольку он образует больше отрицательных зарядов, которые могут взаимодействовать с молекулами воды. Динатрий эдетат также может образовывать комплексы с ионами металлов, что может увеличивать или уменьшать его растворимость в зависимости от стабильности и заряда комплекса. Например, при pH 7 и 25 °C растворимость динатрия эдетата в воде составляет примерно 0,5 М (186 мг/мл), а растворимость его кальциевого комплекса — примерно 0,02 М (7 мг/мл).
| Появление | Белое кристаллическое твердое вещество |
| Удельная плотность | Нет в наличии |
| Цвет | Белый |
| Запах | Без запаха |
| Молярная масса | 292,24 г/моль |
| Плотность | 1,6 г/мл (дигидрат), 0,86 г/мл (безводный) |
| Точка плавления | 248°С (дигидрат), 240°С (безводный) |
| Точка кипения | 614,2°С (разлагается) |
| Мигающая точка | 325,2°С |
| Растворимость в воде | 0,5 М (186 мг/мл) при pH 7 и 25 °C |
| Растворимость | Растворим в щелочных растворах, нерастворим в органических растворителях. |
| Давление газа | 3,77 x 10^-12 мм рт.ст. при 25°C |
| Плотность пара | Нет в наличии |
| пКа | 2.0, 2.7, 6.2, 10.3 |
| рН | от 4 до 6 (0,26 М раствор) |
Риски безопасности ЭДТА
Динатрий эдетат представляет собой синтетическое органическое соединение, способное хелатировать ионы металлов. Его применение разнообразно в областях медицины, промышленности, сельского хозяйства и исследований. Однако при неправильном обращении он также представляет определенный риск для здоровья человека и окружающей среды.
Динатрий эдетат может вызвать раздражение кожи и глаз при попадании на них. При проглатывании он также может вызвать тошноту, рвоту, диарею и боль в животе. При вдыхании может нанести вред дыхательной системе. При попадании в организм он может повлиять на клетки крови и почки. В больших дозах это может быть смертельным.
Динатрий эдетат также может загрязнять почву и воду при попадании в окружающую среду. Он может связываться с основными металлами и влиять на их доступность для растений и животных. Он может мешать биологическим процессам, которые зависят от ионов металлов.
Динатрий эдетат следует используйте с осторожностью и с использованием соответствующих защитных средств. Храните его в прохладном, сухом, хорошо проветриваемом месте. Утилизируйте его в соответствии с местными правилами.
| Символы опасности | |
| Описание безопасности | S24/25: Избегайте контакта с кожей и глазами. |
| Идентификационные номера ООН | UN3077 (твердый), UN3082 (жидкий) |
| код ТН ВЭД | 29224985 |
| Класс опасности | 9 (различные опасные материалы) |
| Группа упаковки | III (низкая опасность) |
| Токсичность | Перорально LD50, крыса: 2000 мг/кг. |
Методы синтеза ЭДТА
Существует несколько методов синтеза динатрия эдетата, но наиболее распространенным является конденсация этилендиамина с хлоруксусной кислотой или ее натриевой солью.
Реакция включает две стадии: во-первых, нуклеофильная атака этилендиамина на хлоруксусную кислоту или ее натриевую соль с образованием промежуточного моноамида. Во-вторых, при удалении соляной кислоты или хлорида натрия образуется группа карбоновой кислоты. Для образования динатрия эдетата его можно ввести в реакцию с другим эквивалентом хлоруксусной кислоты или ее натриевой солью.
Другим методом синтеза динатрия эдетата является окисление этилендиамина гипохлоритом натрия в щелочном растворе. Этот метод дает динатрий эдетат в виде натриевой соли и аммиак в качестве побочного продукта.
Другие методы синтеза эдетата динатрия включают реакцию этилендиамина с формальдегидом и цианидом натрия или реакцию этилендиамина с глиоксиловой кислотой или ее эфирами.
Использование ЭДТА
Динатрий эдетат представляет собой синтетическое органическое соединение, способное хелатировать ионы металлов. Он имеет различное применение в разных областях и отраслях. Некоторые виды использования Эдетата динатрия:
- В медицине динатрий эдетат может лечить отравление тяжелыми металлами, связывая токсичные металлы и выводя их из организма. Он также может предотвратить образование тромбов и кальцификацию артерий путем хелатирования ионов кальция.
- В пищевых продуктах и напитках динатрий эдетат может сохранять цвет, вкус и текстуру продуктов, предотвращая окисление и прогоркание. Это также может предотвратить изменение цвета и ухудшение качества, вызванное ионами металлов.
- В косметике и средствах личной гигиены динатрий эдетат может улучшить стабильность и эффективность продуктов, предотвращая рост микробов и реакции, катализируемые металлами. Он также может улучшить внешний вид продуктов за счет хелатирования минералов, ответственных за жесткость воды.
- В промышленности и исследованиях динатрий эдетат может улучшить производительность и качество продуктов и процессов за счет хелатирования мешающих ионов металлов. Например, он может предотвратить образование накипи в котлах и трубах, улучшить крашение и печать тканей, удалить ржавчину и пятна с металлов, а также контролировать pH и концентрацию металлов с помощью аналитических методов.
Вопросы:
Вопрос: Что такое ЭДТА?
Ответ: Динатрий эдетат представляет собой синтетическое органическое соединение, которое может хелатировать ионы металлов. Это этилендиаминтетрауксусная кислота.
Вопрос: Как приготовить раствор ЭДТА?
Ответ: Чтобы приготовить раствор динатрия эдетата, взвесьте необходимое количество динатрия эдетата и растворите его в дистиллированной воде. Отрегулируйте pH до 8,0 с помощью гидроксида натрия.
Вопрос: Как растворить ЭДТА в воде?
A: Динатрий эдетат растворим в воде, но растворяется медленно. Чтобы растворить динатрий эдетат в воде, нагрейте воду примерно до 80°C и перемешивайте смесь до полного растворения динатрия эдетата.
Вопрос: Как приготовить 0,5 М ЭДТА?
Ответ: Чтобы приготовить 0,5 М динатрий эдетат, взвесьте 73,06 г динатрия эдетата и растворите его в 800 мл дистиллированной воды. Доведите pH до 8,0 с помощью гидроксида натрия и разбавьте раствор до 1 л дистиллированной водой.
Вопрос: Что делает ЭДТА?
Ответ: Динатрий эдетат связывается с ионами металлов и образует с ними устойчивые комплексы. Это предотвращает реакцию ионов металлов с другими веществами или вмешательство в аналитические методы.
Вопрос: Что означает ЭДТА?
A: Эдетат динатрия означает этилендиаминтетрауксусную кислоту, что является названием соединения с формулой [CH2N(CH2CO2H)2]2.
Вопрос: Как рассчитать жесткость воды методом титрования ЭДТА?
Ответ: Чтобы рассчитать жесткость воды путем титрования динатрием эдетата, оттитуйте известный объем пробы воды стандартным раствором динатрия эдетата, используя соответствующий индикатор. Запишите объем использованного динатрия эдетата и используйте следующую формулу: Жесткость (мг/л в пересчете на CaCO3) = (объем ЭДТА x молярность ЭДТА x 1000) / объем пробы воды.
