2-Бутанол — бесцветная легковоспламеняющаяся жидкость со сладким запахом. Он обычно используется в качестве растворителя и при производстве химических веществ, таких как метилэтилкетон и бутилацетат.
| Название ИЮПАК | 2-бутанол |
| Молекулярная формула | C4H10O |
| Количество CAS | 78-92-2 |
| Синонимы | Сухой бутиловый спирт, 2-бутиловый спирт, бутан-2-ол, этилметилкарбинол |
| ИнЧИ | ИнХI=1S/C4H10O/c1-3-4(2)5/h4-5H,3H2,1-2H3 |
Свойства 2-бутанола
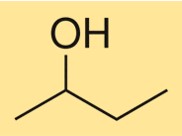
формула 2-бутанола
Химическая формула 2-бутанола — C4H10O, что указывает на то, что он содержит четыре атома углерода, десять атомов водорода и один атом кислорода. Это изомер бутанола и имеет структурную формулу CH3CH(OH)CH2CH3. Цифра «2» в названии соединения обозначает положение гидроксильной группы в углеродной цепи.
2-бутанол Молярная масса
Молярная масса C4H10O составляет 74,12 г/моль. Это значение можно получить, сложив атомные массы всех атомов соединения, которые составляют 12,01 г/моль для углерода, 1,01 г/моль для водорода и 16,00 г/моль для кислорода. Молярная масса — важное свойство C4H10O, поскольку она используется для расчета количества соединения, необходимого в химических реакциях.
Температура кипения 2-бутанола
Температура кипения C4H10O составляет 99,5 ° C (211,1 ° F) при стандартном давлении (1 атм). Это температура, при которой жидкое состояние соединения переходит в газообразное состояние. Температура кипения C4H10O выше, чем у бутана (-0,5 ° C) и бутена (-6,3 ° C) из-за его водородных связей и молекулярной массы.
Точка плавления 2-бутанола
Температура плавления C4H10O составляет -114,7 ° C (-174,5 ° F). Это температура, при которой твердое состояние соединения переходит в жидкое состояние. Температура плавления C4H10O ниже, чем у бутана (-138,4 °С) и бутена (-185,3 °С) из-за его разветвленной структуры и водородных связей.
2-бутанол Плотность г/мл
Плотность C4H10O составляет 0,809 г/мл при 25°C (77°F). Эта величина указывает на массу соединения в единице объема вещества. Плотность C4H10O выше, чем у бутана (0,588 г/мл) и бутена (0,587 г/мл) из-за его молекулярной массы и межмолекулярных сил.
2-бутанол Молекулярный вес
Молекулярная масса C4H10O составляет 74,12 г/моль. Это сумма атомных весов всех атомов в молекуле соединения. Молекулярная масса используется для расчета других свойств соединения, таких как молярная масса, температура кипения и плотность.
Структура 2-бутанола
Структура C4H10O характеризуется разветвленной углеродной цепью с гидроксильной группой, присоединенной ко второму атому углерода. Это первичный спирт с хиральным центром, то есть он существует в виде двух стереоизомеров: (R)-C4H10O и (S)-C4H10O. Соединение имеет трехмерную структуру за счет тетраэдрического расположения атомов углерода и кислорода вокруг гидроксильной группы.
Растворимость 2-бутанола
C4H10O является полярным соединением и частично растворим в воде. Растворимость C4H10O в воде составляет 80 г/л при 25°C (77°F). Соединение более растворимо в органических растворителях, таких как этанол, эфир и ацетон. На растворимость C4H10O влияют такие факторы, как температура, давление и природа растворителя.
| Появление | Чистая жидкость |
| Удельный вес | 0,810 г/мл при 25°C (77°F) |
| Цвет | Бесцветный |
| Запах | Характеристика |
| Молярная масса | 74,12 г/моль |
| Плотность | 0,809 г/мл при 25°C (77°F) |
| Точка плавления | −114,7°C (−174,5°F) |
| Точка кипения | 99,5°C (211,1°F) при давлении 1 атм. |
| Мигающая точка | 39°C (102°F) в закрытом тигле |
| Растворимость в воде | 80 г/л при 25°C (77°F) |
| Растворимость | Растворим в этаноле, эфире и ацетоне. |
| Давление газа | 8,7 мм рт.ст. при 25°C (77°F) |
| Плотность пара | 2,6 (воздух = 1) |
| пКа | 16 |
| рН | 7,0-8,5 |
Безопасность и опасность 2-бутанола
C4H10O считается относительно безопасным химическим веществом при правильном обращении. Однако воздействие высоких концентраций может вызвать раздражение глаз, кожи и дыхательных путей. Это также может вызвать головные боли, головокружение и тошноту. Проглатывание C4H10O может вызвать раздражение желудочно-кишечного тракта и возможную депрессию центральной нервной системы. Кроме того, C4H10O легковоспламеняем и может представлять опасность пожара. Хранить следует в прохладном, сухом, хорошо проветриваемом месте вдали от источников возгорания. При работе с этим химическим веществом следует использовать соответствующие средства индивидуальной защиты, такие как перчатки и очки. Разливы следует немедленно устранять с использованием соответствующих процедур.
| Символы опасности | Ф, Си |
| Описание безопасности | Храните вдали от источников тепла/искры/открытого огня/горячих поверхностей. Надевайте защитные перчатки/защитную одежду/защиту глаз/лица. ПРИ ПОПАДАНИИ НА КОЖУ (или волосы): Немедленно снимите всю загрязненную одежду. Промойте кожу водой/душем. ПРИ ВДЫХАНИИ: Вынесите пострадавшего на свежий воздух и обеспечьте покой в удобном для дыхания положении. ПРИ ПРОГЛАТЫВАНИИ: Прополоскать рот. Не вызывает рвоту. Если вы плохо себя чувствуете, позвоните в ТОКСИКОЛОГИЧЕСКИЙ ЦЕНТР или к врачу. |
| Идентификационные номера ООН | ООН1120 |
| код ТН ВЭД | 2905.13.00 |
| Класс опасности | 3 – Легковоспламеняющиеся жидкости |
| Группа упаковки | III |
| Токсичность | LD50 (перорально, крыса): 4,6 г/кг; LC50 (ингаляция, крыса): 2100 частей на миллион/4 часа. |
Методы синтеза 2-бутанола
Для синтеза C4H10O можно использовать несколько методов.
Один метод включает восстановление ацетона боргидридом натрия в присутствии никелевого или палладиевого катализатора. В результате реакции образуется смесь C4H10O и его изомера изобутанола, которую можно разделить фракционной перегонкой.
Другой метод включает гидратацию 1-бутена с использованием серной кислоты в качестве катализатора. В результате реакции образуется смесь C4H10O и его изомеров, но желаемый C4H10O можно отделить фракционной перегонкой.
Химический процесс Реппе включает использование палладиевого или никелевого катализатора для реакции ацетилена с формальдегидом и водой, что приводит к образованию винилового спирта. Эта реакция далее приводит к синтезу C4H10O. Виниловый спирт затем подвергается гидрированию с образованием C4H10O.
Другой метод синтеза C4H10O предполагает гидрирование кротональдегида в присутствии никелевого катализатора. В результате реакции образуется смесь C4H10O и его изомера, но желаемый C4H10O можно выделить фракционной перегонкой.
Использование 2-бутанола
C4H10O имеет множество применений в различных отраслях промышленности. Некоторые из его применений:
- Растворитель: используется в качестве растворителя при производстве смол, лаков и покрытий. Также используется в качестве растворителя простых и сложных эфиров целлюлозы.
- Топливо: используется в качестве добавки к биотопливу из-за его низкой токсичности и высокого содержания энергии. Было показано, что он имеет более высокую эффективность сгорания, чем этанол, и изучается как потенциальная альтернатива бензину.
- Химическое промежуточное соединение: используется в качестве сырья для производства других химикатов, таких как метилэтилкетон, метилизобутилкетон и диизобутилен.
- Духи и ароматизаторы: Используется в качестве ароматизатора и ароматизатора при производстве духов, мыла и других средств личной гигиены.
- Лабораторный реагент: используется в качестве растворителя и реагента в экспериментах по органической химии.
- Чистящее средство: используется в качестве чистящего средства в промышленных и бытовых чистящих средствах.
- Печатная краска: также используется в качестве растворителя при производстве печатных красок.
Вопросы:
Вопрос: Какое карбонильное соединение и реактив Гриньяра можно использовать для получения 2-бутанола?
Ответ: Карбонильное соединение, которое можно использовать для получения C4H10O, — это бутаналь (также известный как н-бутиральдегид), а реактив Гриньяра, который можно использовать, — это этилмагнийбромид. В результате реакции бутаналя с этилмагнийбромидом в качестве конечного продукта образуется C4H10O.
Вопрос: Полярен ли 2-бутанол?
Ответ: Да, C4H10O полярен. Он содержит гидроксильную группу (-ОН), которая является полярной функциональной группой, которая делает молекулу полярной.
Вопрос: Растворим ли 2-бутанол в воде?
О: Да, C4H10O частично растворим в воде. Полярная гидроксильная группа C4H10O позволяет ему образовывать водородные связи с молекулами воды, что делает его в некоторой степени растворимым в воде.
Вопрос: Имеет ли 2-бутанол водородную связь?
Ответ: Да, C4H10O может образовывать водородные связи. Гидроксильная группа (-OH) в C4H10O может образовывать водородные связи с другими полярными молекулами, содержащими сайты водородных связей, например с водой.
