Фторметан (CH3F) — бесцветный газ со слабым эфирным запахом. Его используют в производстве электроники, фармацевтических препаратов и в качестве хладагента. Он не очень токсичен, но представляет собой мощный парниковый газ.
| Название ИЮПАК | Фторметан |
| Молекулярная формула | CH3F |
| Количество CAS | 593-53-3 |
| Синонимы | Метилфторид, Фреон 41, Галоидуглерод 41, R 41, ООН 2452 |
| ИнЧИ | ИнЧИ=1С/Ч3Ф/с1-2/х1Х3 |
Свойства фторметана
CH3F Точка кипения
Температура кипения CH3F составляет -78,4°C, что является относительно низким показателем. Это делает его идеальным хладагентом для различных применений, таких как системы охлаждения и кондиционирования воздуха. CH3F также используется в качестве пропеллента в аэрозолях из-за его низкой температуры кипения.
CH3F Молярная масса
CH3F — химическое соединение с молекулярной формулой CH3F. Он также известен как метилфторид и имеет молярную массу 34,03 г/моль. CH3F — бесцветный газ со слабым эфирным запахом, который благодаря своим уникальным свойствам широко используется в различных областях.
CH3F Температура плавления
CH3F имеет температуру плавления -141°C, что также является относительно низким. Его низкая температура плавления облегчает обращение и транспортировку, что делает его популярным выбором для различных промышленных применений. Низкая температура плавления CH3F также делает его пригодным для использования в качестве хладагента в низкотемпературных системах.
Плотность CH3F
Плотность CH3F составляет 0,89 г/мл, что является относительно низким показателем. Это делает его менее плотным, чем воздух, плотность которого составляет 1,29 г/мл. В результате CH3F часто используется в качестве газа легче воздуха в различных приложениях, включая обнаружение утечек, газовую хроматографию, а также в качестве подъемного газа для воздушных шаров и дирижаблей.
CH3F Молекулярный вес
Молекулярная масса CH3F составляет 34,03 г/моль, что относительно мало. Это делает его легким соединением, с которым легко обращаться и транспортировать. CH3F часто используется в производстве электроники и фармацевтики из-за его низкой молекулярной массы и уникальных свойств.
Структура CH3F
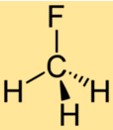
Структура CH3F состоит из одного атома углерода, связанного с тремя атомами водорода и одним атомом фтора. Атом фтора присоединяется к атому углерода, замещая один из атомов водорода в метане. Структура CH3F делает его стабильным соединением с уникальными химическими свойствами.
Формула фторметана
Формула фторметана — CH3F, что отражает расположение атомов в молекуле. Формула показывает, что фторметан состоит из одного атома углерода, трех атомов водорода и одного атома фтора. Формула используется для описания химического состава фторметана и важна в различных приложениях.
| Появление | Бесцветный газ |
| Удельный вес | 0,89 при 20°C (воздух = 1) |
| Цвет | Бесцветный |
| Запах | Легкий эфирный запах |
| Молярная масса | 34,03 г/моль |
| Плотность | 0,89 г/мл |
| Точка плавления | -141°С |
| Точка кипения | -78,4°С |
| Мигающая точка | Не воспламеняется |
| Растворимость в воде | 0,5 г/л при 20°C |
| Растворимость | Смешивается с органическими растворителями. |
| Давление газа | 4,4 бар при 20°C |
| Плотность пара | 1,43 (воздух = 1) |
| пКа | 50,9 |
| рН | Непригодный |
Безопасность и опасность фторметана
Фторметан обычно считается безопасным в обращении и использовании соединением, малотоксичным и негорючим. Однако, как и любое химическое вещество, оно имеет потенциальную опасность и соображения безопасности. Воздействие высоких концентраций фторметана может вызвать головокружение, головные боли и тошноту. Это также мощный парниковый газ, который способствует изменению климата. Работать с фторметаном следует в хорошо проветриваемом помещении и надевать защитное оборудование, такое как перчатки и очки. Важно соблюдать надлежащие процедуры хранения и обращения, чтобы избежать утечек и случайных выбросов в окружающую среду.
| Символы опасности | Ж+ |
| Описание безопасности | Легковоспламеняющийся газ; Токсично при вдыхании; Вызывает раздражение кожи; Вызывает серьезное раздражение глаз; Может вызвать сонливость или головокружение; Может вызвать повреждение органов |
| Идентификаторы сети | ООН2452 |
| код ТН ВЭД | 2903.49.90 |
| Класс опасности | 2.1 |
| Группа упаковки | II |
| Токсичность | Низкая токсичность, но может нанести вред здоровью при вдыхании в высоких концентрациях. |
Методы синтеза фторметана
Несколько методов, включая прямое фторирование метана и реакции галогенного обмена, позволяют синтезировать фторметан.
Распространенным методом является реакция метанола с фтористым водородом в присутствии катализатора, такого как оксид алюминия или фторид алюминия.
Другой метод включает реакцию хлорметана или бромметана с газообразным фтористым водородом. Оба этих метода производят фторметан в качестве побочного продукта, который затем можно отделить и очистить перегонкой или другими методами.
Другой метод синтеза фторметана включает реакцию фтороформа и хлористого водорода в присутствии катализатора, например цинка или меди. В результате этой реакции образуется смесь хлорфторметана и фторметана, которую можно разделить и очистить перегонкой.
Использование фторметана
Фторметан имеет несколько применений в различных отраслях промышленности, в том числе:
- Охлаждение: используется в качестве хладагента в промышленных и коммерческих холодильных системах из-за его низкой температуры кипения и негорючести.
- Электроника: используется в качестве чистящего средства для электронных компонентов и в качестве средства плазменного травления в полупроводниковой промышленности.
- Медицинское применение: Используется в качестве анестетика в ветеринарии из-за низкой токсичности и быстрого действия.
- Производство пестицидов: используется в качестве прекурсора при производстве некоторых пестицидов, включая гербициды и инсектициды.
- Производство полимеров: используется в качестве вспенивателя при производстве пенопластов, например пенополиуретана.
- Лабораторное применение: используется в качестве растворителя и реагента в различных лабораторных применениях, включая химический синтез и анализ.
- Пожаротушение: также используется в качестве средства пожаротушения в некоторых типах огнетушителей, особенно в компьютерных и телекоммуникационных помещениях.
Вопросы:
Вопрос: CH3F полярный или неполярный?
Ответ: CH3F является полярной молекулой из-за асимметричного расположения атомов фтора и водорода вокруг центрального атома углерода, что приводит к суммарному дипольному моменту.
Вопрос: Есть ли у CH3F водородная связь?
Ответ: Фторметан не имеет водородной связи, поскольку он не содержит атома водорода, связанного с сильно электроотрицательным элементом, таким как азот, кислород или фтор.
Вопрос: Какое соединение обладает самыми сильными межмолекулярными силами: HF, CH3Cl, CH3F, HCl?
Ответ: HF обладает сильнейшими межмолекулярными силами из-за его способности образовывать водородные связи, которые сильнее диполь-дипольных сил других соединений.
Вопрос: Что обладает самыми слабыми диполь-дипольными силами: N2, CO, CH3F, HCl?
Ответ: N2 имеет самые низкие диполь-дипольные силы, поскольку это неполярная молекула и, следовательно, не имеет суммарного дипольного момента. CO, CH3F и HCl являются полярными молекулами и обладают диполь-дипольными силами, но сила этих сил возрастает в порядке HCl < CH3F < CO из-за увеличения полярности молекул.
