Дихлорметан (CH2Cl2) или метиленхлорид растворяет широкий спектр органических соединений и обычно используется в качестве растворителя в химических лабораториях. Его также можно использовать в процессах снятия краски и обезжиривания.
| Название ИЮПАК | дихлорметан |
| Молекулярная формула | CH2Cl2 |
| Количество CAS | 75-09-2 |
| Синонимы | Метиленхлорид, метилендихлорид, ДХМ, Наркотил, Солаэстин, Солметин и т. д. |
| ИнЧИ | InChI=1S/CH2Cl2/c2-1-3/h1H2 |
Дихлорметан Плотность г/мл
Плотность дихлорметана составляет 1,326 г/мл. Это значение указывает массу дихлорметана на единицу объема при данной температуре и давлении. Плотность дихлорметана относительно высока, что делает его более плотной жидкостью, чем вода. Это свойство делает его полезным в некоторых лабораторных приложениях, где его можно использовать для разделения веществ различной плотности.
Температура кипения дихлорметана
Температура кипения дихлорметана составляет 39,6°C (103,3°F). Эта температура указывает точку, в которой жидкая форма дихлорметана перейдет в газообразное состояние. Низкая температура кипения дихлорметана делает его очень летучим соединением, которое легко испаряется при комнатной температуре. Это свойство делает его полезным в качестве растворителя во многих лабораторных применениях, где его можно легко испарить.
дихлорметан Молярная масса
Молярная масса дихлорметана, также называемого метиленхлоридом, составляет 84,93 г/моль. Это значение получается сложением атомных масс атомов одной молекулы дихлорметана. Молекулярная формула дихлорметана — CH2Cl2, что указывает на то, что он содержит один атом углерода, два атома водорода и два атома хлора. Молярная масса является важным свойством для определения количества вещества, присутствующего в данном образце.
Точка плавления дихлорметана
Температура плавления CH2Cl2 составляет -97,4°C (-143,3°F). Эта температура указывает точку, в которой твердая форма CH2Cl2 перейдет в жидкое состояние. Однако CH2Cl2 редко встречается в твердой форме, так как при комнатной температуре он является летучей жидкостью. Низкая температура плавления CH2Cl2 затрудняет его замерзание, и он остается жидким даже при низких температурах.
Дихлорметан Молекулярный вес
Молекулярная масса CH2Cl2 составляет 84,93 г/моль. Эта величина представляет собой сумму атомных весов атомов одной молекулы CH2Cl2. Молекулярная масса является важным свойством для определения количества вещества, присутствующего в данном образце.
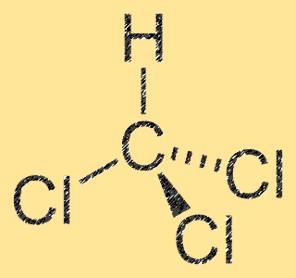
Структура дихлорметана
CH2Cl2 имеет тетраэдрическую молекулярную структуру, в которой центральный атом углерода связан с двумя атомами хлора и двумя атомами водорода. Молекула обладает дипольным моментом, который возникает из-за разницы в электроотрицательности атомов углерода и хлора. Атом углерода имеет частично положительный заряд, а атомы хлора — частичный отрицательный заряд. Это свойство делает CH2Cl2 полярной молекулой.
Формула дихлорметана
Молекулярная формула дихлорметана – CH2Cl2. Формула указывает, что молекула содержит один атом углерода, два атома водорода и два атома хлора. Формула также предоставляет информацию об относительном количестве атомов в одной молекуле дихлорметана. Формула полезна для определения стехиометрии химических реакций с участием дихлорметана.
| Появление | Бесцветная жидкость |
| Удельный вес | 1326 |
| Цвет | Бесцветный |
| Запах | Легкий запах, похожий на хлороформ. |
| Молярная масса | 84,93 г/моль |
| Плотность | 1326 г/мл |
| Точка плавления | -97,4°C (-143,3°F) |
| Точка кипения | 39,6°С (103,3°Ф) |
| Мигающая точка | -22°C (-8°F) |
| Растворимость в воде | 16,5 г/л при 20°C (68°F) |
| Растворимость | Смешивается со многими органическими растворителями. |
| Давление газа | 44,6 кПа при 20°C (68°F) |
| Плотность пара | 2,93 |
| пКа | 4 |
| рН | Нейтральный |
Безопасность и опасность дихлорметана
Дихлорметан (CH2Cl2), также известный как метиленхлорид, представляет собой опасное химическое вещество, которое представляет значительную угрозу безопасности при неправильном обращении. Он легко воспламеняется и может вызвать пожар или взрыв при воздействии тепла или открытого огня. Вдыхание его паров может вызвать раздражение дыхательных путей, головную боль, головокружение и даже потерю сознания. Контакт CH2Cl2 с кожей может вызвать раздражение, ожоги или химические ожоги. Это также потенциальный канцероген, длительное воздействие которого увеличивает риск рака печени и легких. При работе с CH2Cl2 необходимы надлежащие меры безопасности, такие как использование соответствующих средств индивидуальной защиты и работа в хорошо проветриваемом помещении.
| Символы опасности | Хн,Ф |
| Описание безопасности | Легковоспламеняющаяся жидкость и пар. Вреден при проглатывании, вдыхании или попадании через кожу. Вызывает раздражение кожи и серьезное раздражение глаз. Может вызвать раздражение дыхательных путей. Может вызвать сонливость или головокружение. Может быть смертельно при проглатывании и попадании в дыхательные пути. |
| Идентификаторы сети | ООН 1593 |
| код ТН ВЭД | 29031200 |
| Класс опасности | 3 |
| Группа упаковки | II |
| Токсичность | Дихлорметан классифицируется как канцероген категории 2 и связан с раком печени и легких. Также известно, что он вызывает депрессию центральной нервной системы и может быть смертельным при проглатывании или вдыхании в высоких концентрациях. При работе с дихлорметаном всегда следует соблюдать надлежащие меры безопасности. |
Методы синтеза дихлорметана
Существует несколько методов синтеза дихлорметана (CH2Cl2), бесцветной жидкости, используемой в качестве растворителя и средства для снятия краски. Распространенный метод включает реакцию газообразного метана с газообразным хлором в присутствии катализатора, обычно хлорида алюминия или хлорида железа. В результате реакции в качестве побочных продуктов образуются как CH2Cl2, так и газообразный хлористый водород. Другой метод включает хлорирование метанола газообразным хлористым водородом или тионилхлоридом. В результате этой реакции также образуется CH2Cl2 в качестве продукта, а также вода или диоксид серы в качестве побочных продуктов.
Другой метод предполагает реакцию хлороформа с цинком в присутствии соляной кислоты. В результате этой реакции в качестве продуктов образуются CH2Cl2 и хлорид цинка, а в качестве побочного продукта — газообразный водород.
Хлорирование различных органических соединений, таких как этан или пропан, в присутствии катализатора может привести к образованию CH2Cl2 в качестве побочного продукта.
Независимо от используемого метода, важно обращаться с CH2Cl2 осторожно из-за его опасных свойств. При синтезе и обращении с CH2Cl2 важно принимать соответствующие меры безопасности, например, носить соответствующие средства индивидуальной защиты и работать в хорошо проветриваемом помещении.
Использование дихлорметана
Дихлорметан, также известный как метиленхлорид, находит множество применений в промышленности и исследованиях в качестве универсального органического растворителя. Он играет решающую роль в производстве фармацевтических препаратов и покрытий, таких как краски и лаки. Кроме того, это полезное чистящее средство для обезжиривания в электронной и металлургической промышленности.
Дихлорметан растворяет и удаляет многие типы красок и покрытий, что делает его популярным средством для снятия краски. Также заслуживает внимания его использование в качестве вспенивателя при производстве пенополиуретанов, поликарбонатных смол и других пластмасс.
Помимо промышленного использования, дихлорметан ценен при экстракции натуральных продуктов, таких как эфирные масла и парфюмерия, из растительного сырья. Он также является эффективным растворителем многих органических соединений, используемых в лабораторных реагентах органического синтеза.
Однако дихлорметан требует осторожного обращения из-за его опасных свойств, таких как воспламеняемость и токсичность. Важно принять надлежащие меры безопасности, в том числе работать в хорошо проветриваемом помещении и носить соответствующие средства индивидуальной защиты при работе с дихлорметаном.
Вопросы:
Вопрос: Полярен ли дихлорметан?
Ответ: Да, дихлорметан является полярным растворителем.
Вопрос: Какие из следующих рисков связаны с дихлорметаном?
Ответ: Опасности, связанные с дихлорметаном, включают его воспламеняемость, токсичность и возможность раздражения кожи и дыхательных путей.
Вопрос: Является ли дихлорметан легковоспламеняющимся?
Ответ: Да, дихлорметан легковоспламеняем и может вызвать пожар или взрыв при воздействии тепла или открытого огня.
Вопрос: Растворяется ли дихлорметан в воде?
Ответ: Да, дихлорметан слабо растворим в воде. Однако он в основном используется в качестве растворителя неполярных соединений и обычно не используется в водных растворах.
