Гептоксид хлора или Cl2O7 — взрывоопасное и реакционноспособное соединение. Он может бурно разлагаться при контакте с органическими веществами и является мощным окислителем, используемым в химическом синтезе и анализе.
| Название ИЮПАК | Гептоксид хлора |
| Молекулярная формула | Cl2O7 |
| Количество CAS | 12015-53-1 |
| Синонимы | Перхлорный ангидрид, гептоксид дихлора, оксид хлора (VII), оксид хлора, перхлорилперхлорат |
| ИнЧИ | InChI=1S/Cl2O7/c2-1(3,4,5,6)10-7(8,9)11-12-13-14-10 |
Молярная масса гептоксида хлора
Гептоксид хлора, химическая формула Cl2O7, имеет молярную массу 182,9 г/моль. Это соединение состоит из двух атомов хлора и семи атомов кислорода, что делает его сильным окислителем. Молярная масса гептоксида хлора используется для расчета количества вещества в заданной массе или объеме образца с использованием константы Авогадро.
Температура кипения гептоксида хлора
Гептоксид хлора представляет собой летучее твердое вещество от бесцветного до желтоватого цвета. Температура кипения гептоксида хлора точно не определена, поскольку он разлагается, не достигнув точки кипения. Гептоксид хлора — мощный окислитель, способный вступать в реакцию с органическими веществами, водой и другими веществами с образованием взрывоопасных соединений.
Температура плавления гептоксида хлора
Гептоксид хлора имеет температуру плавления -96°C (-141°F), что делает его легкоплавким твердым веществом. Гептоксид хлора может существовать в виде желтоватой жидкости при комнатной температуре из-за его низкой температуры плавления и высокой реакционной способности. Важно обращаться с гептоксидом хлора осторожно, поскольку он может вызвать серьезные ожоги и является сильным окислителем.
Плотность гептоксида хлора г/мл
Плотность гептоксида хлора составляет 2,48 г/мл при комнатной температуре. Высокая плотность гептоксида хлора делает его плотной жидкостью, которая может быстро опуститься на дно контейнера. Высокая плотность и реакционная способность гептоксида хлора затрудняют обращение с ним и требуют особых мер безопасности при использовании в химическом синтезе или анализе.
Молекулярный вес гептоксида хлора
Молекулярная масса гептоксида хлора, также известная как относительная молекулярная масса, составляет 182,9 г/моль. Молекулярная масса гептоксида хлора важна в химических расчетах, включающих количество вещества, массу и объем. Высокая молекулярная масса гептоксида хлора делает его плотным и летучим соединением, требующим осторожного обращения и хранения.
Структура гептоксида хлора
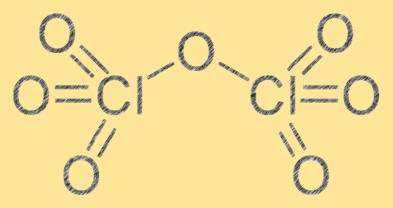
Структура гептоксида хлора состоит из двух атомов хлора и семи атомов кислорода. Он имеет молекулярную формулу Cl2O7, а его молекулярная геометрия представляет собой искаженную октаэдрическую форму из-за отталкивания между атомами кислорода. Гептоксид хлора является сильным окислителем и может реагировать с различными органическими и неорганическими веществами. Структура гептоксида хлора важна для понимания его химических свойств и поведения в различных реакциях.
Формула гептоксида хлора
Химическая формула гептоксида хлора – Cl2O7. Формула указывает, что каждая молекула гептоксида хлора содержит два атома хлора и семь атомов кислорода. Формула используется для расчета стехиометрии химических реакций с участием гептоксида хлора. Формула гептоксида хлора также важна для определения его молекулярной массы, плотности и других физических и химических свойств.
| Появление | Твердое вещество от бесцветного до желтоватого цвета |
| Удельный вес | 2,48 при 25°С |
| Цвет | От бесцветного до желтоватого |
| Запах | Пряный, кислый |
| Молярная масса | 182,9 г/моль |
| Плотность | 2,48 г/мл при 25°C |
| Точка плавления | -96°С (-141°Ф) |
| Точка кипения | Разлагается до точки кипения |
| Мигающая точка | Непригодный |
| Растворимость в воде | Бурно реагирует с водой |
| Растворимость | Растворим в органических растворителях |
| Давление газа | Нет в наличии |
| Плотность пара | Нет в наличии |
| пКа | Нет в наличии |
| рН | Непригодный |
Безопасность и опасность гептоксида хлора
Гептоксид хлора — это высокореактивное и опасное соединение, которое представляет значительную угрозу безопасности при неправильном обращении. При контакте он может вызвать серьезные ожоги и повреждения глаз, кожи и дыхательной системы. Гептоксид хлора также может бурно реагировать с водой и органическими материалами, вызывая взрывы и опасность пожара. При работе с гептоксидом хлора важно использовать соответствующие средства индивидуальной защиты, включая перчатки, очки и респираторы. Состав следует хранить и транспортировать в надежной, плотно закрытой таре, вдали от источников возгорания, тепла и влаги. Чтобы свести к минимуму риски, связанные с гептоксидом хлора, следует соблюдать надлежащие процедуры обращения и меры предосторожности.
| Символы опасности | Окислитель, коррозионный |
| Описание безопасности | Избегайте контакта с водой, кислотами, органическими материалами и восстановителями. Используйте соответствующие средства индивидуальной защиты. Хранить в плотно закрытой таре вдали от источников тепла, влаги и источников возгорания. В случае попадания в глаза, кожу или органы дыхания немедленно обратитесь за медицинской помощью. |
| Идентификационные номера ООН | ООН 3083 |
| код ТН ВЭД | 28299090 |
| Класс опасности | 5.1 (Окисляющие материалы) |
| Группа упаковки | II |
| Токсичность | Очень токсичен при вдыхании, проглатывании или попадании через кожу. Вызывает сильные ожоги и повреждения тканей. Может вызвать взрывы и опасность пожара при контакте с водой, органическими материалами и другими химически активными веществами. |
Методы синтеза гептоксида хлора
Гептоксид хлора — высокореактивное соединение, его трудно синтезировать.
Одним из наиболее распространенных методов синтеза гептоксида хлора является реакция газообразного хлора и озона. Эта реакция является экзотермической и может привести к взрывной реакции, если ее не контролировать тщательно.
Другой метод включает реакцию газообразного хлора с хлоратом калия, в результате которой в качестве побочных продуктов образуются гептоксид хлора и хлорид калия. Этот метод также требует тщательного контроля условий реакции, чтобы предотвратить образование взрывоопасных промежуточных продуктов.
Гептоксид хлора можно синтезировать путем реакции газообразного хлора с пентаоксидом дихлора, в результате чего в качестве побочных продуктов образуются гептоксид хлора и гексоксид дихлора. Однако исследователи обычно не используют этот метод из-за опасной природы пентоксида дихлора.
Другие методы синтеза гептоксида хлора включают реакцию газообразного хлора с различными органическими соединениями, такими как бензол или толуол, в контролируемых условиях. Однако эти методы требуют тщательной оптимизации условий реакции и не так надежны и широко используются, как методы хлор-озон или хлор-хлорат калия.
В целом, синтез гептоксида хлора требует тщательного контроля условий реакции и представляет значительный риск для безопасности из-за высокореактивной природы соединения. При работе с гептоксидом хлора или любыми другими опасными веществами следует соблюдать меры предосторожности и надлежащие процедуры обращения.
Использование гептоксида хлора
- Cl2O7 находит свое основное применение в качестве окислителя в химическом синтезе и исследованиях.
- Он действует как мощный окислитель, реагируя с широким спектром органических и неорганических соединений, что делает его полезным во многих химических реакциях.
- Одним из наиболее распространенных применений Cl2O7 является производство диоксида хлора, мощного дезинфицирующего и отбеливающего средства, используемого при очистке воды, производстве целлюлозы, бумаги и текстиля.
- Он также используется в качестве мощного окислителя в синтезе ряда органических соединений, включая фармацевтические препараты и агрохимикаты.
- Cl2O7 используется в научных кругах и исследованиях для изучения реакционной способности различных органических и неорганических соединений. Он также служит катализатором при синтезе некоторых соединений, таких как эпоксидные смолы и уксусный ангидрид.
- Из-за его опасного характера в крупномасштабных промышленных применениях Cl2O7 обычно не используется. Он требует осторожного обращения и хранения во избежание образования взрывоопасных промежуточных продуктов и других угроз безопасности.
В целом Cl2O7 является полезным соединением в химическом синтезе и исследованиях, но для минимизации рисков, связанных с его использованием, требуются меры предосторожности и надлежащие процедуры обращения.
Вопросы:
Вопрос: Что такое Cl2O7?
Ответ: Cl2O7 представляет собой химическое соединение, состоящее из двух атомов хлора и семи атомов кислорода, с химической формулой Cl2O7.
Вопрос: Как правильно называть Cl2O7?
Ответ: Правильное название Cl2O7 — гептоксид дихлора.
Вопрос: Cl2O7 ионный или ковалентный?
Ответ: Cl2O7 — ковалентное соединение. Он состоит из двух неметаллических элементов, хлора и кислорода, и образует молекулярное соединение за счет обмена электронами между атомами.
Вопрос: Какой оксид ниже реагирует с водой с образованием слабой кислоты? MgO, Cl2O7, P4O10, Bi2O3, N2O5.
Ответ: Оксид, который реагирует с водой с образованием слабой кислоты, — это N2O5. При реакции N2O5 с водой образуется азотная кислота, которая является слабой кислотой. Остальные перечисленные оксиды — MgO, P4O10, Bi2O3 и Cl2O7 — не реагируют с водой с образованием слабых кислот.
