Карбонат-ион CO32- представляет собой отрицательно заряженный ион, состоящий из одного атома углерода, трех атомов кислорода и общим зарядом -2. Он обычно встречается в таких минералах, как кальцит и доломит, а также в водных растворах в виде бикарбоната. Он играет решающую роль в контроле уровня pH в океане и других водоемах.
| Название ИЮПАК | Карбонат-ион |
| Молекулярная формула | CO32- |
| Количество CAS | 497-19-8 |
| Синонимы | Угольная кислота, Триоксид углерода |
| ИнЧИ | InChI=1S/CH2O3.2K/c2-1(3)4;/h(H2,2,3,4);/q;+2/p-2 |
Свойства карбонат-ионов
Карбонатная формула
Формула карбонат-иона представлена CO3^2-, где C представляет собой углерод, O представляет собой кислород, а символ 2- представляет отрицательный заряд иона. Эта формула указывает на то, что в карбонат-ионе имеется три атома кислорода и один атом углерода, что придает ему характерную молекулярную структуру.
Загрузка карбоната CO3
Карбонат-ион CO3^2- имеет отрицательный заряд 2 из-за присутствия в его химической формуле трех атомов кислорода и одного атома углерода. Отрицательный заряд возникает в результате присутствия дополнительных электронов в карбонат-ионе, что делает его отрицательно заряженным ионом.
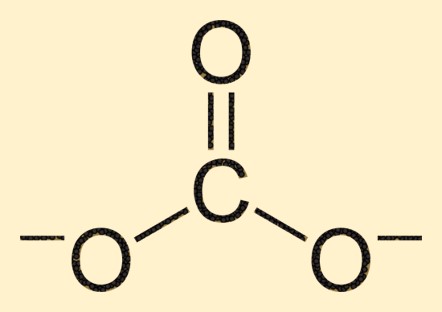
Карбонатная структура
Карбонат-ион состоит из атома углерода в центре, окруженного тремя атомами кислорода в тригональном плоском расположении. Атом углерода образует двойную связь с атомом кислорода, тогда как два других атома кислорода связаны с атомом углерода посредством одинарных связей. Эта структура придает иону CO3 2- характерную форму и свойства.
Карбонат-ион Молекулярный вес
Молекулярная масса карбонат-иона составляет примерно 60,01 г/моль, рассчитанная исходя из атомных масс составляющих его элементов (углерода, кислорода). Молекулярная масса угольной кислоты важна для определения количества угольной кислоты в образце, а также для определения ее физических и химических свойств.
| Появление | Твердый белый порошок |
| Удельный вес | 2,5 |
| Цвет | Белый |
| Запах | Никто |
| Молярная масса | 100,09 г/моль |
| Плотность | 2,83 г/см3 |
| Точка плавления | 825°С |
| Точка кипения | 1484°С |
| Мигающая точка | Непригодный |
| Растворимость в воде | Растворим в воде |
| Растворимость | Растворим в кислотах |
| Давление газа | Непригодный |
| Плотность пара | Непригодный |
| ПКа | 10:33 утра. |
| PH | 8,6 |
Безопасность и опасность карбонат-ионов
Карбонат-ион CO32- широко используется в различных отраслях промышленности, но с ним следует обращаться с осторожностью. Вдыхание большого количества карбонатной пыли может вызвать проблемы с дыханием, а проглатывание ее в больших количествах может вызвать проблемы с пищеварением. Контакт с кожей может вызвать раздражение и повреждение кожи. Он также легковоспламеняем и может вступать в реакцию с другими химическими веществами с образованием опасных газов. Важно соблюдать меры безопасности, такие как ношение средств индивидуальной защиты и хранение ионов карбоната в соответствующих контейнерах, чтобы свести к минимуму риск несчастных случаев.
| Символ опасности | Никто |
| Описание безопасности | Он не считается опасным и не связан с какими-либо конкретными символами опасности. |
| ИН ID | Н/Д |
| код ТН ВЭД | Н/Д |
| Класс опасности | Н/Д |
| Группа упаковки | Н/Д |
| Токсичность | Нетоксичный |
Методы синтеза карбонат-ионов
Карбонат-ионы (CO3 2- ) можно синтезировать множеством различных методов. Наиболее распространенным методом получения ионов CO3 2- является реакция углекислого газа и воды. В результате этой реакции образуется раствор угольной кислоты, который затем можно нейтрализовать щелочью, например гидроксидом натрия, с получением угольной кислоты. Угольную кислоту также можно получить электролизом раствора соли, при котором на катоде образуются ионы карбоната. Эти ионы также можно получить в лаборатории путем химической реакции между кислотой и карбонатной солью.
Использование карбонат-ионов
В промышленности широко используют угольную кислоту для различных целей. Производители разрыхлителей, производители антацидов и компании по производству напитков обычно включают угольную кислоту в свою продукцию. Промышленность водоподготовки контролирует уровень pH в питьевой воде и плавательных бассейнах с помощью ионов карбоната. Строительная индустрия использует ионы CO3 2- в качестве основного компонента цемента для изготовления бетона. Фермеры добавляют ионы карбоната в почву, чтобы улучшить ее щелочность и способствовать росту сельскохозяйственных культур. Химическая промышленность использует карбонат-ионы в качестве катализатора и реагента в различных химических реакциях. Пищевая промышленность сохраняет продукты питания за счет включения ионов карбоната. Благодаря своей универсальности карбонат-ионы играют важную роль во многих повседневных продуктах и промышленных процессах.
