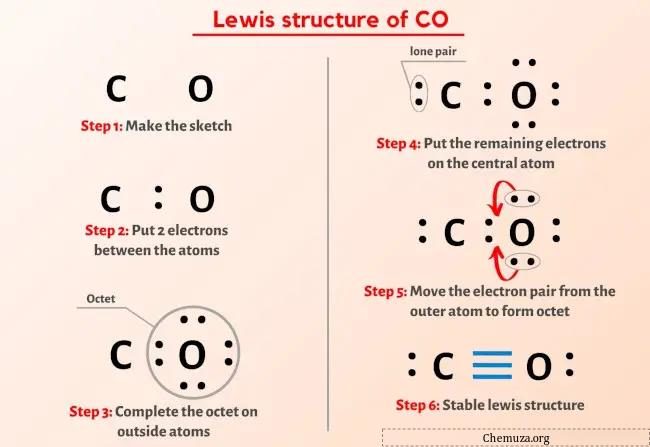
Итак, вы уже видели изображение выше, верно?
Позвольте мне кратко объяснить изображение выше.
Структура CO Льюиса состоит из атома углерода (C) и атома кислорода (O), между которыми имеется тройная связь. У атома углерода (С) и атома кислорода (О) имеется одна неподеленная пара.
Если вы ничего не поняли из приведенного выше изображения структуры Льюиса CO (оксида углерода), оставайтесь со мной, и вы получите подробное пошаговое объяснение того, как нарисовать структуру Льюиса CO .
Итак, давайте перейдем к этапам рисования структуры Льюиса CO.
Шаги по рисованию структуры Льюиса CO
Шаг 1: Найдите общее количество валентных электронов в молекуле CO.
Чтобы найти общее количество валентных электронов в молекуле СО (моноксида углерода) , прежде всего необходимо знать, сколько валентных электронов имеется в отдельном атоме углерода, а также в атоме кислорода.
(Валентные электроны — это электроны, находящиеся на самой внешней орбите любого атома.)
Здесь я расскажу вам, как легко найти валентные электроны углерода, а также кислорода с помощью таблицы Менделеева .
Общее количество валентных электронов в молекуле CO
→ Валентные электроны, отдаваемые атомом углерода:
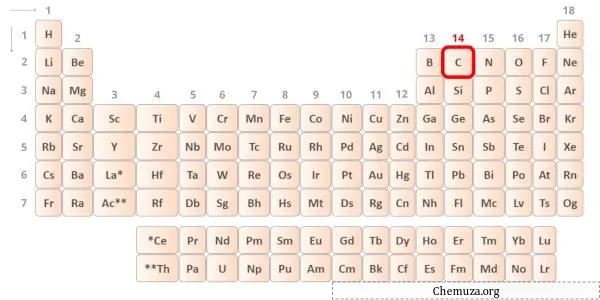
Углерод — элемент 14-й группы таблицы Менделеева. [1] Следовательно, валентные электроны, присутствующие в углероде, равны 4 .
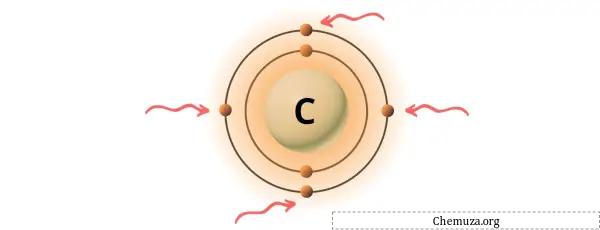
Вы можете увидеть 4 валентных электрона, присутствующих в атоме углерода, как показано на изображении выше.
→ Валентные электроны, отдаваемые атомом кислорода:

Кислород — элемент 16-й группы таблицы Менделеева. [2] Следовательно, валентные электроны, присутствующие в кислороде, равны 6 .
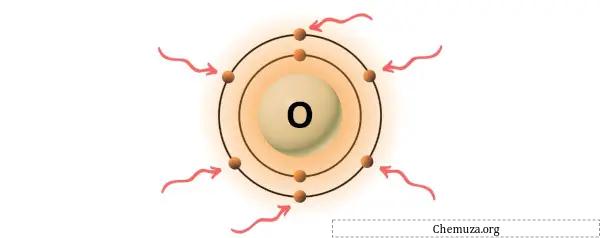
Вы можете увидеть 6 валентных электронов, присутствующих в атоме кислорода, как показано на изображении выше.
Так,
Общее количество валентных электронов в молекуле CO = валентные электроны, пожертвованные 1 атомом углерода + валентные электроны, подаренные 1 атомом кислорода = 4 + 6 = 10 .
Шаг 2: Выберите центральный атом
Чтобы выбрать центральный атом, надо помнить, что в центре остается наименее электроотрицательный атом.
Здесь данной молекулой является CO (окись углерода). В нем всего два атома, поэтому вы можете выбрать любой из них в качестве центрального атома.

Предположим, что атом углерода является центральным атомом.
(Вы должны считать наименее электроотрицательный атом центральным атомом).
Шаг 3: Соедините каждый атом, поместив между ними пару электронов.
Теперь в молекуле СО нужно разместить электронные пары между атомом углерода (С) и атомом кислорода (О).

Это указывает на то, что атом углерода (С) и атом кислорода (О) химически связаны друг с другом в молекуле CO.
Шаг 4: Сделайте внешние атомы стабильными. Поместите оставшуюся пару валентных электронов на центральный атом.
На этом этапе вам необходимо проверить стабильность внешнего атома.
Здесь на схеме молекулы СО мы предположили, что атом углерода является центральным атомом. Таким образом, кислород является внешним атомом.
Поэтому вам нужно сделать атом кислорода стабильным.
На изображении ниже вы можете видеть, что атом кислорода образует октет и поэтому стабилен.
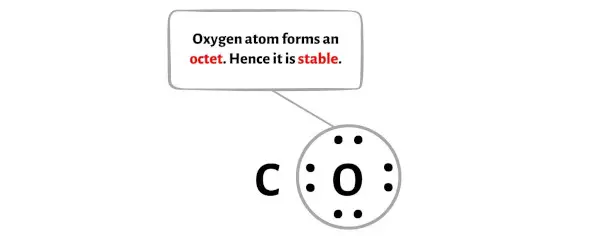
Дополнительно на шаге 1 мы рассчитали общее количество валентных электронов, присутствующих в молекуле CO.
Молекула CO имеет всего 10 валентных электронов , из них на диаграмме выше используются только 8 валентных электронов .
Таким образом, количество оставшихся электронов = 10 – 8 = 2 .
Вам нужно поместить эти 2 электрона на атом углерода на схеме молекулы CO выше.

Теперь перейдем к следующему шагу.
Шаг 5: Проверьте октет центрального атома. Если у него нет октета, переместите неподеленную пару, чтобы сформировать двойную или тройную связь.
На этом этапе вам нужно проверить, стабилен ли центральный атом углерода (С) или нет.
Чтобы проверить стабильность этого атома углерода (С), мы должны проверить, образует ли он октет или нет.
К сожалению, здесь этот атом углерода не образует октет. У углерода всего 4 электрона, и он нестабилен.

Теперь, чтобы сделать этот атом углерода стабильным, вам нужно переместить электронную пару от атома кислорода.
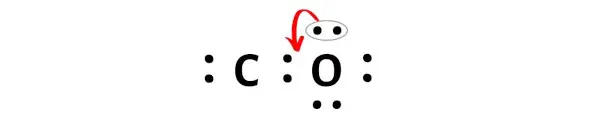
Но после перемещения пары электронов атом углерода все равно не образует октет, поскольку у него всего 6 электронов.

Опять же, нам нужно отодвинуть лишнюю пару электронов от атома кислорода.
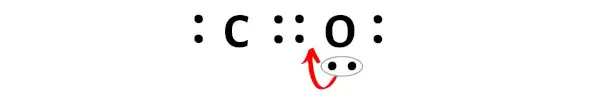
После перемещения этой пары электронов атом углерода получит еще 2 электрона, и, таким образом, общее количество электронов станет 8.
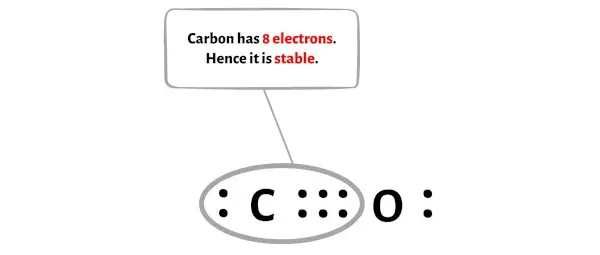
На изображении выше вы можете видеть, что атом углерода и атом кислорода образуют октет.
Следовательно, указанная выше точечная структура Льюиса молекулы CO стабильна.
В приведенной выше точечной структуре Льюиса CO вы также можете представить каждую пару связывающих электронов (:) как одинарную связь (|). Это приведет к следующей структуре Льюиса CO.
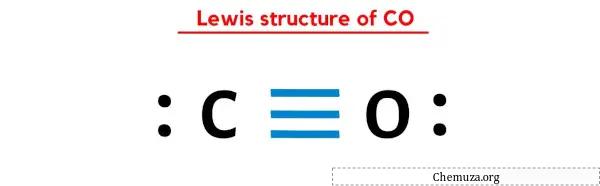
Надеюсь, вы полностью поняли все шаги, описанные выше.
Для большей практики и лучшего понимания вы можете попробовать другие структуры Льюиса, перечисленные ниже.
Попробуйте (или хотя бы посмотрите) эти структуры Льюиса для лучшего понимания:
