Итак, вы уже видели изображение выше, верно?
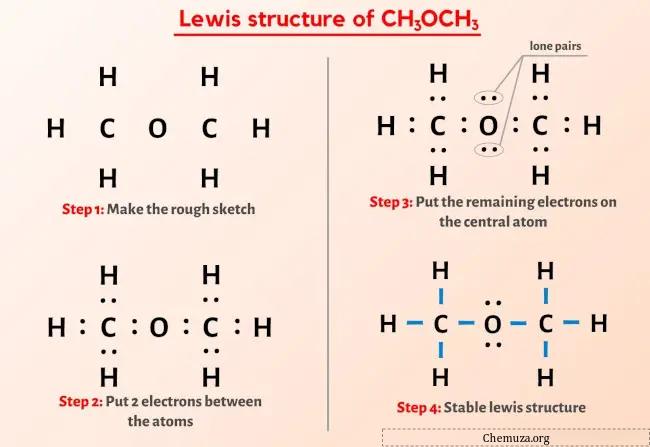
Позвольте мне кратко объяснить изображение выше.
Структура Льюиса CH3OCH3 имеет одинарную связь между атомами углерода и кислорода, а также между атомом углерода (C) и атомом водорода (H). У атома кислорода (О) имеются 2 неподеленные пары.
Если вы ничего не поняли из приведенного выше изображения структуры Льюиса CH3OCH3, оставайтесь со мной, и вы получите подробное пошаговое объяснение рисования структуры Льюиса CH3OCH3 .
Итак, давайте перейдем к этапам рисования структуры Льюиса CH3OCH3.
Шаги по рисованию структуры Льюиса CH3OCH3
Шаг 1: Найдите общее количество валентных электронов в молекуле CH3OCH3.
Чтобы найти общее количество валентных электронов в молекуле CH3OCH3, сначала необходимо узнать количество валентных электронов, присутствующих в атоме углерода , атоме водорода, а также атоме кислорода.
(Валентные электроны — это электроны, находящиеся на самой внешней орбите любого атома.)
Здесь я расскажу вам, как легко найти валентные электроны углерода, водорода, а также кислорода с помощью таблицы Менделеева.
Сумма валентных электронов в молекуле CH3OCH3
→ Валентные электроны, отдаваемые атомом углерода:
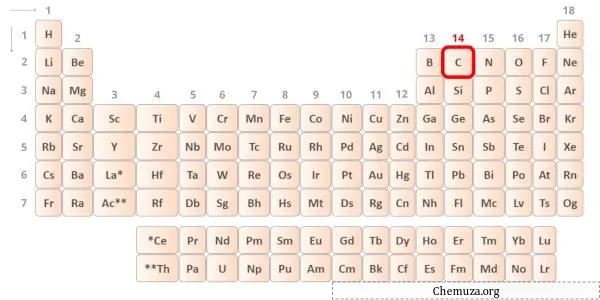
Углерод — элемент 14-й группы таблицы Менделеева. [1] Следовательно, валентные электроны, присутствующие в углероде, равны 4 .
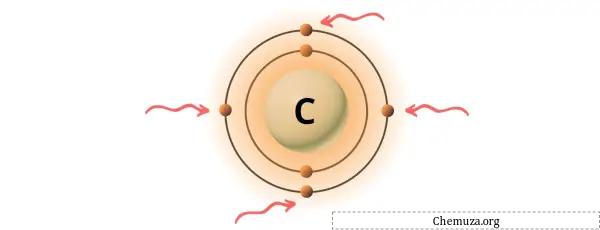
Вы можете увидеть 4 валентных электрона, присутствующих в атоме углерода, как показано на изображении выше.
→ Валентные электроны, отдаваемые атомом водорода:
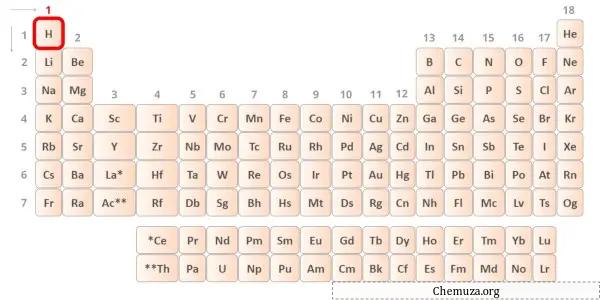
Водород — элемент 1 группы таблицы Менделеева.[2] Следовательно, валентный электрон, присутствующий в водороде, равен 1 .

Вы можете видеть, что в атоме водорода присутствует только один валентный электрон, как показано на изображении выше.
→ Валентные электроны, отдаваемые атомом кислорода:

Кислород — элемент 16-й группы таблицы Менделеева. [3] Следовательно, валентные электроны, присутствующие в кислороде, равны 6 .
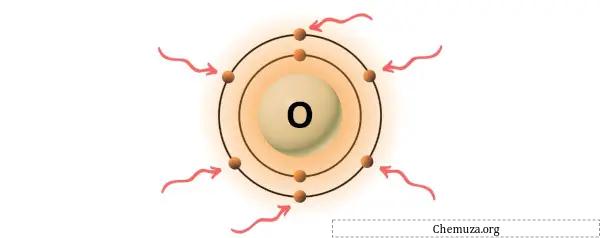
Вы можете увидеть 6 валентных электронов, присутствующих в атоме кислорода, как показано на изображении выше.
Так,
Общее количество валентных электронов в молекуле CH3OCH3 = валентные электроны, пожертвованные 2 атомами углерода + валентные электроны, подаренные 6 атомами водорода + валентные электроны, подаренные 1 атомом кислорода = 4(2) + 1(6) + 6 = 20 .
Шаг 2: Подготовьте эскиз
Чтобы нарисовать схему молекулы CH3OCH3, просто посмотрите на ее химическую формулу. Вы можете видеть, что в центре находится атом кислорода (O), окруженный с обеих сторон CH3.
Итак, давайте сделаем приблизительный набросок того же самого.
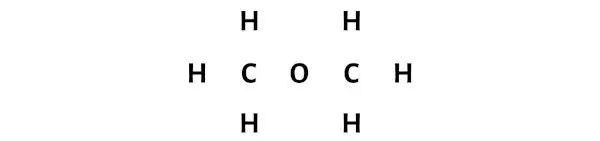
Шаг 3: Соедините каждый атом, поместив между ними пару электронов.
Теперь в молекуле CH3OCH3 нужно разместить электронные пары между атомами углерода (С) и кислорода (О), а также между атомами углерода (С) и водорода (Н).
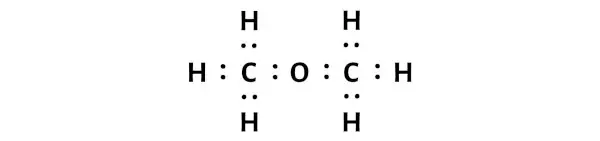
Это указывает на то, что эти атомы химически связаны друг с другом в молекуле CH3OCH3.
Шаг 4: Поместите оставшуюся пару валентных электронов на центральный атом.
На приведенном выше рисунке CH3OCH3 вы можете видеть, что внешние атомы представляют собой атомы водорода и они стабильны, поскольку образуют дуплет.
Теперь, на шаге 1, мы рассчитали общее количество валентных электронов, присутствующих в молекуле CH3OCH3.
Молекула CH3OCH3 имеет всего 20 валентных электронов , из них на диаграмме выше используются только 16 валентных электронов .
Таким образом, количество оставшихся электронов = 20 – 16 = 4 .
Вам нужно разместить эти 4 электрона на центральном атоме кислорода на диаграмме выше молекулы CH3OCH3.
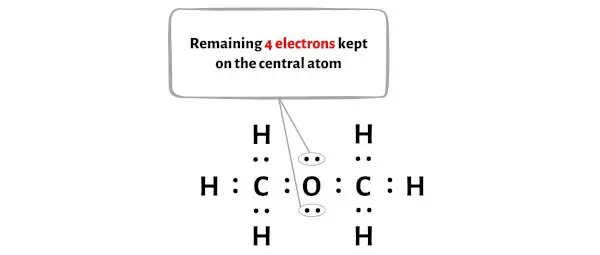
Теперь вы можете видеть, что на диаграмме выше все атомы стабильны (поскольку атомы водорода образуют дублеты , а атомы углерода и кислорода образуют октет).
Таким образом, указанная выше структура Льюиса CH3OCH3 стабильна.
В приведенной выше точечной структуре Льюиса CH3OCH3 вы также можете представить каждую пару связывающих электронов (:) как одинарную связь (|). В результате получится следующая структура Льюиса CH3OCH3.
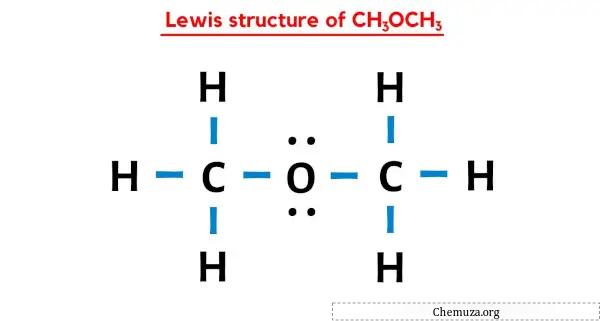
Надеюсь, вы полностью поняли все шаги, описанные выше.
Для большей практики и лучшего понимания вы можете попробовать другие структуры Льюиса, перечисленные ниже.
Попробуйте (или хотя бы посмотрите) эти структуры Льюиса для лучшего понимания:
