Карбонат цинка (ZnCO3) представляет собой белое твердое вещество без запаха, образующееся в результате реакции цинка с ионами карбоната. Благодаря своим уникальным свойствам он используется в различных областях, например, в керамике и фармацевтике.
| Название ИЮПАК | Цинк карбонат |
| Молекулярная формула | ZnCO3 |
| Количество CAS | 3486-35-9 |
| Синонимы | карбонат цинка(II); Смитсонит; Газированный цинк; Цинк карбонат |
| ИнЧИ | InChI=1S/CH2O3.Zn/c2-1(3)4;/h(H2,2,3,4);/q;+2/p-2 |
Свойства карбоната цинка
Формула карбоната цинка
Химическая формула карбоната цинка — ZnCO3. Он состоит из одного атома цинка (Zn), одного атома углерода (С) и трех атомов кислорода (О). Это соединение представляет собой белое твердое вещество без запаха и обычно встречается в природе как минерал смитсонит.
карбонат цинка Молярная масса
Молярную массу карбоната цинка можно рассчитать путем сложения атомных масс составляющих его элементов. Цинк имеет молярную массу примерно 65,38 г/моль, углерод 12,01 г/моль и кислород 16,00 г/моль (приблизительно). Таким образом, молярная масса карбоната цинка составляет примерно 125,38 г/моль.
Температура кипения карбоната цинка
Карбонат цинка не имеет четкой точки кипения, поскольку при нагревании он разлагается, выделяя углекислый газ и оставляя после себя оксид цинка (ZnO). Однако он стабилен до температуры около 300°C.
Температура плавления карбоната цинка
Температура плавления карбоната цинка составляет около 333°C (приблизительно). При этой температуре карбонаты цинка подвергаются термическому разложению с образованием оксида цинка и углекислого газа.
Плотность карбоната цинка г/мл
Плотность карбоната цинка составляет примерно 4,398 г/мл (приблизительно). Это значение указывает на то, что карбонат цинка является относительно плотным твердым веществом по сравнению со многими другими соединениями.
Молекулярный вес карбоната цинка
Молекулярная масса карбоната цинка, также называемая молярной массой, составляет примерно 125,38 г/моль. Это масса одного моля молекул карбоната цинка, которая используется в различных химических расчетах.
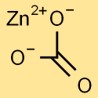
Структура карбоната цинка
Карбонат цинка имеет тригональную кристаллическую структуру. Катион цинка (Zn2+) окружен карбонат-анионами (CO32-) в тригонально-планарном расположении. Такое расположение придает карбонату цинка уникальные физические и химические свойства.
Растворимость карбоната цинка
Карбонат цинка плохо растворяется в воде. Его растворимость уменьшается с понижением температуры и увеличением pH. Он также может растворяться в кислых растворах из-за образования растворимых солей цинка. Однако он образует нерастворимые осадки в присутствии карбонатов или гидроксидов.
| Появление | Белый твердый |
| Удельный вес | 4398 г/мл (приблизительно) |
| Цвет | Белый |
| Запах | Без запаха |
| Молярная масса | 125,38 г/моль |
| Плотность | 4398 г/мл (приблизительно) |
| Точка плавления | 333°С (приблизительно) |
| Точка кипения | Разложившийся |
| Мигающая точка | Непригодный |
| Растворимость в воде | Плохо растворим |
| Растворимость | Нерастворим в большинстве растворителей, также может растворяться в кислых растворах. |
| Давление газа | Нет в наличии |
| Плотность пара | Нет в наличии |
| пКа | Нет в наличии |
| рН | Слабощелочная (около 8-9) |
Безопасность и опасность карбоната цинка
Карбонат цинка представляет определенные риски для безопасности, требующие особого внимания. Он может вызвать раздражение кожи, глаз и дыхательной системы при контакте или вдыхании. Избегайте приема внутрь, так как это может вызвать расстройство желудочно-кишечного тракта. При работе надевайте соответствующие средства индивидуальной защиты, такие как перчатки и очки, чтобы избежать прямого контакта. Храните карбонат цинка в прохладном, сухом месте, вдали от несовместимых веществ. В случае проглатывания или случайного воздействия немедленно обратитесь за медицинской помощью. Кроме того, соблюдайте надлежащие процедуры утилизации этого соединения, чтобы свести к минимуму воздействие на окружающую среду. Правильные методы обращения и хранения необходимы для обеспечения безопасного использования карбоната цинка в различных целях.
| Символы опасности | Никто |
| Описание безопасности | Вреден при проглатывании или вдыхании. Раздражает кожу и глаза. Избегать контакта. Используйте при достаточной вентиляции. |
| Идентификационные номера ООН | Непригодный |
| код ТН ВЭД | 28369900 |
| Класс опасности | Неклассифицированный |
| Группа упаковки | Непригодный |
| Токсичность | От низкой до умеренной токсичности |
Методы синтеза карбоната цинка
Карбонат цинка можно синтезировать различными методами. Распространенным подходом является взаимодействие оксида цинка (ZnO) с диоксидом углерода (CO2) в присутствии воды или подходящего растворителя. Реакцию можно проводить при контролируемой температуре и давлении, чтобы способствовать образованию карбоната цинка.
Другой метод включает реакцию хлорида цинка (ZnCl2) или сульфата цинка (ZnSO4) с карбонатом натрия (Na2CO3) или карбонатом калия (K2CO3) в водном растворе. В результате этого процесса образуется карбонат цинка в виде осадка, который можно отделить и собрать.
Кроме того, карбонат цинка можно получить карбонизацией гидроксида цинка (Zn(OH)2) или оксида цинка диоксидом углерода как в газообразной форме, так и растворенным в воде.
В промышленных условиях карбонат цинка часто образуется как побочный продукт переработки цинка или в результате реакций с участием цинксодержащих материалов.
Для получения чистого и высококачественного продукта очень важно обеспечить правильную стехиометрию и условия реакции во время синтеза. Выбор метода зависит от таких факторов, как наличие реагентов, желаемая чистота продукта и предполагаемое применение карбоната цинка.
Использование карбоната цинка
Карбонат цинка находит разнообразное применение в различных отраслях промышленности благодаря своим уникальным свойствам. Вот некоторые известные варианты использования:
- Керамика: Карбонат цинка активно снижает температуру плавления материалов и улучшает их блеск и прозрачность при использовании в качестве флюса в керамических глазурях.
- Фармацевтика: В медицинских целях карбонат цинка служит активным ингредиентом в некоторых антисептических и вяжущих составах.
- Краски: Карбонат цинка активно действует как белый пигмент в красках и покрытиях, обеспечивая блеск и отличную укрывистость.
- Резиновая промышленность: В процессе вулканизации карбонат цинка действует как ускоритель, активно улучшая механические свойства резиновых изделий.
- Текстильная промышленность: Карбонат цинка в качестве протравы активно улучшает удержание красителей на тканях в процессе крашения.
- Электроника: карбонат цинка находит активное применение в электронных компонентах и в качестве материала для покрытия полупроводников благодаря своим электрическим свойствам.
- Сельское хозяйство: Карбонат цинка активно действует как фунгицид и средство профилактики плесени на сельскохозяйственных культурах.
- Производство стекла. В процессе производства стекла карбонат цинка действует как флюс, активно снижая температуру плавления стекла и улучшая его прозрачность.
- Кормовая добавка для животных. Производители активно добавляют карбонат цинка в корма для животных как важнейший источник незаменимого цинка, который активно поддерживает общее состояние здоровья скота.
- Очистка воды: водоочистные сооружения активно используют карбонат цинка в своих процессах для активного контроля уровня pH и активного удаления примесей тяжелых металлов.
Универсальность карбоната цинка в различных отраслях промышленности подчеркивает его важность как ценного соединения с широким спектром практического применения.
Вопросы:
Вопрос: Растворим ли ZnCO3 в воде?
Ответ: Карбонат цинка плохо растворяется в воде.
Вопрос: Какая реакция наиболее вероятна? Pt + FeCl3 Mn + CaO Li + ZnCO3 Cu + 2KNO3
Ответ: Наиболее вероятная реакция — Li + ZnCO3.
Вопрос: Какая масса ZnCO3 содержит 3,11×10^22 атомов O?
A: Массу ZnCO3, содержащего 3,11×10^22 атомов O, можно рассчитать на основе молярной массы и стехиометрии соединения.
Вопрос: Как называется ZnCO3?
A: Название ZnCO3 — карбонат цинка.
Вопрос: Какое из следующих соединений растворимо в воде? Cu3(PO4)2, CoS, Pb(NO3)2, ZnCO3?
Ответ: ZnCO3 плохо растворяется в воде.
Вопрос: Какой тип связи образуется между ZnCO3?
A: Между ZnCO3 образуются ионные связи.
Вопрос: Растворим ли карбонат цинка в воде?
Ответ: Карбонат цинка плохо растворяется в воде.
Вопрос: Что такое углеродно-цинковый аккумулятор?
Ответ: Угольно-цинковая батарея — это тип сухой батареи, в которой используется цинковый анод и угольный катод с электролитической пастой.
Вопрос: Чем щелочная батарея отличается от сухой углеродно-цинковой батареи?
Ответ: Щелочные батареи имеют более высокую плотность энергии и более длительный срок службы, чем сухие углеродно-цинковые элементы, благодаря использованию щелочного электролита.
Вопрос: В чем разница между углеродно-цинковыми и щелочными батареями?
О: Углеродно-цинковые батареи имеют меньшую энергоемкость и более короткий срок службы, чем щелочные батареи, из-за различий в электролите и конструкции.
Вопрос: Можно ли использовать углеродно-цинковые батарейки вместо щелочных?
О: Да, но углеродно-цинковые батареи могут иметь более короткий срок службы и менее подходят для устройств с высоким потреблением энергии, чем щелочные батареи.
