Хлоросульфоновая кислота — сильная кислота с формулой HSO₃Cl. Он очень агрессивен, используется как реагент в органическом синтезе и как сульфирующий агент при производстве моющих средств и красителей.
| Название ИЮПАК | Хлоросульфоновая кислота |
| Молекулярная формула | HSO₃Cl |
| Количество CAS | 7790-94-5 |
| Синонимы | Серный хлоргидрин, хлорсерная кислота, хлорсульфоновая кислота |
| ИнЧИ | InChI=1S/ClHO3S/c1-5(2,3)4/h(H,2,3,4) |
Свойства хлорсульфоновой кислоты
Формула хлорсульфоновой кислоты
Формула хлорсульфоновой кислоты: HSO₃Cl. Он состоит из одного атома водорода, одного атома серы, трёх атомов кислорода и одного атома хлора.
хлорсульфоновая кислота Молярная масса
Молярную массу хлорсерной кислоты рассчитывают путем сложения атомных масс составляющих ее атомов. Молярная масса HSO₃Cl составляет примерно 116,5 грамм на моль.
Температура кипения хлорсульфоновой кислоты
Температура кипения хлорсерной кислоты относительно высока. Это около 151 градуса по Цельсию (304 градуса по Фаренгейту). При этой температуре хлорсерная кислота переходит из жидкой фазы в газовую.
Хлорсульфоновая кислота Температура плавления
Хлорсерная кислота имеет температуру плавления около -82 градусов по Цельсию (-116 градусов по Фаренгейту). Это температура, при которой твердая форма хлорсерной кислоты превращается в жидкость.
Плотность хлорсульфоновой кислоты г/мл
Хлорсерная кислота имеет плотность примерно 1,75 грамма на миллилитр (г/мл) при комнатной температуре. Это означает, что данный объем хлорсерной кислоты относительно тяжел по сравнению с равным объемом воды.
Хлорсульфоновая кислота Молекулярный вес
Молекулярная масса хлорсерной кислоты рассчитывается путем сложения атомных масс всех атомов ее химической формулы. Хлорсерная кислота имеет молекулярную массу примерно 116,5 грамм на моль.
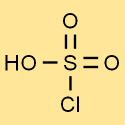
Структура хлорсульфоновой кислоты
Структура хлорсерной кислоты состоит из одного атома серы, связанного с тремя атомами кислорода и одним атомом хлора. Атом водорода присоединен к одному из атомов кислорода. Эта структура придает хлорсерной кислоте ее уникальные свойства и реакционную способность.
Растворимость хлорсульфоновой кислоты
Хлорсерная кислота хорошо растворима в воде. Легко растворяется в воде, образуя сильнокислый раствор. Растворимость хлорсерной кислоты обусловлена ее полярной природой и образованием водородных связей с молекулами воды.
| Появление | Бесцветная или желтая жидкость |
| Удельный вес | 1,75 (при 20°С) |
| Цвет | От бесцветного до желтого |
| Запах | Сильный, резкий запах |
| Молярная масса | 116,5 г/моль |
| Плотность | 1,75 г/мл (при 20°C) |
| Точка плавления | -82°С (-116°Ф) |
| Точка кипения | 151°С (304°Ф) |
| Мигающая точка | Нет в наличии |
| Растворимость в воде | смешивается |
| Растворимость | Растворим в органических растворителях, таких как хлороформ, дихлорметан, нитробензол. |
| Давление газа | Нет в наличии |
| Плотность пара | Нет в наличии |
| пКа | -2,6 |
| рН | Очень кислый (pH < 1) |
Примечание. Имейте в виду, что значения, приведенные в этой таблице, являются общими свойствами, связанными с хлорсерной кислотой. Фактические значения могут незначительно отличаться в зависимости от конкретных условий и чистоты соединения.
Безопасность и опасность хлорсульфоновой кислоты
Хлорсерная кислота представляет значительную угрозу безопасности, и с ней следует обращаться с особой осторожностью. Он очень едкий и может вызвать серьезные ожоги при контакте с кожей, глазами и дыхательной системой. Вдыхание или проглатывание может вызвать серьезные риски для здоровья, включая расстройство дыхания и повреждение внутренних органов. Он бурно реагирует с водой, выделяя токсичные газы и выделяя тепло. Риск пожара и взрыва существует при контакте с органическими материалами. При работе с хлорсерной кислотой следует использовать соответствующие средства индивидуальной защиты, такие как перчатки, очки и респиратор. Надлежащая вентиляция и меры по локализации имеют решающее значение для минимизации воздействия и обеспечения безопасности при обращении с этим опасным веществом.
| Символы опасности | Коррозионный (C), Вредный (Xn) |
| Описание безопасности | – Обращаться с особой осторожностью\n- Использовать соответствующие защитные средства\n- Избегать контакта с кожей, глазами и вдыханиями\n- Хранить в хорошо проветриваемом помещении\n- Не смешивать с водой или химически активными веществами. |
| Идентификационные номера ООН | ООН 1751 |
| код ТН ВЭД | 28121100 |
| Класс опасности | Класс 8 – Коррозионные вещества |
| Группа упаковки | Группа упаковки II |
| Токсичность | Очень токсичен; вызывает серьезные ожоги и повреждения органов дыхания |
Методы синтеза хлорсульфоновой кислоты
Существует несколько методов синтеза хлорсерной кислоты. Обычный метод включает реакцию между триоксидом серы (SO₃) и хлористым водородом (HCl) . В этом процессе раствор HCl барботируется газом SO₃ для получения хлорсерной кислоты. Тщательный контроль температуры и условий реакции необходим из-за высокой экзотермичности реакции.
Другой метод заключается в реакции газообразного хлора (Cl₂) с серной кислотой (H₂SO₄) с образованием хлорсерной кислоты. Прохождение газообразного хлора через концентрированную серную кислоту приводит к образованию хлорсерной кислоты. Для обеспечения безопасности необходимо принять соответствующие меры против этой экзотермической реакции.
Кроме того, получение хлорсерной кислоты включает реакцию серной кислоты с сульфурилхлоридом (SO₂Cl₂). Сульфурилхлорид реагирует с серной кислотой с образованием хлорсерной кислоты и газообразного хлористого водорода.
Следует отметить, что синтез хлорсерной кислоты следует проводить в хорошо оснащенной лаборатории с соблюдением соответствующих протоколов безопасности. Химик должен использовать защитное оборудование, такое как перчатки, очки и капюшон, чтобы обеспечить свою безопасность.
Эти методы синтеза позволяют химикам производить хлорсерную кислоту — универсальное соединение, используемое в различных отраслях промышленности, включая органический синтез, реакции сульфирования, а также производство красителей и моющих средств.
Использование хлорсульфоновой кислоты
Хлорсерная кислота находит широкое применение в различных отраслях промышленности благодаря своим универсальным свойствам. Вот некоторые из его применений:
- Хлорсерная кислота активно участвует в различных реакциях органического синтеза, включая этерификацию, сульфирование и галогенирование, выступая в качестве сильнодействующего реагента. Он эффективно вводит функциональные группы и модифицирует молекулярные структуры.
- В производстве красителей хлорсерная кислота играет решающую роль, поскольку она активно сульфирует ароматические соединения, позволяя создавать сульфокислотные группы. Эти группы улучшают растворимость красителей и улучшают цветовые свойства.
- В производстве моющих средств хлорсерная кислота активно действует как сульфирующий агент при синтезе моющих соединений. Активно способствует образованию ПАВ, улучшая их моющие и пенообразующие свойства.
- Фармацевтическая промышленность широко использует хлорсерную кислоту в качестве активного компонента в исследованиях и производстве. Он активно вводит сульфаниламидные группы в молекулы лекарственных средств, что оказывает существенное влияние на их фармакологические свойства.
- В реакциях полимеризации активно используют хлорсерную кислоту в качестве катализаторов или инициаторов синтеза специальных полимеров. Эти полимеры активно находят применение в различных отраслях промышленности, таких как покрытия, клеи и электроизоляция.
- Он служит важным промежуточным продуктом в производстве различных химикатов, включая сульфоновые кислоты, эфиры серной кислоты и хлорсульфонаты. Эти соединения находят применение в различных отраслях промышленности, таких как фармацевтика, агрохимия и производство полимеров.
- В лаборатории исследователи активно используют хлорсерную кислоту в качестве реагента для различных химических реакций, таких как реакции этерификации, ацилирования и дегидратации.
Важно обращаться с хлорсерной кислотой с осторожностью из-за ее коррозионной природы и потенциального риска для здоровья.
Вопросы:
Вопрос: Как получить ацетамидобензолсульфонилхлорид из ацетанилида и хлорсульфоновой кислоты?
А: Ацетамидобензолсульфонилхлорид образуется при обработке ацетанилида хлорсерной кислотой, что приводит к замене аминогруппы на сульфонилхлоридную группу.
Вопрос: Как использовать хлорсульфоновую кислоту?
Ответ: Хлорсерная кислота используется в качестве реагента в различных химических реакциях, таких как сульфирование, этерификация и ацилирование, для введения функциональных групп или модификации молекулярных структур.
Вопрос: Является ли хлорсульфоновая кислота хорошей уходящей группой?
Ответ: Да, хлорсерная кислота является хорошей уходящей группой из-за стабильности группы сульфоновой кислоты и ее способности подвергаться реакциям замещения.
Вопрос: Как удалить хлорсульфоновую кислоту?
О: Хлорсерную кислоту следует нейтрализовать основанием, например карбонатом натрия, затем разбавить водой и тщательно утилизировать в соответствии с местными правилами.
Вопрос: Что происходит при контакте хлорсульфоновой кислоты с водой?
Ответ: Когда хлорсерная кислота вступает в контакт с водой, она бурно реагирует, выделяя тепло и токсичные газы, такие как диоксид серы и хлористый водород.
Вопрос: Можно ли получить лаурилсульфат натрия заменой хлорсульфоновой кислоты другим реагентом?
Ответ: Да, лаурилсульфат натрия можно синтезировать путем замены хлорсерной кислоты на серную в реакции с лауриловым спиртом с последующей нейтрализацией гидроксидом натрия.
Вопрос: Какова плотность хлорсульфоновой кислоты?
A: Плотность хлорсерной кислоты составляет примерно 1,75 г/мл при комнатной температуре.
Вопрос: Сколько молей хлорсульфоновой кислоты необходимо для получения одного моля ацетамидобензолсульфонилхлорида?
Ответ: Один моль ацетамидобензолсульфонилхлорида можно получить путем взаимодействия одного моля ацетанилида с одним молем хлорсерной кислоты.
Вопрос: Можно ли хранить хлорсульфоновую кислоту вместе с окислителями?
О: Нет, хлорсерную кислоту следует хранить отдельно от окислителей, так как она может бурно реагировать или увеличивать риск возгорания при контакте с окислителями.
